(1)将4.6g钠投入到___ g水中,才能使溶液中的Na+和H2O的个数比为1∶20。钠完全反应后所得溶液的溶质质量分数为___ 。
(2)相同质量的钠、镁、铝与足量的稀盐酸反应时放出的氢气的质量比为___ 。(可以不通分)
(2)相同质量的钠、镁、铝与足量的稀盐酸反应时放出的氢气的质量比为
更新时间:2021-03-14 22:37:11
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)9 g H2O中含有_______ 个H原子。
(2)6.02×1023个OH-的质量为_______ g,含有电子的物质的量为_______ mol。
(3)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为_______ g·mol-1
(4)0.5molCH4的质量是_______ g,在标准状况下的体积为_______ L。
(1)9 g H2O中含有
(2)6.02×1023个OH-的质量为
(3)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为
(4)0.5molCH4的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将14 g Na2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶液的体积为400 mL。试计算:
(1)原混合物中Na2O的质量为_______ g。
(2)所得溶液的物质的量浓度为_______ mol·L-1。
(1)原混合物中Na2O的质量为
(2)所得溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】完成下列问题
(1)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定地方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量,并求出FeClx中x的值_______ (列出计算过程)。
(2)探究小组用滴定法测定CuSO4·5H2O(Mr=250)含量。取ag试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用cmol·L-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL。滴定反应如下:Cu2++H2Y2-=CuY2-+2H+,写出计算CuSO4·5H2O质量分数的表达式ω=_______ 。
(1)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定地方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量,并求出FeClx中x的值
(2)探究小组用滴定法测定CuSO4·5H2O(Mr=250)含量。取ag试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用cmol·L-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL。滴定反应如下:Cu2++H2Y2-=CuY2-+2H+,写出计算CuSO4·5H2O质量分数的表达式ω=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸铜晶体受热脱水是分步进行的。现取1.60gCuSO4·5H2O样品,在隔绝空气条件下受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。
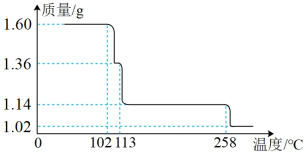
请回答下列问题:
(1)试确定200℃时:①固体物质的化学式___ ;
②写出推断计算过程:___ 。
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉未和一种氧化性气体,该反应的化学方程式为___ 。把该黑色粉未溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为___ ,其存在的最高温度是___ ;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为___ 。

请回答下列问题:
(1)试确定200℃时:①固体物质的化学式
②写出推断计算过程:
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉未和一种氧化性气体,该反应的化学方程式为
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】1774年,瑞典化学家舍勒发现软锰矿(主要成分是 )和浓盐酸混合加热能制取氯气:
)和浓盐酸混合加热能制取氯气: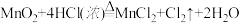 。现将
。现将 含
含 的质量分数为75%的软锰矿石与足量
的质量分数为75%的软锰矿石与足量 浓盐酸完全反应(杂质不参加反应)。
浓盐酸完全反应(杂质不参加反应)。
计算:
(1)参加反应的 的质量
的质量___________ 
(2)生成的 的体积(标准状况)
的体积(标准状况)___________ 
(3)反应中被氧化的 的物质的量
的物质的量___________ 
(4)参加反应的浓盐酸的体积___________ 
 )和浓盐酸混合加热能制取氯气:
)和浓盐酸混合加热能制取氯气: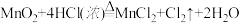 。现将
。现将 含
含 的质量分数为75%的软锰矿石与足量
的质量分数为75%的软锰矿石与足量 浓盐酸完全反应(杂质不参加反应)。
浓盐酸完全反应(杂质不参加反应)。计算:
(1)参加反应的
 的质量
的质量
(2)生成的
 的体积(标准状况)
的体积(标准状况)
(3)反应中被氧化的
 的物质的量
的物质的量
(4)参加反应的浓盐酸的体积

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】一定量的H2在Cl2中燃烧后,所得混合气体用100 mL 3.00 mol/L的NaOH溶液恰好完全吸收,测得溶液中含0.03 mol NaClO(不考虑水解)。氢气和氯气物质的量之比为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
(1)乙组实验中,盐酸_____________ (填“过量”、“适量”或“不足量”),理由是_________ 。
(2)要计算盐酸的物质的量浓度,题中可做计算依据的是____ 。
(3)合金中Mg、Al的物质的量之比为_________________ 。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,求所加NaOH溶液的体积。(写出计算过程)_____________
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
(1)乙组实验中,盐酸
(2)要计算盐酸的物质的量浓度,题中可做计算依据的是
(3)合金中Mg、Al的物质的量之比为
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,求所加NaOH溶液的体积。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将一定质量的镁和铝的混合物投入100mL盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
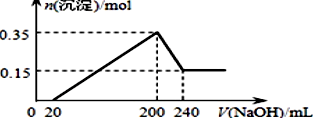
(1)原混合液中镁和铝的质量比为___________
(2)NaOH溶液的物质的量浓度为__________ mol/L。
(3)生成的气体在标准状况下的体积为_________ L。

(1)原混合液中镁和铝的质量比为
(2)NaOH溶液的物质的量浓度为
(3)生成的气体在标准状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】实验研究发现, 发生氧化还原反应时,
发生氧化还原反应时, 溶液的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入
溶液的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入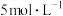 的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量的关系如图所示。
的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量的关系如图所示。

(1)b与a的差值为______________________ 。
(2)C点对应的NaOH溶液的体积为__________ mL。
(3)原稀硝酸中所含 的物质的量为
的物质的量为__________ mol。
(4)铝粉和铁粉的混合物中铝粉与铁粉的物质的量之比为________________ 。
(5)写出铝与该浓度的稀硝酸反应的离子方程式:________________________________________ 。
 发生氧化还原反应时,
发生氧化还原反应时, 溶液的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入
溶液的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入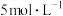 的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量的关系如图所示。
的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量的关系如图所示。
(1)b与a的差值为
(2)C点对应的NaOH溶液的体积为
(3)原稀硝酸中所含
 的物质的量为
的物质的量为(4)铝粉和铁粉的混合物中铝粉与铁粉的物质的量之比为
(5)写出铝与该浓度的稀硝酸反应的离子方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】将镁、铝的混合物0.1 mol溶于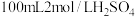 溶液中,然后再滴加1mol/L的NaOH溶液,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示
溶液中,然后再滴加1mol/L的NaOH溶液,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示
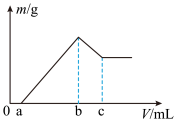
计算:
(1)当a =160mL时,金属混合物中n(Mg)=_____ mol,n(Al)=______ mol,c =______ mL;
(2)若欲使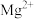 、
、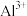 刚好完全沉淀,则加入的NaOH的体积V应为
刚好完全沉淀,则加入的NaOH的体积V应为______ 毫升?
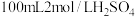 溶液中,然后再滴加1mol/L的NaOH溶液,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示
溶液中,然后再滴加1mol/L的NaOH溶液,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示
计算:
(1)当a =160mL时,金属混合物中n(Mg)=
(2)若欲使
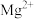 、
、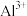 刚好完全沉淀,则加入的NaOH的体积V应为
刚好完全沉淀,则加入的NaOH的体积V应为
您最近一年使用:0次



