计算:
(1)3.6 g H2O的物质的量是_______ mol,含有_______ mol质子。
(2)22 g CO2在标准状况下的体积是_______ L。
(3)10.6 g Na2CO3固体溶于水配成100 mL溶液,其物质的量浓度为_______ mol/L。将其稀释至1000 mL,其物质的量浓度为_______ mol/L。
(4)现有200 mL0.27 kg的质量分数为10%的CuCl2溶液。计算:溶液中CuCl2物质的量浓度为_______ 。
(1)3.6 g H2O的物质的量是
(2)22 g CO2在标准状况下的体积是
(3)10.6 g Na2CO3固体溶于水配成100 mL溶液,其物质的量浓度为
(4)现有200 mL0.27 kg的质量分数为10%的CuCl2溶液。计算:溶液中CuCl2物质的量浓度为
更新时间:2021-03-19 21:03:24
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】填空。
(1) 的摩尔质量为
的摩尔质量为_______ ;96g 中含有
中含有_______ 个 ,所含电子的物质的量为
,所含电子的物质的量为_______ 。
(2)0.5mol 加入适量水中配成2L溶液,则溶质的物质的量浓度是
加入适量水中配成2L溶液,则溶质的物质的量浓度是_______ 。
(3)标况下44.8LHCl气体与_______ g 中所含氢原子总数相等。
中所含氢原子总数相等。
(1)
 的摩尔质量为
的摩尔质量为 中含有
中含有 ,所含电子的物质的量为
,所含电子的物质的量为(2)0.5mol
 加入适量水中配成2L溶液,则溶质的物质的量浓度是
加入适量水中配成2L溶液,则溶质的物质的量浓度是(3)标况下44.8LHCl气体与
 中所含氢原子总数相等。
中所含氢原子总数相等。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将 4.6g 金属钠投入一定量的水中,待反应完毕后,得到 100mL 溶液.求:
(1)标准状况下产生氢气多少 mL_______________ ?
(2)所得溶液的物质的浓度是多少_____________ ?
(1)标准状况下产生氢气多少 mL
(2)所得溶液的物质的浓度是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】已知3.25g金属Zn恰好与250mL某浓度的盐酸完全反应,计算:
(1)该盐酸的物质的量浓度;___________
(2)标准状况下,该反应生成的气体的体积。_____________
(1)该盐酸的物质的量浓度;
(2)标准状况下,该反应生成的气体的体积。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)0.5 mol CH4的质量是____ ,在标准状况下的体积为____ 。
(2) 3.1 g Na2X含有Na+ 0.1mol,则Na2X的摩尔质量为___ ,X的相对原子质量为___ 。
(3)0.6 mol的氧气与0.4 mol臭氧 O3质量之比为____ ,分子个数之比为___ , 氧原子个数之比为____ 。
(4)8.5g氢氧根离子含有的电子数目为____ 。
(5)将6.5 g锌投入200 mL某浓度的稀盐酸中,锌和稀盐酸恰好完全反应。则所用稀盐酸中HCl的物质的量浓度为____ ; 反应中生成的H2在标准状况下的体积为___ ;若向反应后的溶液中加水至500 mL,则此时氯化锌的物质的量浓度为_____ 。
(2) 3.1 g Na2X含有Na+ 0.1mol,则Na2X的摩尔质量为
(3)0.6 mol的氧气与0.4 mol臭氧 O3质量之比为
(4)8.5g氢氧根离子含有的电子数目为
(5)将6.5 g锌投入200 mL某浓度的稀盐酸中,锌和稀盐酸恰好完全反应。则所用稀盐酸中HCl的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】填空
(1)标准状况下有①44.8LCH4,② 个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是
个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是______ 。
(2)40.5g某金属氯化物MCl2中含有0.6molCl-,则M的相对原子质量为______ 。
(3)amLAl2(SO4)3溶液中含 bg,则溶液中Al3+的物质的量浓度
bg,则溶液中Al3+的物质的量浓度______ 。
(4)将一定量的CO2和SO2混合,测得混合气体中碳元素和硫元素的质量之比为3∶8,则该混合气体中CO2与SO2的物质的量之比为______ ,该混合气体的密度是同温同压下氢气密度的______ 倍。
(5)把VL含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含bmolBaCl2的溶液,恰好使 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为______ 。
(1)标准状况下有①44.8LCH4,②
 个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是
个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是(2)40.5g某金属氯化物MCl2中含有0.6molCl-,则M的相对原子质量为
(3)amLAl2(SO4)3溶液中含
 bg,则溶液中Al3+的物质的量浓度
bg,则溶液中Al3+的物质的量浓度(4)将一定量的CO2和SO2混合,测得混合气体中碳元素和硫元素的质量之比为3∶8,则该混合气体中CO2与SO2的物质的量之比为
(5)把VL含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含bmolBaCl2的溶液,恰好使
 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
您最近一年使用:0次

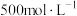 硫酸溶液吸收放出的氨,剩余的酸用38.0mL
硫酸溶液吸收放出的氨,剩余的酸用38.0mL 氢氧化钠溶液可恰好完全中和。
氢氧化钠溶液可恰好完全中和。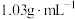 )
)


