填空
(1)标准状况下有①44.8LCH4,② 个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是
个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是______ 。
(2)40.5g某金属氯化物MCl2中含有0.6molCl-,则M的相对原子质量为______ 。
(3)amLAl2(SO4)3溶液中含 bg,则溶液中Al3+的物质的量浓度
bg,则溶液中Al3+的物质的量浓度______ 。
(4)将一定量的CO2和SO2混合,测得混合气体中碳元素和硫元素的质量之比为3∶8,则该混合气体中CO2与SO2的物质的量之比为______ ,该混合气体的密度是同温同压下氢气密度的______ 倍。
(5)把VL含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含bmolBaCl2的溶液,恰好使 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为______ 。
(1)标准状况下有①44.8LCH4,②
 个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是
个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是(2)40.5g某金属氯化物MCl2中含有0.6molCl-,则M的相对原子质量为
(3)amLAl2(SO4)3溶液中含
 bg,则溶液中Al3+的物质的量浓度
bg,则溶液中Al3+的物质的量浓度(4)将一定量的CO2和SO2混合,测得混合气体中碳元素和硫元素的质量之比为3∶8,则该混合气体中CO2与SO2的物质的量之比为
(5)把VL含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含bmolBaCl2的溶液,恰好使
 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
更新时间:2023-12-19 19:33:57
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】O2和O3是氧元素的两种单质,根据其化学式完成下列各题:
(1)等质量的O2和O3原子个数比为_______________ 。等温等压下,等体积的O2和O3所的质量比为___________ 。
(2)设NA为阿伏加 德罗常数的数值,如果ag氧气中含有的分子数为b,则cg氧气在标准状况下的体积约是_____________ L(用含NA的式子表示)。
(3)已知CO、O2两种气体的混和气体的密度在相同条件下是氢气的15倍,则该混和气体的平均相对分子质量为_____ 。
(4)实验室需要配制920mL1mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为____ mL。
(1)等质量的O2和O3原子个数比为
(2)设NA为阿伏加 德罗常数的数值,如果ag氧气中含有的分子数为b,则cg氧气在标准状况下的体积约是
(3)已知CO、O2两种气体的混和气体的密度在相同条件下是氢气的15倍,则该混和气体的平均相对分子质量为
(4)实验室需要配制920mL1mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某同学利用下图所示的装置进行实验(实验条件下气体摩尔体积为Vm),实验开始前各活塞均关闭(两烧瓶容积相同)。

(1)同温同压下,两个烧瓶内HCl与NH3分子数目之比为_______ ,烧瓶Ⅱ中喷泉的颜色是____________ 。
(2)实验结束后烧瓶I中c(Cl- ) =_________ mol•L-1。
(3)实验表明,若只是关闭b、打开a、c,则易在烧瓶I中观察到白烟,这表明气体分子扩散速率随着气体相对分子质量的增大而_____ (填“增大”或“减小”)

(1)同温同压下,两个烧瓶内HCl与NH3分子数目之比为
(2)实验结束后烧瓶I中c(Cl- ) =
(3)实验表明,若只是关闭b、打开a、c,则易在烧瓶I中观察到白烟,这表明气体分子扩散速率随着气体相对分子质量的增大而
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】化学计量是化学学习的工具,请回答下列问题:
(1)标准状况下,1.7gNH3与__ LH2S气体含有的氢原子数相同。
(2)VmLAl2(SO4)3溶液中含Al3+ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中SO42-的物质的量浓度是___ mol/L。
(3)常温常压下22.4LCO2中分子个数__ 64克SO2的分子个数(填“>”、“<”或“=”)。
(4)标准状况下,33.6L的NH3所含电子的物质的量约为__ mol。
(5)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为__ 。
(6)某盐混合溶液含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO42-)=___ 。
(7)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为___ ,NH3的体积分数(即NH3的体积与混合气体总体积的比值)为__ 。
(1)标准状况下,1.7gNH3与
(2)VmLAl2(SO4)3溶液中含Al3+ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中SO42-的物质的量浓度是
(3)常温常压下22.4LCO2中分子个数
(4)标准状况下,33.6L的NH3所含电子的物质的量约为
(5)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为
(6)某盐混合溶液含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO42-)=
(7)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】在无土栽培中,需配制一定组成的植物营养液。已知某植物营养液的配方为0.3molKCl、0.2molK2SO4、0.1molZnSO4和1LH2O。若以KCl、K2SO4、ZnCl2和1LH2O为原料,需三种溶质各多少克_________ ?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】分别称取2.12g (NH4)2SO4和NH4NO3固体混合物两份
(1)将其中一份配成溶液,逐滴加入一定浓度的 Ba(OH)2 溶液,产生的沉淀质量m/g与加入Ba(OH)2 溶液体积的关系如图.混合物中 n[(NH4)2SO4]:n(NH4NO3)为_____ 。
(2)另一份固体混合物中 NH 与 Ba(OH)2 溶液(浓度同上)恰好完全反应时,溶液中 c(NO
与 Ba(OH)2 溶液(浓度同上)恰好完全反应时,溶液中 c(NO )=
)=_____ (溶液体积变化忽略不计,保留小数点后面 3 位)。
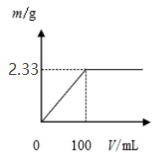
(1)将其中一份配成溶液,逐滴加入一定浓度的 Ba(OH)2 溶液,产生的沉淀质量m/g与加入Ba(OH)2 溶液体积的关系如图.混合物中 n[(NH4)2SO4]:n(NH4NO3)为
(2)另一份固体混合物中 NH
 与 Ba(OH)2 溶液(浓度同上)恰好完全反应时,溶液中 c(NO
与 Ba(OH)2 溶液(浓度同上)恰好完全反应时,溶液中 c(NO )=
)=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积______ 。
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为______ 。
(3)标准状况下,1.7gNH3与______ LH2S气体含有的氢原子数相同,
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L该混合气体中NH3的体积分数为______ ,该混合气体对氢气的相对密度为______ 。
(1)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为
(3)标准状况下,1.7gNH3与
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L该混合气体中NH3的体积分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】根据所学知识填空(NA表示阿伏加德罗常数的值):
(1)98gH2SO4的物质的量是___________ mol,含有___________ g H原子。
(2)约1.204×1024个CO的物质的量是___________ mol;与___________ molNa2O2含有的氧原子数相等。
(3)标准状况下,67.2LCO2是_______ mol,质量为_______ g,含有______ 个CO2分子,含有___________ mol氧原子。
(1)98gH2SO4的物质的量是
(2)约1.204×1024个CO的物质的量是
(3)标准状况下,67.2LCO2是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)6.02×1023个氢氧根离子的物质的量是________ mol,其摩尔质量为________ 。
(2)3.01×1023个H2O的物质的量为________ mol,其中,所有原子的物质的量为________ mol,所含电子的物质的量为________ mol。
(3)标准状况下,2 mol O2 的体积是________ ;标准状况下,11.2 L O2的质量是________ 含有的氧气分子数目是________ ;含有的氧原子数目是________ 。
(2)3.01×1023个H2O的物质的量为
(3)标准状况下,2 mol O2 的体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】在0.2 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题

(1)该混合液中,NaCl的物质的量为_________ mol,含溶质MgCl2的质量为_______ g。
(2)该混合液中CaCl2的物质的量为___________ mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为__________ mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________ mol。

(1)该混合液中,NaCl的物质的量为
(2)该混合液中CaCl2的物质的量为
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在 300 mL 2 mol/L H2SO4溶液中,SO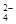 的物质的量浓度是多少?H+的物质的量浓度是多少?溶质的质量是多少?此溶液中含 H+的物质的量是少?其中含有多少个 SO
的物质的量浓度是多少?H+的物质的量浓度是多少?溶质的质量是多少?此溶液中含 H+的物质的量是少?其中含有多少个 SO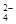 ?
?
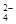 的物质的量浓度是多少?H+的物质的量浓度是多少?溶质的质量是多少?此溶液中含 H+的物质的量是少?其中含有多少个 SO
的物质的量浓度是多少?H+的物质的量浓度是多少?溶质的质量是多少?此溶液中含 H+的物质的量是少?其中含有多少个 SO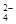 ?
?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1 mol·L-1,加入等体积0.3 mol·L-1的BaCl2溶液恰好使 完全沉淀,则混合溶液中Na+的浓度为
完全沉淀,则混合溶液中Na+的浓度为________ 。
(2)将0.1 mol·L-1的K2SO4溶液、0.2 mol·L-1的Al2(SO4)3溶液和纯水混合,要使混合液中K+、Al3+、 的浓度分别为0.1 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,则K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比
的浓度分别为0.1 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,则K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比________ (忽略体积的变化)。
(3)在标准状况下,将一个充满HCl气体和氧气的集气瓶倒放于盛水的水槽中,水面上升至集气瓶容积的 ,把集气瓶从水中取出(假设HCl全部留在集气瓶中),若溶液密度的变化忽略不计,则HCl的物质的量浓度为
,把集气瓶从水中取出(假设HCl全部留在集气瓶中),若溶液密度的变化忽略不计,则HCl的物质的量浓度为________ mol·L-1。
 完全沉淀,则混合溶液中Na+的浓度为
完全沉淀,则混合溶液中Na+的浓度为(2)将0.1 mol·L-1的K2SO4溶液、0.2 mol·L-1的Al2(SO4)3溶液和纯水混合,要使混合液中K+、Al3+、
 的浓度分别为0.1 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,则K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比
的浓度分别为0.1 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,则K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比(3)在标准状况下,将一个充满HCl气体和氧气的集气瓶倒放于盛水的水槽中,水面上升至集气瓶容积的
 ,把集气瓶从水中取出(假设HCl全部留在集气瓶中),若溶液密度的变化忽略不计,则HCl的物质的量浓度为
,把集气瓶从水中取出(假设HCl全部留在集气瓶中),若溶液密度的变化忽略不计,则HCl的物质的量浓度为
您最近一年使用:0次

 的钠块10.8g,将其投入100mL水中,产生标准状况下2.24L气体(溶液体积的变化可以忽略不计)。
的钠块10.8g,将其投入100mL水中,产生标准状况下2.24L气体(溶液体积的变化可以忽略不计)。

