计算:(1)22gCO2的物质的量是__ mol;在标准状况下的体积是__ L。
(2)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是_______ ,X的相对原子质量是_______ 。
(3)2molOH-含有的质子数为_______ 个,电子数为_______ 个。
(4)现有0.27kg的质量分数为10%的CuCl2溶液,则溶液中CuCl2物质的量为_______ ;Cl-的物质的量为_______ 。
(5)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c( )=
)=_______ 。
(2)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是
(3)2molOH-含有的质子数为
(4)现有0.27kg的质量分数为10%的CuCl2溶液,则溶液中CuCl2物质的量为
(5)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c(
 )=
)=
更新时间:2021-03-20 09:36:34
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)现有8种物质:① ②
② ③浓硫酸④铝⑤
③浓硫酸④铝⑤ 胶体 ⑥蔗糖溶液⑦
胶体 ⑥蔗糖溶液⑦ ⑧
⑧ 上述物质中属于电解质的有
上述物质中属于电解质的有_______ (选填序号);写出②的溶液与⑤反应的离子方程式_______
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,研究人员提出,在碱性条件下可以用铝粉处理
的浓度,研究人员提出,在碱性条件下可以用铝粉处理 ,发生反应的化学方程式为:
,发生反应的化学方程式为: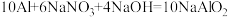
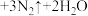 ,该反应中,还原剂为
,该反应中,还原剂为_______ ,若反应过程中转移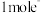 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为_______  。
。
(3)在含有一定量 和
和 溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生
溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生 的物质的量与滴入盐酸的量的关系如图,回答下列问题:
的物质的量与滴入盐酸的量的关系如图,回答下列问题:
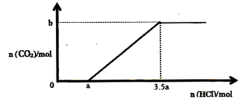
① 点发生反应的离子方程式为
点发生反应的离子方程式为_______
② 与
与 物质的量之比为
物质的量之比为_______
③
_______ (用含 的代数式表示)
的代数式表示)
(4)现有密度为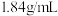 ,浓度为
,浓度为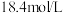 的浓硫酸,则该溶液中溶质的质量分数为
的浓硫酸,则该溶液中溶质的质量分数为_______
 ②
② ③浓硫酸④铝⑤
③浓硫酸④铝⑤ 胶体 ⑥蔗糖溶液⑦
胶体 ⑥蔗糖溶液⑦ ⑧
⑧ 上述物质中属于电解质的有
上述物质中属于电解质的有(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,研究人员提出,在碱性条件下可以用铝粉处理
的浓度,研究人员提出,在碱性条件下可以用铝粉处理 ,发生反应的化学方程式为:
,发生反应的化学方程式为: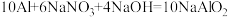
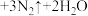 ,该反应中,还原剂为
,该反应中,还原剂为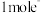 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为 。
。(3)在含有一定量
 和
和 溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生
溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生 的物质的量与滴入盐酸的量的关系如图,回答下列问题:
的物质的量与滴入盐酸的量的关系如图,回答下列问题:
①
 点发生反应的离子方程式为
点发生反应的离子方程式为②
 与
与 物质的量之比为
物质的量之比为③
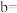
 的代数式表示)
的代数式表示)(4)现有密度为
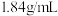 ,浓度为
,浓度为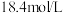 的浓硫酸,则该溶液中溶质的质量分数为
的浓硫酸,则该溶液中溶质的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)在抗击新型冠状病毒疫情中,常常选用“84消毒液”等进行环境消毒,已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
该“84消毒液”的物质的量浓度约为___ mol·L-1。某同学取1L该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=___ mol·L-1。
(2)7.20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为___ 。
| 84消毒液 [有效成分] NaClO [规格] 1000 mL [质量分数] 25% [密度] 1.19 g·cm-3 |
该“84消毒液”的物质的量浓度约为
(2)7.20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下面问题:
(1)下列所给出的几组物质中:标准状况下体积最大的是______ 。(填序号)
①1 g H2;② 个CH4;③10.8 g H2O;④标准状况下6.72 L CO2
个CH4;③10.8 g H2O;④标准状况下6.72 L CO2
(2)在标准状况下51 g CO与CO2的混合气体,体积为28 L,其中CO2的质量为_______ ,CO物质的量为_______ ,该混合气体中CO的物质的量分数为_______ 。
(1)下列所给出的几组物质中:标准状况下体积最大的是
①1 g H2;②
 个CH4;③10.8 g H2O;④标准状况下6.72 L CO2
个CH4;③10.8 g H2O;④标准状况下6.72 L CO2(2)在标准状况下51 g CO与CO2的混合气体,体积为28 L,其中CO2的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】回答下列问题
(1)49 g H2SO4的物质的量是_______ ;1.5 mol H2SO4的质量是_______ ,其中含有_______ molH
(2)已知NH3的相对分子质量为17,则NH3的摩尔质量为_______ 。
(3)标准状况下,16gO2的体积_______ L。
(4)6.02×1023个水分子的物质的量_______ mol。
(1)49 g H2SO4的物质的量是
(2)已知NH3的相对分子质量为17,则NH3的摩尔质量为
(3)标准状况下,16gO2的体积
(4)6.02×1023个水分子的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】有关物质的量的计算填空:
(1)2 mol尿素[CO(NH2)2]含___ 个H原子,所含氧原子跟___ g H2O所含氧原子个数相等。
(2)①标准状况下,22.4L CH4;②1.5mol NH3; ③1.806×1024个H2O;④标准状况下,73gHCl。所含H原子个数由多到少的顺序是_________________ 。
(3)30.9 g NaR含有Na+ 0.3mol,则NaR的摩尔质量为______________ 。
(4)100 mL 某Al2(SO4)3溶液中,c(Al3+) = 2.0 mol/L,则其中c(SO42-) =______ mol/L。
(5)工业上利用下列反应进行海水中溴元素的富集:Br2 + SO2 + 2H2O = H2SO4 + 2HBr。若反应中转移了1 mol电子,则消耗SO2的体积(标准状况)是___________ L。
(1)2 mol尿素[CO(NH2)2]含
(2)①标准状况下,22.4L CH4;②1.5mol NH3; ③1.806×1024个H2O;④标准状况下,73gHCl。所含H原子个数由多到少的顺序是
(3)30.9 g NaR含有Na+ 0.3mol,则NaR的摩尔质量为
(4)100 mL 某Al2(SO4)3溶液中,c(Al3+) = 2.0 mol/L,则其中c(SO42-) =
(5)工业上利用下列反应进行海水中溴元素的富集:Br2 + SO2 + 2H2O = H2SO4 + 2HBr。若反应中转移了1 mol电子,则消耗SO2的体积(标准状况)是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】Ⅰ.现有硫酸和盐酸的混合溶液20mL,在该溶液中滴入0.05mol/L的Ba(OH)2溶液时,生成BaSO4的质量和溶液的pH得到如图所示的结果,求:

⑴最初混合液中硫酸的物质的量浓度____________________
盐酸的物质的量浓度____________________
⑵在A点溶液的pH=____________________ 。
Ⅱ.Ba2+是一种重金属离子,对生物体有害,环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的浓度。
(1)现需配制250mL0.100mol·L—1标准Na2S2O3溶液,所需要的玻璃仪器除量筒、250mL容量瓶、玻璃棒外,还需要_____________________ 。
(2)需准确称取Na2S2O3固体的质量为________________ g。
(3)另取废水50.00mL,控制适当的酸度加入足量的K2Cr2O7溶液,得BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液反应,反应液中再滴加上述Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。
已知有关的离子方程式为:
①Cr2O72-+6I-+14H+ 2Cr3++3I2+7H2O;
②I2+2S2O32- 2I-+S4O62-.试计算该工厂废水中Ba2+的物质的量浓度c(Ba2+)=________________________ 。
Ⅲ.试回答下列问题:
(1)已知24 g A和40 g B恰好完全反应生成0.4 mol C和32 g D,则C的摩尔质量为_________________ 。
(2)把1 mol Na和1 mol Mg分别投入到等量且过量的盐酸中,分别得到溶液a和b,则溶液a和b的质量关系为ma_____________ mb。
(3)如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试根据标签上的有关数据回答下列问题:
①该浓盐酸中HCl的物质的量浓度为____________ mol·L-1。
②标准状况下,1.00 L水(密度为1.00 g·cm-3)吸收_____________ L的HCl可制得上述浓盐酸(保留整数)。

⑴最初混合液中硫酸的物质的量浓度
盐酸的物质的量浓度
⑵在A点溶液的pH=
Ⅱ.Ba2+是一种重金属离子,对生物体有害,环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的浓度。
(1)现需配制250mL0.100mol·L—1标准Na2S2O3溶液,所需要的玻璃仪器除量筒、250mL容量瓶、玻璃棒外,还需要
(2)需准确称取Na2S2O3固体的质量为
(3)另取废水50.00mL,控制适当的酸度加入足量的K2Cr2O7溶液,得BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液反应,反应液中再滴加上述Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。
已知有关的离子方程式为:
①Cr2O72-+6I-+14H+ 2Cr3++3I2+7H2O;
②I2+2S2O32- 2I-+S4O62-.试计算该工厂废水中Ba2+的物质的量浓度c(Ba2+)=
Ⅲ.试回答下列问题:
(1)已知24 g A和40 g B恰好完全反应生成0.4 mol C和32 g D,则C的摩尔质量为
(2)把1 mol Na和1 mol Mg分别投入到等量且过量的盐酸中,分别得到溶液a和b,则溶液a和b的质量关系为ma
(3)如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试根据标签上的有关数据回答下列问题:
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19 g·cm-3 HCl的质量分数:36.5% |
①该浓盐酸中HCl的物质的量浓度为
②标准状况下,1.00 L水(密度为1.00 g·cm-3)吸收
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)1mol HNO3的质量是____________ , 1mol HNO3含有_____ mol氧原子。
(2)标准状况下11.2L HCl气体溶于水中配成1L溶液,所得盐酸溶液的物质的量浓度是_______________ 。
(3)2mol OH 约含有__________________ 个电子。
(4)9.5gMgCl2固体溶于水配成500mL溶液,其中Cl-浓度为________ mol· L-1。
(2)标准状况下11.2L HCl气体溶于水中配成1L溶液,所得盐酸溶液的物质的量浓度是
(3)2mol OH 约含有
(4)9.5gMgCl2固体溶于水配成500mL溶液,其中Cl-浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】在标准状况下,将224LHCl气体溶于635mL水中,所得盐酸的密度为1.18g·cm-3试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是___________ 、___________ 。
(2)取这种盐酸100 mL,稀释至1.18L,所得稀盐酸的物质的量浓度是___________ 。
(3)在40.0 mL 0.065 mol·L-1Na2CO3溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过___________ mL。
(4)将不纯的NaOH样品1g(样品含少量Na2CO3和水),放入50mL2mol·L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL1mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到___________ g固体。
(1)所得盐酸的质量分数和物质的量浓度分别是
(2)取这种盐酸100 mL,稀释至1.18L,所得稀盐酸的物质的量浓度是
(3)在40.0 mL 0.065 mol·L-1Na2CO3溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过
(4)将不纯的NaOH样品1g(样品含少量Na2CO3和水),放入50mL2mol·L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL1mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】按国家规定,每千克食用碘盐中碘的含量在20-50 mg之间,现对某品牌碘盐中碘(以KIO3形式加入)含量的测定:①准确称取食盐100 g,配制成250 mL溶液;②量取上述溶液25.00 mL于锥形瓶中,硫酸酸化后加入足量的KI充分反应;③经调节pH后,用0.001 mol·L-1Na2S2O3溶液滴定,消耗Na2S2O3溶液的体积为18.00 mL。
已知:KIO3+5KI+3H2SO4=3I2+K2SO4+3H2
I2+2Na2S2O3=2NaI+Na2S4O6
(1)所配制的食盐溶液的物质的量浓度为____ mol·L-1。
(2)该品牌食盐中碘的含量为___ mg·kg-1(写出简要的计算过程)。
已知:KIO3+5KI+3H2SO4=3I2+K2SO4+3H2
I2+2Na2S2O3=2NaI+Na2S4O6
(1)所配制的食盐溶液的物质的量浓度为
(2)该品牌食盐中碘的含量为
您最近一年使用:0次

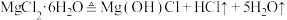 ;
; 。研究人员称取氯化镁晶体ag,经加热后得到固体bg。
。研究人员称取氯化镁晶体ag,经加热后得到固体bg。 、MgO混合物,则a与b的关系是
、MgO混合物,则a与b的关系是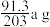 ,则它们的物质的量之比为
,则它们的物质的量之比为 的物质的量浓度为3.0 mol·L−1。请计算:
的物质的量浓度为3.0 mol·L−1。请计算:

