(1)依据反应:Cu2++Zn(s)=Zn2+(aq)+Cu(s)设计的原电池如下图甲所示。
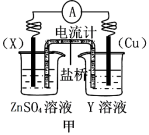
①电极X的材料是_______ ;Y溶液可以是_______ 。
②Cu电极上发生的电极反应式是_______ 。
③电池放电时,电子从_______ 电极经电流计流向_______ 电极。(填电极材料)
④电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向ZnSO4溶液一端扩散的离子是____ (填离子符号)。
(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防腐。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:_______ 。
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案:
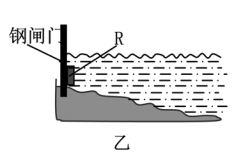
其中连接在铁闸门上的固体材料R可以采用_______ (填写字母序号)。
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则石墨应连接直流电源的_______ 极。
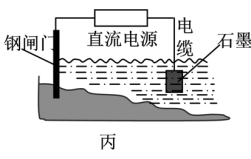
(3)电解原理在工业上有着广泛的用途,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
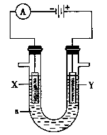
①若X、Y都是惰性电极,a是饱和NaCl溶液,则:X极上的电极反应式为_______ ;Y电极上的电极反应式为_______ 。
②如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:X电极的材料是_______ (填粗铜或纯铜),Y电极上主要的电极反应式_______ 。

①电极X的材料是
②Cu电极上发生的电极反应式是
③电池放电时,电子从
④电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向ZnSO4溶液一端扩散的离子是
(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防腐。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案:

其中连接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则石墨应连接直流电源的

(3)电解原理在工业上有着广泛的用途,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。

①若X、Y都是惰性电极,a是饱和NaCl溶液,则:X极上的电极反应式为
②如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:X电极的材料是
更新时间:2021-03-21 18:57:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】《化学与生活》化学与社会经济建设、生态文明建设、人类健康保障等密切相关。材料是经济和生态文明建设的重要物质基础。
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是____________ 。
②橡胶是制造轮胎的重要原料,橡胶属于____________ (填字母)。
A.金属材料 B.无机非金属材料 C.有机高分子材料
③钢铁制品在潮湿的空气中能发生____________ 腐蚀。发生该腐蚀时的负极反应式为____________
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是
②橡胶是制造轮胎的重要原料,橡胶属于
A.金属材料 B.无机非金属材料 C.有机高分子材料
③钢铁制品在潮湿的空气中能发生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。

(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为_________ 。
(2)利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于________ 处。
②若X为锌,开关K置于M处,该电化学防护法称为_______ 。
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量________ 3.2 g(填“<”“>”或“=”)。
(4)图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是______________ ,若将开关K置于N处,发生的总反应是___________ 。

(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为
(2)利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于
②若X为锌,开关K置于M处,该电化学防护法称为
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量
(4)图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】生活中处处有化学。请回答下列问题:
(1)维生素C能增强对疾病的抵抗力在西红柿、薯片和牛肉干三种食物中,富含维生素C的是___ 。
(2)合理饮食和正确使用药物是促进身心健康的关键
①某橙汁的食品添加剂包括柠檬酸、柠檬酸钠、维生素C和日落黄,其中属于着色剂的是___ 。
②现有复方氢氧化铝片和阿司匹林两种药物,感冒时应该服用___ 。
(3)金属材料应用十分广泛,但容易被腐蚀,需要加以保护。请列举一种防止钢铁腐蚀的方法:___ 。
(4)室内空气污染危害身体健康。请列举一条减少室内空气污染的措施:___ 。
(1)维生素C能增强对疾病的抵抗力在西红柿、薯片和牛肉干三种食物中,富含维生素C的是
(2)合理饮食和正确使用药物是促进身心健康的关键
①某橙汁的食品添加剂包括柠檬酸、柠檬酸钠、维生素C和日落黄,其中属于着色剂的是
②现有复方氢氧化铝片和阿司匹林两种药物,感冒时应该服用
(3)金属材料应用十分广泛,但容易被腐蚀,需要加以保护。请列举一种防止钢铁腐蚀的方法:
(4)室内空气污染危害身体健康。请列举一条减少室内空气污染的措施:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有如下原电池装置,插入电解质溶液前 和
和 电极的质量相等。
电极的质量相等。
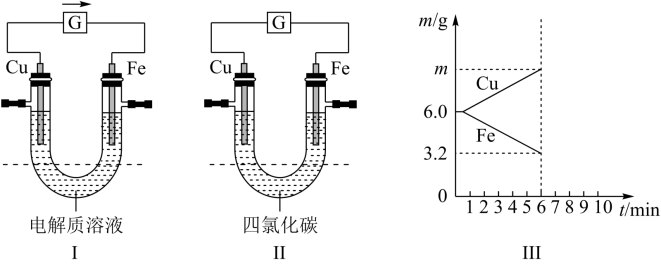
请回答下列问题:
(1)当图Ⅰ中的电解质溶液为稀硫酸时,铁片作_______ 极,铜片上的现象是_______ ;图中箭头的方向表示_______ (填“电子”或“电流”)的流向。
(2)若将图Ⅰ中的 形管虚线以下的电解质溶液换为四氯化碳(不导电),如图Ⅱ所示,则该装置
形管虚线以下的电解质溶液换为四氯化碳(不导电),如图Ⅱ所示,则该装置_______ (填“能”或“不能”)形成原电池,原因是_______ 。
(3)①当电解质溶液为某溶液时,两电极的质量变化曲线如图Ⅲ所示,则该电解质溶液可以是下列中的_______ (填字母)。
A.稀硫酸 B. 溶液 C.稀盐酸 D.
溶液 C.稀盐酸 D. 溶液
溶液
② 电极的电极反应式为
电极的电极反应式为_______ ;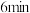 时
时 电极的质量为
电极的质量为_______  。
。
 和
和 电极的质量相等。
电极的质量相等。
请回答下列问题:
(1)当图Ⅰ中的电解质溶液为稀硫酸时,铁片作
(2)若将图Ⅰ中的
 形管虚线以下的电解质溶液换为四氯化碳(不导电),如图Ⅱ所示,则该装置
形管虚线以下的电解质溶液换为四氯化碳(不导电),如图Ⅱ所示,则该装置(3)①当电解质溶液为某溶液时,两电极的质量变化曲线如图Ⅲ所示,则该电解质溶液可以是下列中的
A.稀硫酸 B.
 溶液 C.稀盐酸 D.
溶液 C.稀盐酸 D. 溶液
溶液②
 电极的电极反应式为
电极的电极反应式为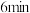 时
时 电极的质量为
电极的质量为 。
。
您最近一年使用:0次
【推荐2】回答下列问题:
(1)高铁电池是一种能量密度大的新型二次电源,被广泛应用于电动公交车。我国在高铁电池研究方面居于世界领先水平。如图是某高铁电池与某常用的高能碱性电池的放电曲线对比示意图。请回答:
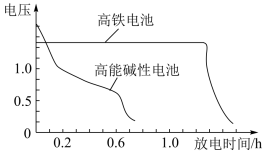
①高铁电池的优点是:_____ 。
②某高铁电池可发生如下反应:2K2FeO4+3Zn+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:
3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:_____ 。
(2)我国自行设计并使用的蛟龙号载人深海潜水器使用了性能优越的Al-Ag2O电池。其原理如图所示。该电池反应的化学方程式为:_____ 。
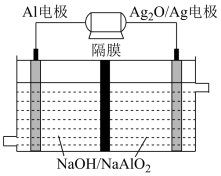
(3)铅蓄电池是常用的化学电源,电极材料分别是Pb和PbO2,电解液为硫酸。根据上述情况判断:
①该蓄电池充电时,Pb极应连接电源的_____ (填“正极”或“负极”),正极附近溶液的pH_____ (填“增大”、“减小”或“不变”)。
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050molCl2,这时电池内消耗的H2SO4的物质的量至少是_____ 。
(1)高铁电池是一种能量密度大的新型二次电源,被广泛应用于电动公交车。我国在高铁电池研究方面居于世界领先水平。如图是某高铁电池与某常用的高能碱性电池的放电曲线对比示意图。请回答:

①高铁电池的优点是:
②某高铁电池可发生如下反应:2K2FeO4+3Zn+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:
3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:(2)我国自行设计并使用的蛟龙号载人深海潜水器使用了性能优越的Al-Ag2O电池。其原理如图所示。该电池反应的化学方程式为:

(3)铅蓄电池是常用的化学电源,电极材料分别是Pb和PbO2,电解液为硫酸。根据上述情况判断:
①该蓄电池充电时,Pb极应连接电源的
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050molCl2,这时电池内消耗的H2SO4的物质的量至少是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)_____ 设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过_____ mol电子。

(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为_____ ,这是由于NH4Cl溶液显_____ (填“酸性”、“碱性”或“中性”)。用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量的氯水,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高价态。”如果+3价铁被氧化为FeO ,试写出反应的离子方程式
,试写出反应的离子方程式_____ 。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)

(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为
 ,试写出反应的离子方程式
,试写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某科研小组设计利用甲醇(CH3OH)燃料电池(酸性溶液作离子导体),模拟工业电镀、精炼和海水淡化的装置如图。
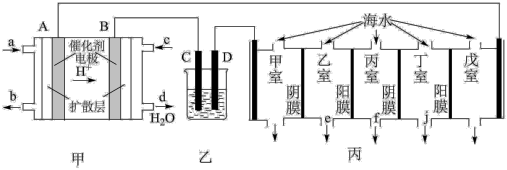
(1)甲装置中c口通入的气体是___________ ,A电极的电极反应式为___________ 。
(2)乙装置用来模拟精炼和电镀。
①若用于粗铜的精炼,装置中电极C是___________ (填“粗铜”或“纯铜”),工作一段时间后,电解质CuSO4溶液的浓度将___________ (填“增大”“减小”或“不变”)。
②若用于电镀金属银,则电镀液宜使用___________ 溶液,镀件是___________ (填“C”或“D”)。
(3)电渗析法是海水淡化的常用方法,某地海水中主要离子的含量如表,现利用“电渗析法”进行淡化,技术原理如图丙所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。
①淡化过程中在___________ 室中易形成水垢[主要成分CaCO3和Mg(OH)2],该室中除发生电极反应外,还发生反应的离子方程式为___________ 。
②产生淡水的出水口为___________ (选填“e”、“f”、“j”)。
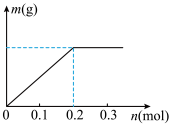
(4)若乙装置中C,D都是惰性电极,溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是___________ 。

(1)甲装置中c口通入的气体是
(2)乙装置用来模拟精炼和电镀。
①若用于粗铜的精炼,装置中电极C是
②若用于电镀金属银,则电镀液宜使用
(3)电渗析法是海水淡化的常用方法,某地海水中主要离子的含量如表,现利用“电渗析法”进行淡化,技术原理如图丙所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。
| 离子 | Na+ | K+ | Ca2+ | Mg2+ | Cl- |  |  |
| 含量/mg•L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |
②产生淡水的出水口为
(4)若乙装置中C,D都是惰性电极,溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
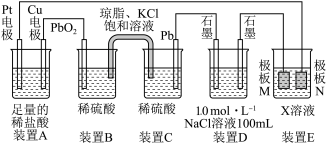
【推荐2】电化学及其产品与能源、材料、环境和健康等领域紧密联系,被广泛地应用于生产生活的许多方面。观察下列装置,回答下列问题:___________ ;盐桥中的Cl-移向装置___________ (填“B”或“C”);当电路中通过的电子为0.2mol时,Pb电极质量增重___________ g。
(2)若装置E的目的是在Cu材料上镀银,则X溶液为___________ ,极板N的材料为___________ 。
(3)当装置A中Cu电极质量改变0.64g时,装置D中发生反应的总方程式为________ ;要使电解质溶液恢复至原来状态,可向装置D剩余溶液中加入下列物质中的________ (填序号)。
A.NaCl固体 B.NaOH固体 C.HCl气体 D.H2O
(2)若装置E的目的是在Cu材料上镀银,则X溶液为
(3)当装置A中Cu电极质量改变0.64g时,装置D中发生反应的总方程式为
A.NaCl固体 B.NaOH固体 C.HCl气体 D.H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】双氧水(过氧化氢的水溶液)在工业生产和日常生活中应用广泛。
(1)双氧水常用于伤口消毒,这一过程利用了过氧化氢的_________ (填过氧化氢的化学性质)。
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。已知0.4 mol液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,并放出256.652kJ的热量。该反应的热化学方程式为__________ 。
(3)双氧水能将碱性废水中的CN-转化成碳酸盐和一种对环境无污染的气体,CN-的电子式为________ ,写出该反应的离子方程式________ 。
(4)下图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式_______ 。

(5)下图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。

①Ir-Ru惰性电极吸附O2生成H2O2,其电极反应式是_______ 。
②处理废氨水中溶质(以NH3计)的质量是34g,理论上电路中转移电子数为__________ mol。
(1)双氧水常用于伤口消毒,这一过程利用了过氧化氢的
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。已知0.4 mol液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,并放出256.652kJ的热量。该反应的热化学方程式为
(3)双氧水能将碱性废水中的CN-转化成碳酸盐和一种对环境无污染的气体,CN-的电子式为
(4)下图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式

(5)下图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。

①Ir-Ru惰性电极吸附O2生成H2O2,其电极反应式是
②处理废氨水中溶质(以NH3计)的质量是34g,理论上电路中转移电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图X是直流电源。Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒。接通电路后,发现d附近显红色。

(1)①电源上b为___ 极
②Z槽中e为___ 极。
③连接Y、Z槽线路中,电子流动的方向是d___ e(用“→”或“←”填空)。
(2)①写出Y槽中总反应的化学方程式:____ 。
②写出Z槽中e极上反应的电极反应式:___ 。

(1)①电源上b为
②Z槽中e为
③连接Y、Z槽线路中,电子流动的方向是d
(2)①写出Y槽中总反应的化学方程式:
②写出Z槽中e极上反应的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】I.用如图所示装置做电解实验,a、b、c、d均为铂电极,A槽与B槽选择的溶液足量但不同,可供选择的电解质溶液有:①500mL2mol·L-1CuSO4溶液②500mL2mol·L-1NaCl溶液③500mL2mol·L-1Na2SO4溶液④500mL2mol·L-1AgNO3溶液⑤500mL2mol·L-1CuCl2溶液。

(1)若A槽选择500mL2mol·L-1CuCl2溶液,B槽选择500mL2mol·L-1CuSO4溶液,闭合开关K2,则b极为_______ (填阴极”或“阳极”),与a极现象相同的电极为_______ (填“c极”或“d极”),d极上的电极反应式为_______ 。
(2)若电解池工作时,a、b、c、d电极均有气体产生,且只有a极产生的是黄绿色气体,则A槽选择的溶液为_______ (填标号,下同),B槽选择的溶液为_______ ,闭合的开关是_______ ,相同时间内,a、c电极上产生气体的体积(相同状况)之比为_______ 。
(3)若A槽选择500mL2mol·L-1AgNO3溶液,B槽选择500mL2mol·L-1CuSO4溶液,闭合开关K1,则析出固体的电极是_______
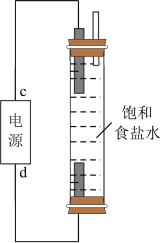
II.新冠疫情期间,某同学为解决环境卫生消毒问题,设计了一个电解装置,用于制备“84”消毒液的有效成分。
(4)如图所示,则c为电源的_______ 极;该发生器中发生反应的离子方程式为_______ 。

(1)若A槽选择500mL2mol·L-1CuCl2溶液,B槽选择500mL2mol·L-1CuSO4溶液,闭合开关K2,则b极为
(2)若电解池工作时,a、b、c、d电极均有气体产生,且只有a极产生的是黄绿色气体,则A槽选择的溶液为
(3)若A槽选择500mL2mol·L-1AgNO3溶液,B槽选择500mL2mol·L-1CuSO4溶液,闭合开关K1,则析出固体的电极是
II.新冠疫情期间,某同学为解决环境卫生消毒问题,设计了一个电解装置,用于制备“84”消毒液的有效成分。
(4)如图所示,则c为电源的

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
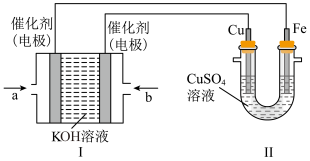
【推荐3】甲烷作为一种新能源在化学领域应用广泛,如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
请回答下列问题:
(1)b处应通入___________ (填“CH4”或“O2”),a处电极上发生的电极反应是___________ 。
(2)电镀结束后,装置Ⅰ中溶液的pH___________ (填“增大”“减小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度___________ 。
(3)电镀结束后,装置Ⅰ溶液中的阴离子除了OH-外,还含有___________ (忽略水解)。
(4)在此过程中若完全反应,装置Ⅱ中阴极质量变化25.6 g,则装置Ⅰ中理论上消耗甲烷___________ L(标准状况)。

请回答下列问题:
(1)b处应通入
(2)电镀结束后,装置Ⅰ中溶液的pH
(3)电镀结束后,装置Ⅰ溶液中的阴离子除了OH-外,还含有
(4)在此过程中若完全反应,装置Ⅱ中阴极质量变化25.6 g,则装置Ⅰ中理论上消耗甲烷
您最近一年使用:0次



