根据热化学方程式(在101kPa时):S(s)+O2(g)=SO2(g) ΔH=-297.23kJ·mol-1,分析下列说法中不正确的是
| A.S的燃烧热为297.23kJ·mol-1 |
| B.1mol S(g)和足量的O2(g)完全反应生成SO2(g),放出的热量大于297.23kJ |
| C.1mol S(g)和足量的O2(g)完全反应生成SO2(g),放出的热量小于297.23kJ |
| D.形成1molSO2(g)的化学键释放的总能量大于断裂1molS(s)和1molO2(g)的化学键吸收的总能量 |
9-10高二下·安徽·期中 查看更多[8]
吉林省油田第十一中学2019-2020学年高二上学期第一次月考化学试题浙江省温州市求知中学2018-2019学年高二上学期期中考试(选考)化学试题2015-2016学年山东省烟台市莱山一中高二化学上学期段考试卷2015-2016学年辽宁省沈阳铁路实验中学高一下期中化学试卷(已下线)2010年安徽师大附中高二第二学期期中考查2015-2016学年河北省秦皇岛市卢龙县高二上学期期末考试化学试卷(已下线)2014-2015学年吉林延边二中高二9月阶段考试化学试卷(已下线)2011-2012学年河南省商丘市回民中学高二上期月考化学试卷
更新时间:2016-12-09 03:31:24
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】关于A、B、C三种物质之间的转化及能量变化如下图所示,下列说法中不正确的是


| A.物质A具有的能量高于B和C具有的能量总和 |
| B.对于A=B+C的过程是一个吸热的过程 |
| C.对于A=B+C和B+C=A两个反应吸收和放出的热量相同 |
| D.反应A=B+C是吸热过程,B+C=A必然是放热过程 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】 是电子工业使用的一种新型蚀刻气体。实验分别测得断裂
是电子工业使用的一种新型蚀刻气体。实验分别测得断裂 所需的能量如图:
所需的能量如图:

下列说法错误的是
 是电子工业使用的一种新型蚀刻气体。实验分别测得断裂
是电子工业使用的一种新型蚀刻气体。实验分别测得断裂 所需的能量如图:
所需的能量如图:
下列说法错误的是
A.相同条件下, 化学性质比 化学性质比 稳定 稳定 |
B. 的能量一定比 的能量一定比 和 和 总和高 总和高 |
C. |
| D.断裂化学键需要吸收能量,则形成化学键一定放出能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】先进的甲醇蒸气重整—变压吸附技术可得到高浓度 混合气、
混合气、 ,化学反应原理是
,化学反应原理是 ,其能量变化如图所示。下列说法正确的是
,其能量变化如图所示。下列说法正确的是
 混合气、
混合气、 ,化学反应原理是
,化学反应原理是 ,其能量变化如图所示。下列说法正确的是
,其能量变化如图所示。下列说法正确的是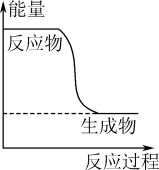
A. 转变成 转变成 的过程是一个吸收能量的过程 的过程是一个吸收能量的过程 |
| B.反应物的总能量大于生成物的总能量 |
C.形成 键吸收能量 键吸收能量 |
D.断开 键放出能量 键放出能量 |
您最近一年使用:0次
【推荐2】2020年10月,我国建成全球首套千吨级液态太阳燃料合成示范装置,其原理如图所示。下列说法错误的是
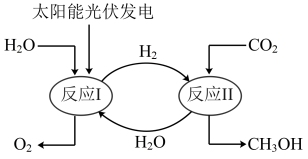
| A.高纯硅可用于制造太阳能光伏电池 |
| B.反应Ⅰ中电能转化为化学能 |
C.反应Ⅰ与 的燃烧反应互为可逆反应 的燃烧反应互为可逆反应 |
D.反应Ⅱ能够促进 资源化利用,有助于实现“碳中和” 资源化利用,有助于实现“碳中和” |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】亚硝酰氯(NOCl)在有机合成中有重要应用。2NO(g)+Cl2(g)→2NOCl(g)的反应历程如图。下列说法错误 的是


| A.相对于曲线Ⅱ,曲线Ⅰ表示加入催化剂 |
| B.催化剂能提高反应物的相对能量 |
| C.反应物总能量高于生成物的总能量 |
| D.2NO(g)+Cl2(g)→2NOCl(g)+77.1kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知几种化学键的键能和热化学方程式如下:
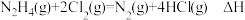 ,下列推断正确的是
,下列推断正确的是
化学键 | H-N | N-N | Cl-Cl |
| H-Cl |
键能 | 391 | 193 | 243 | 945 | 431 |
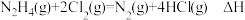 ,下列推断正确的是
,下列推断正确的是A.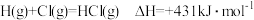 |
B.断裂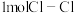 键吸收能量比断裂 键吸收能量比断裂 键多 键多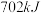 |
C.上述反应中,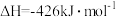 |
| D.上述反应中,断裂了极性键和非极性键,只形成了极性键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】根据如图的能量图,下列说法正确的是


| A.A2(g)+B2(g)=2AB(g)是一个放热反应 |
| B.2molAB的总能量大于1molA2和lmolB2的能量之和 |
| C.1molA2(g)和1molB2(g)的能量之和为a kJ |
| D.2AB(g)=A2(l)+B2(l) △H<(b-a)kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列有关能量的判断和表示方法正确的是
A.由C(s,石墨)=C(s,金刚石)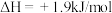 ,可知:金刚石比石墨更稳定 ,可知:金刚石比石墨更稳定 |
| B.等质量的硫蒸气和固体流分别完全燃烧,后者放出的热量更多 |
C.已知: ,但含 ,但含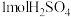 的溶液与含 的溶液与含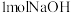 的溶液混合,放出的热量不一定等于 的溶液混合,放出的热量不一定等于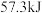 |
D. 完全燃烧生成液态水放出 完全燃烧生成液态水放出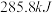 热量,则氢气燃烧的热化学方程式为: 热量,则氢气燃烧的热化学方程式为: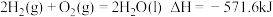 |
您最近一年使用:0次


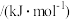
 键消耗能量
键消耗能量 ,断开
,断开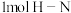 键消耗能量
键消耗能量 ,
,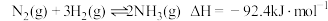 ,则断开
,则断开
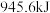 能量
能量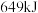 能量
能量 反应过程中的能量变化情况如图所示,曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
反应过程中的能量变化情况如图所示,曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
 变小
变小

