是电子工业使用的一种新型蚀刻气体。实验分别测得断裂
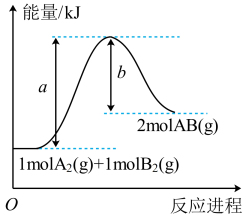
是电子工业使用的一种新型蚀刻气体。实验分别测得断裂 所需的能量如图:
所需的能量如图:
下列说法错误的是
A.相同条件下, 化学性质比 化学性质比 稳定 稳定 |
B. 的能量一定比 的能量一定比 和 和 总和高 总和高 |
C. |
| D.断裂化学键需要吸收能量,则形成化学键一定放出能量 |
更新时间:2024-01-06 11:09:10
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g) ΔΗ= -283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔΗ= -241.8kJ/mol
据此判断下列说法正确的是
①CO(g)+1/2O2(g)=CO2(g) ΔΗ= -283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔΗ= -241.8kJ/mol
据此判断下列说法正确的是
| A.H2(g)+1/2O2(g)=H2O(l) ΔΗ>-241.8kJ/mol |
| B.H2(g)的燃烧热ΔΗ =-241.8 kJ/mol |
| C.H2(g)转变成H2O(g)的化学反应一定放出能量 |
| D.CO(g)+ H2O(g)= CO2(g)+ H2(g)的ΔΗ =-41.2kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】1mol H2完全燃烧生成液态水的焓变为ΔH1,0.5mol H2完全燃烧生成液态水的焓变为ΔH2,则ΔH1、ΔH2的关系大小为( )
| A.ΔH1<ΔH2 | B.ΔH1=ΔH2 | C.ΔH1>ΔH2 | D.无法确定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】下列说法或表示正确的是
A.500℃、30 MPa 下,将 0.5 mol N2和 1.5 mol H2置于密闭容器中充分反应生成 NH3(g), 放热 19.3 kJ,其热化学方程式为:N2(g) + 3H2(g)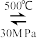 2NH3(g) △ H =− 38.6 kJ · mol−1 2NH3(g) △ H =− 38.6 kJ · mol−1 |
| B.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量少 |
| C.由 C(石墨) = C(金刚石) ΔH =+ 1.9kJ·mol−1,可知,金刚石比石墨稳定 |
| D.1 mol 甲烷燃烧生成气态水和二氧化碳气体所放出的热量就是甲烷的燃烧热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知H—H键、Cl—Cl键和H—Cl键的键能分别为436 kJ·mol-1、243 kJ·mol-1和431 kJ·mol-1,由此可知,由1 mol Cl2和1 mol H2生成2 mol HCl的反应过程中 ( )
| A.放热183 kJ | B.放热91.5 kJ |
| C.吸热183 kJ | D.吸热91.5 kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】利用固体表面催化工艺进行NO分解的过程如图所示( N
N O)。下列说法不正确的是( )
O)。下列说法不正确的是( )

 N
N O)。下列说法不正确的是( )
O)。下列说法不正确的是( )
| A.NO属于极性分子 |
| B.含有非极性共价键 |
| C.过程②释放能量,过程③吸收能量 |
| D.标准状况下,NO分解生成5.6LN2转移电子数为6.02×1023 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】 和
和 在一定条件下能发生反应:
在一定条件下能发生反应: ,生成2molHCl(g)反应放出热量183kJ,下图为
,生成2molHCl(g)反应放出热量183kJ,下图为 与
与 在一定条件下反应生成的HCl(g)微观示意图
在一定条件下反应生成的HCl(g)微观示意图

注:示意图中的能量表示断裂或形成1mol共价键吸收或放出的热量,a大于零。
下列说法正确的是
 和
和 在一定条件下能发生反应:
在一定条件下能发生反应: ,生成2molHCl(g)反应放出热量183kJ,下图为
,生成2molHCl(g)反应放出热量183kJ,下图为 与
与 在一定条件下反应生成的HCl(g)微观示意图
在一定条件下反应生成的HCl(g)微观示意图
注:示意图中的能量表示断裂或形成1mol共价键吸收或放出的热量,a大于零。
下列说法正确的是
| A.通过计算可知示意图中a=431 |
| B.反应物的总能量低于生成物的总能量 |
| C.该反应历程中既有极性键的断裂,也有非极性键的形成 |
| D.断开1molH-H键和1molCl-Cl键所需的总能量大于形成2molH-Cl键所需的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】罗马大学Fulvio Cacace等人获得了极具理论研究意义的N4分子,N4分子结构如右图所示(与白磷P4相似)。已知断裂1 mol N—N键吸收167 kJ热量,生成 1 mol N≡N键放出 942 kJ 热量。由此判断下列说法正确的是( )
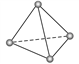

| A.N4属于一种新型的化合物 | B.N4与N2互为同分异构体 |
| C.N4沸点比P4(白磷)高 | D.1 mol N4气体转变为N2将放出882 kJ热量 |
您最近一年使用:0次

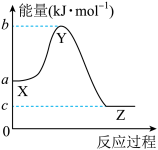
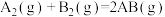
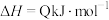 的能量变化如图所示,判断下列叙述中正确的是
的能量变化如图所示,判断下列叙述中正确的是