从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。以下是氮元素形成物质的价类二维图的及氮的循环的部分信息。
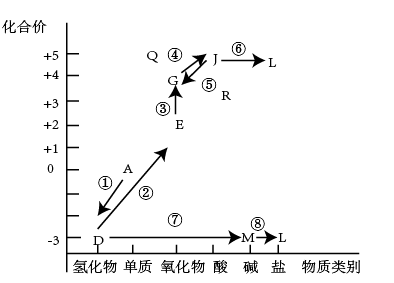
(1)①是一种人工固氮的重要途径,按反应的化学方程式是_______ 。
(2)②、④的化学方程式分别是_______ 。
(3)铜与J的稀溶液反应的离子方程式是_______ 。
(4)R可与NaOH溶液反应:HNO2+NaOH=NaNO2+H2O,该反应体现了R的_______ 性。
(5)Q的化学式是_______ ,Q属于酸性氧化物,写出Q与水反应的化学方程式_______ 。
(6)L在水体中过多蓄积会导致水体富营养化。将水体调节为酸性后加入适量NaClO,可将L中阳离子转化为无污染气体以去除,写出L与NaClO反应的离子方程式:_______ 。

(1)①是一种人工固氮的重要途径,按反应的化学方程式是
(2)②、④的化学方程式分别是
(3)铜与J的稀溶液反应的离子方程式是
(4)R可与NaOH溶液反应:HNO2+NaOH=NaNO2+H2O,该反应体现了R的
(5)Q的化学式是
(6)L在水体中过多蓄积会导致水体富营养化。将水体调节为酸性后加入适量NaClO,可将L中阳离子转化为无污染气体以去除,写出L与NaClO反应的离子方程式:
更新时间:2021-04-03 10:52:03
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】一定条件下,含氮元素的物质可发生如图所示的循环转化。
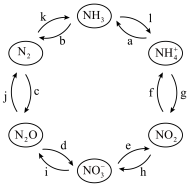
回答下列问题:
(1)氮原子结构示意图为________ 。
(2)图中属于“氮的固定”的是________ (填字母)。
(3)转化过程中发生非氧化还原反应的是________ (填字母)。
(4)若“反应i”是在酸性条件下由 与Zn的作用实现,则该反应的离子方程式为
与Zn的作用实现,则该反应的离子方程式为__________ 。
(5)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为________ (填字母)。
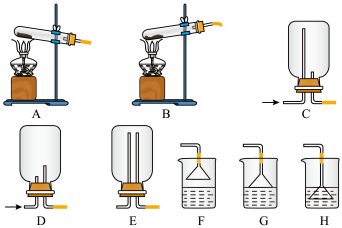
(6)在标准状况下,有甲乙两个容积相同的圆底烧瓶,在甲中充满NH3,乙中充满NO2和O2的混合气体,把它们分别倒扣在盛水的水槽中,最终两个烧瓶中均充满液体,则甲乙两圆底烧瓶中所得溶液的物质的量浓度之比为________ 。

回答下列问题:
(1)氮原子结构示意图为
(2)图中属于“氮的固定”的是
(3)转化过程中发生非氧化还原反应的是
(4)若“反应i”是在酸性条件下由
 与Zn的作用实现,则该反应的离子方程式为
与Zn的作用实现,则该反应的离子方程式为(5)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为

(6)在标准状况下,有甲乙两个容积相同的圆底烧瓶,在甲中充满NH3,乙中充满NO2和O2的混合气体,把它们分别倒扣在盛水的水槽中,最终两个烧瓶中均充满液体,则甲乙两圆底烧瓶中所得溶液的物质的量浓度之比为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】生物地球氮化学循环模式图的一部分如图,请根据所学知识回答问题。
已知:硝化作用是在有氧的条件下,氨或铵根经亚硝酸细菌和硝酸细菌的作用转化为硝酸的过程。铵根浓度或pH过大,都会使硝化作用减弱。

(1)属于氮的固定的是_______ (填标号)。
(2)利用如图装置可以制备、检验和收集NO。
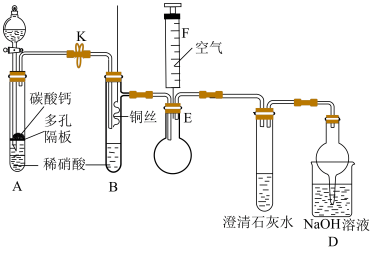
①实验前先打开开关K通入 一段时间,其目的是
一段时间,其目的是_______ 。采用抽拉铜丝与稀硝酸反应的优点为_______ 。
②检验生成的气体为NO的操作是_______ 。
③装置D的作用是_______ 。
(3)NO与 反应生成
反应生成 的离子方程式为
的离子方程式为_______ ,该反应中氧化产物与还原产物的物质的量之比为_______ 。
(4)写出铵根经硝化作用直接转化为硝酸根的离子方程式:_______ ,铵根浓度或pH过大,都会使硝化作用减弱的可能原因为_______ 。
已知:硝化作用是在有氧的条件下,氨或铵根经亚硝酸细菌和硝酸细菌的作用转化为硝酸的过程。铵根浓度或pH过大,都会使硝化作用减弱。

(1)属于氮的固定的是
(2)利用如图装置可以制备、检验和收集NO。

①实验前先打开开关K通入
 一段时间,其目的是
一段时间,其目的是②检验生成的气体为NO的操作是
③装置D的作用是
(3)NO与
 反应生成
反应生成 的离子方程式为
的离子方程式为(4)写出铵根经硝化作用直接转化为硝酸根的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】亚硝酸钠(NaNO2)是一种常 见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并进行纯度测定(夹持装置及A中加热装置已略去)。

已知:①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4溶液氧化成NO , MnO
, MnO 被还原为Mn2+。
被还原为Mn2+。
③在酸性条件下NaNO2能把I-氧化为I2; S2O 能把I2还原为I-。
能把I2还原为I-。
(1)装置A中盛装浓HNO3的仪器名称为_______ ,三领烧瓶中发生反应的化学方程式为_______ 。
(2)二氧化氮在装置B中与水反应转化为一氧化氮, 其中铜发生反应的离子方程式为_______ 。
(3)为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是_______(填序号)。
(4)E装置的作用是_______ ,若撤去装置E中试管,则导管口可能看到的现象为_______ 。
(5)利用滴定的方法进行纯度测定。
可供选择的试剂有: A.稀硫酸 B.稀硝酸 C.c1mol·L-1KI溶液 D.淀粉溶液 E. c2mol·L -1Na2S2O3溶液 F. c3 mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,须选用的试剂是_______ (填序号),滴定终点的现象为_______ 。
②利用NaNO2的氧化性来测定其纯度,须选用的试剂有_______ (填序号)。

已知:①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4溶液氧化成NO
 , MnO
, MnO 被还原为Mn2+。
被还原为Mn2+。③在酸性条件下NaNO2能把I-氧化为I2; S2O
 能把I2还原为I-。
能把I2还原为I-。(1)装置A中盛装浓HNO3的仪器名称为
(2)二氧化氮在装置B中与水反应转化为一氧化氮, 其中铜发生反应的离子方程式为
(3)为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是_______(填序号)。
| A.P2O5 | B.碱石灰 | C.无水CaCl2 | D.氧化钙 |
(5)利用滴定的方法进行纯度测定。
可供选择的试剂有: A.稀硫酸 B.稀硝酸 C.c1mol·L-1KI溶液 D.淀粉溶液 E. c2mol·L -1Na2S2O3溶液 F. c3 mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,须选用的试剂是
②利用NaNO2的氧化性来测定其纯度,须选用的试剂有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】在下图所示的物质转化关系中。A是常见气态氢化物,B是能使带火星的木条复燃的无色无味气体,E的相对分子质量比D大17,G是一种紫红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)
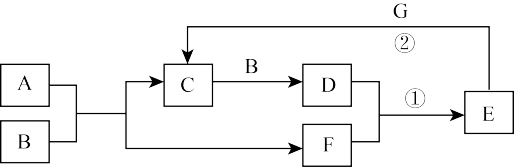
请回答下列问题:
(1)B的化学式为_________________ 。
(2)A的电子式为_________________ 。
(3)反应①的化学方程式为________________________________ 。
(4)反应②的离子方程式为_________________________________ 。

请回答下列问题:
(1)B的化学式为
(2)A的电子式为
(3)反应①的化学方程式为
(4)反应②的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】为研究硝酸的性质,某同学设计并完成如下实验:室温下,将铁片分别置于适量的稀HNO3和浓HNO3中(如图所示)。
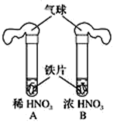
(1)气球的作用是___________ 。
(2)A中溶液最终变为浅绿色,发生反应的离子方程式是___________ 。
(3)B中无明显变化,该同学进一步探究如下:
假设①常温下铁与浓硝酸不反应。
假设②___________ 。
进行实验:将B中的铁片取出并洗净后,放入CuSO4溶液中,无明显变化,则说明假设①___________ (填“成立”或“不成立”)。
(4)若将B试管加热,可观察到___________ 色气体产生。若将此气体与O2混合通入Na2CO3溶液中吸收,写出其反应方程式___________ 。

(1)气球的作用是
(2)A中溶液最终变为浅绿色,发生反应的离子方程式是
(3)B中无明显变化,该同学进一步探究如下:
假设①常温下铁与浓硝酸不反应。
假设②
进行实验:将B中的铁片取出并洗净后,放入CuSO4溶液中,无明显变化,则说明假设①
(4)若将B试管加热,可观察到
您最近一年使用:0次



