锌与硫所形成化合物晶体的晶胞如图所示。下列判断正确的是
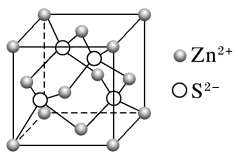

| A.该晶体属于分子晶体 |
| B.该晶胞中Zn2+和S2-数目不相等 |
| C.阳离子的配位数为6 |
| D.氧化锌的熔点高于硫化锌 |
20-21高二下·甘肃平凉·阶段练习 查看更多[8]
河南省郑州市十校2022-2023学年高二下学期期中联考化学试题(已下线)第五章 物质结构与性质元素周期律 第31练 晶体结构与性质山东省聊城市颐中外国语学校2021-2022学年高二下学期第一次月考化学试题山东省聊城市颐中外国语学校2021-2022学年高二下学期期中考试化学试题四川省遂宁市射洪中学2021—2022学年高二上学期期中考试化学试题江苏省常州市礼嘉中学2020-2021学年高二下学期第二次阶段质量调研化学试题(已下线)3.3 金属晶体与离子晶体(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)甘肃省静宁县第一中学2020-2021学年高二下学期第一次月考化学(普)试题
更新时间:2021-04-09 09:03:11
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关物质结构与性质的因果关系论述中,错误的是
A.因为键能 ,所以 ,所以 的热稳定性强于 的热稳定性强于 |
B.因为 的孤电子对数多于 的孤电子对数多于 ,所以 ,所以 的键角小于 的键角小于 |
C.因为 的非羟基氧数目多于 的非羟基氧数目多于 ,所以 ,所以 酸性强于 酸性强于 |
D.因为 半径大于 半径大于 ,所以 ,所以 中阳离子的配位数比 中阳离子的配位数比 中的大 中的大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】有关晶格能的叙述正确的是
| A.晶格能是气态离子形成1摩离子晶体释放的能量 |
| B.晶格能通常取正值,但是有时也取负值 |
| C.晶格能越大,形成的离子晶体越不稳定 |
| D.晶格能越大,物质的硬度反而越小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】模型在科学认识中具有描述、解释和预测等功能。下列有关化学模型的说法错误的是
| A.金属晶体的简单立方堆积是密置层得到的一种堆积方式 |
| B.氯化钠和氯化铯晶体中氯离子的配位数不同可用阳离子与阴离子的半径比不同解释 |
| C.由NH3和BF3易化合生成H3NBF3可预测H3NBF3中含有配位键 |
D.根据VSEPR理论可推测BF3的键角大于BF |
您最近半年使用:0次
【推荐2】元素ⅹ位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子。X与Y形成的化合物的晶胞结构如图所示,下列关于该晶体的说法正确的是
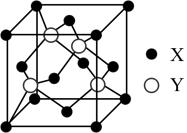

| A.1个晶胞中所含离子总数为18 |
| B.X2+的配位数为8,Y2-的配位数为4 |
| C.与每个X2+距离最近且相等的X2+共有12个 |
| D.该化合物的化学式为CaS |
您最近半年使用:0次
【推荐1】有关结构如图所示,下列说法不正确的是
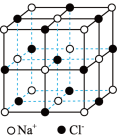  晶体 晶体 | 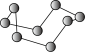  分子 分子 | 晶体硼结构单元(有12个B原子)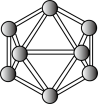 | 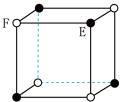 有E原子和F原子构成的气态团簇能分子模型 |
在 晶体中,距 晶体中,距 最近的 最近的 形成正八面体 形成正八面体 | 固态硫 中S原子为 中S原子为 杂化 杂化 | 晶体硼的结构单元中含有30个 键,含20个正三角形 键,含20个正三角形 | 该气态团簇分子的分子式为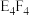 或 或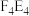 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各项叙述中,正确的是
A.基态氮原子的轨道表示式为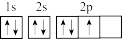 |
| B.氯化钠晶体中,每个Na+周围距离最近且相等的Na+共有6个 |
| C.氯原子有17种不同运动状态的电子 |
| D.H2O分子的VSEPR模型为V形 |
您最近半年使用:0次

 的晶体结构与
的晶体结构与 代替,
代替, 代替(如图),晶体中含有的哑铃形
代替(如图),晶体中含有的哑铃形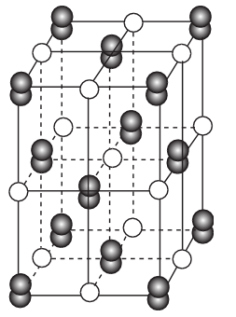
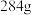
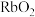 的熔点低
的熔点低 晶体中,一个
晶体中,一个 表示阿伏加德罗常数)
表示阿伏加德罗常数)

