漂白粉是一种常用杀菌、消毒剂,其有效成分为次氯酸钙。如图为制取漂白粉的工业流程简图。

(1)流程Ⅰ得到浓度为80 g/L氢氧化钠溶液,其物质的量浓度是_______ mol/L。
(2)流程 Ⅱ的反应条件(2)是_______ 。
(3)流程 Ⅲ中发生两个反应,写出其中一个的氧化还原反应的方程式:_______ 。
(4)流程 Ⅳ中操作b是_______ (写名称)。
(5)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因:_______ 。

(1)流程Ⅰ得到浓度为80 g/L氢氧化钠溶液,其物质的量浓度是
(2)流程 Ⅱ的反应条件(2)是
(3)流程 Ⅲ中发生两个反应,写出其中一个的氧化还原反应的方程式:
(4)流程 Ⅳ中操作b是
(5)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因:
更新时间:2021-04-12 18:58:50
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】汽车尾气中CO、NO2在一定条件下可发生反应: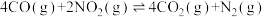 。回答下列问题。
。回答下列问题。
(1)一定温度下,在体积不变的密闭容器中发生反应: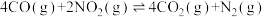 ,下列说法中可判断该反应达到平衡状态的是_______(填序号)。
,下列说法中可判断该反应达到平衡状态的是_______(填序号)。
(2)某温度下,将4 mol CO和2 mol NO2气体通入4 L的恒容密闭容器中,发生上述反应(不考虑NO2与N2O4的转化)。反应进行到5s时,测得生成CO2的物质的量为1 mol;反应进行到60s时达到平衡,此时容器内NO2与N2的物质的量相等。
①0~5s内,用CO2表示的化学反应速率v(CO2)=_______ 。
②5s时,容器中NO2的物质的量浓度为_______ 。
③体系中起始时的压强与平衡时的压强之比为_______ 。
(3)要想提高上述反应的反应速率,可采取的措施有_______ (回答两种)。
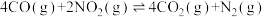 。回答下列问题。
。回答下列问题。(1)一定温度下,在体积不变的密闭容器中发生反应:
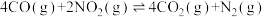 ,下列说法中可判断该反应达到平衡状态的是_______(填序号)。
,下列说法中可判断该反应达到平衡状态的是_______(填序号)。| A.当生成n mol N2时,同时消耗2n mol NO2 |
| B.容器中混合气体的压强不再变化 |
| C.混合气体的颜色不再改变 |
| D.CO和CO2的物质的量相等 |
①0~5s内,用CO2表示的化学反应速率v(CO2)=
②5s时,容器中NO2的物质的量浓度为
③体系中起始时的压强与平衡时的压强之比为
(3)要想提高上述反应的反应速率,可采取的措施有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列十种物质:①H2 ②铝 ③醋酸 ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸⑨熔融Al2(SO4)3 ⑩NaHSO4。
(1)按物质的分类方法填写表格的空白处:
属于非电解质的是__________ ;属于电解质的是__________ ;能导电的是____________ 。
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH−===H2O,该离子反应对应的化学方程式为_____________________________ 。
(3)写出③和⑦反应的离子方程式为__________________ ,34.2 g ⑨溶于水配成250 mL溶液,SO42-的物质的量浓度为_________________ 。
(4)过量的④通入⑥的溶液中反应的离子方程式为______________________ 。
(5)将⑩的溶液加入⑥的溶液中至溶液中的Ba2+离子恰好完全沉淀时反应的离子方程式为__________ 。
(1)按物质的分类方法填写表格的空白处:
属于非电解质的是
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH−===H2O,该离子反应对应的化学方程式为
(3)写出③和⑦反应的离子方程式为
(4)过量的④通入⑥的溶液中反应的离子方程式为
(5)将⑩的溶液加入⑥的溶液中至溶液中的Ba2+离子恰好完全沉淀时反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氨气是一种重要的基础化工原料,用途广泛。
(1)在微电子工业中,氨水可作刻蚀剂H2O2的清除剂,产物不污染环境。该反应的化学方程式为2NH3 + 3H2O2=_______ +6H2O
(2)工业中常用以下反应合成氨:N2+3H2 2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入N2和H2,浓度均为c(N2)=0.100mol/L,c(H2)= 0.300mol/L,进行反应时, N2的浓度随时间的变化如图①、②、③曲线所示。
2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入N2和H2,浓度均为c(N2)=0.100mol/L,c(H2)= 0.300mol/L,进行反应时, N2的浓度随时间的变化如图①、②、③曲线所示。
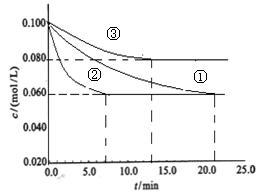
该反应平衡常数的数学表达式为____________ ;实验②平衡时H2的转化率为____________ 。
(3)据图所示,②、③两装置中各有一个条件与①不同。请指出,并说明判断的理由。
②条件:____________ 理由:_________________ ;
③条件:____________ 理由:_________________ 。
(1)在微电子工业中,氨水可作刻蚀剂H2O2的清除剂,产物不污染环境。该反应的化学方程式为2NH3 + 3H2O2=
(2)工业中常用以下反应合成氨:N2+3H2
 2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入N2和H2,浓度均为c(N2)=0.100mol/L,c(H2)= 0.300mol/L,进行反应时, N2的浓度随时间的变化如图①、②、③曲线所示。
2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入N2和H2,浓度均为c(N2)=0.100mol/L,c(H2)= 0.300mol/L,进行反应时, N2的浓度随时间的变化如图①、②、③曲线所示。
该反应平衡常数的数学表达式为
(3)据图所示,②、③两装置中各有一个条件与①不同。请指出,并说明判断的理由。
②条件:
③条件:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铜在自然界多以+1价存在于矿石中,在固态特别是高温下,+1价铜的化合物比+2价稳定。用辉铜矿(Cu2S)炼铜的方法如下:
(1)将辉铜矿在空气中高温焙烧,生成两种氧化物,反应的化学方程式是_____________ 。
(2)向焙烧得到的矿石中,再加上原矿石一半质量的未经焙烧过的矿石,混合后隔绝空气进行高温煅烧,得到金属铜和一种具有刺激性气味的气体,反应的化学方程式是____________ 。
(1)将辉铜矿在空气中高温焙烧,生成两种氧化物,反应的化学方程式是
(2)向焙烧得到的矿石中,再加上原矿石一半质量的未经焙烧过的矿石,混合后隔绝空气进行高温煅烧,得到金属铜和一种具有刺激性气味的气体,反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】(1)某混合物中含有硫酸钠和硫酸铝,经实验测得其中硫元素的质量分数为25%,则其中铝元素的质量分数为_______________ 。
(2)油炸食物中通常含有铝元素,对人体健康不利,市售不含铝的膨松剂主要成分为:NaHCO3和Ca(H2PO4)2,请配平下列化学方程式:
_____ NaHCO3 + ______ Ca(H2PO4)2—_____ CaHPO4 +_____ Na2HPO4 +_____ CO2 +_____ H2O
(3)已知:在化学反应中,有元素化合价升高的过程,就一定有元素化合价降低。工业上常用NH3来检测输送Cl2的管道是否泄漏,检测过程中会产生大量白烟(NH4Cl),还会生成一种无毒的气态单质,试写出该检测过程方程式:______________
(2)油炸食物中通常含有铝元素,对人体健康不利,市售不含铝的膨松剂主要成分为:NaHCO3和Ca(H2PO4)2,请配平下列化学方程式:
(3)已知:在化学反应中,有元素化合价升高的过程,就一定有元素化合价降低。工业上常用NH3来检测输送Cl2的管道是否泄漏,检测过程中会产生大量白烟(NH4Cl),还会生成一种无毒的气态单质,试写出该检测过程方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.NaClO是“84”消毒液的有效成分。请回答下列问题:
(1)NaClO中Cl元素的化合价是________ 。
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:_______________ 。(已知酸性: )
)
(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是____________________ 。
Ⅱ. 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。
(1)已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为______________ 。
(2)喷射石灰乳等碱性物质可以减轻少量 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是__________________ 。
(3)实验室常用烧碱溶液吸收 。若将
。若将 通入热的烧碱溶液中,可以得到NaCl、NaClO和
通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为15∶2时,混合液中
的个数比为15∶2时,混合液中 和
和 的个数比为
的个数比为_______________ 。
(1)NaClO中Cl元素的化合价是
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:
 )
)(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是
Ⅱ.
 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。(1)已知
 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为(2)喷射石灰乳等碱性物质可以减轻少量
 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是(3)实验室常用烧碱溶液吸收
 。若将
。若将 通入热的烧碱溶液中,可以得到NaCl、NaClO和
通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为15∶2时,混合液中
的个数比为15∶2时,混合液中 和
和 的个数比为
的个数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】由氢气和氯气组成的混合气体,经光照充分反应后,通入100mL1molLNaOH溶液中,溶液中某种离子的物质的量(图甲)和溶液的导电性(图乙)随着反应后的混合气体通入体积的变化而变化。
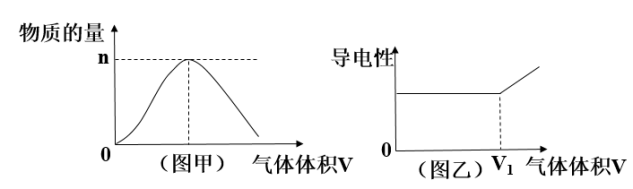
(1)图甲曲线表示溶液中___________ 离子的变化。
(2)对溶液进行导电性实验时,发现当通入的光照反应后的混合气体体积大于V1时,随着混合气体的通入,溶液导电性明显增强,引起导电性增强的主要正、负离子是___________ 。
(3)当图甲中n=0.01mol时,则光照前的混合气体中H2和Cl2的物质的量之比为___________ 。(书写必要步骤)

(1)图甲曲线表示溶液中
(2)对溶液进行导电性实验时,发现当通入的光照反应后的混合气体体积大于V1时,随着混合气体的通入,溶液导电性明显增强,引起导电性增强的主要正、负离子是
(3)当图甲中n=0.01mol时,则光照前的混合气体中H2和Cl2的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择填充并简述理由。
(1)处理钢瓶的方法正确的是_______ ,简述理由____________________________ 。
A、钢瓶推到坡下的小河里
B、把钢瓶丢到深坑里,用石灰填埋
C、把钢瓶扔到农田中
(2)钢瓶处理后,工人应立即__________ ,简述理由_________________________ 。
A、转移到坡下 B、转移到坡上
(3)若在场工人没有防毒面具,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子。最适宜采用的物质是________ 。(A、NaOH B、NaCl C、Na2O2 D、Na2CO3)
(1)处理钢瓶的方法正确的是
A、钢瓶推到坡下的小河里
B、把钢瓶丢到深坑里,用石灰填埋
C、把钢瓶扔到农田中
(2)钢瓶处理后,工人应立即
A、转移到坡下 B、转移到坡上
(3)若在场工人没有防毒面具,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子。最适宜采用的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
I.利用价类二维图像,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:
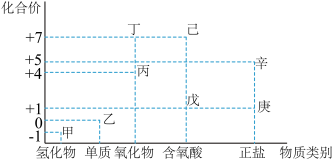
(1)丙的化学式为_______ ;戊的化学式为_______ ,具有_______ (任意写出一种戊具有的性质);
(2)根据氯元素的化合价判断,乙物质_______ 。
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)若庚是源白粉的有效成分。漂白粉也是常用消毒剂之一、漂白粉溶于水后,受空气中的 作用,产生有漂白、杀菌作用的次氯酸,其化学方程式为:
作用,产生有漂白、杀菌作用的次氯酸,其化学方程式为:_______ 。
II.某校化学课外小组为了鉴别 和
和 两种白色固体。用不同的方法做了以下实验,如图所示:
两种白色固体。用不同的方法做了以下实验,如图所示:

(4)方法I中逐滴加入 溶液
溶液_______ (填“能”或“不能”)鉴别 和
和 。
。
(5)方法II能鉴别 和
和 的现象是
的现象是_______ 。
(6)方法III、IV均能鉴别这两种物质,其中加热试管发生反应的化学方程式为____ ,与方法Ⅲ相比,方法IV的优点是____ (填字母)。
A.IV比III复杂
B.IV比III安全
C.IV比III操作简便
D.IV可以做到用一套装置同时进行两个实验,而III不行
(7)若用方法IV验证 和
和 的稳定性,则试管B中装入的固体是
的稳定性,则试管B中装入的固体是____ (填化学式)
I.利用价类二维图像,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为
(2)根据氯元素的化合价判断,乙物质
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)若庚是源白粉的有效成分。漂白粉也是常用消毒剂之一、漂白粉溶于水后,受空气中的
 作用,产生有漂白、杀菌作用的次氯酸,其化学方程式为:
作用,产生有漂白、杀菌作用的次氯酸,其化学方程式为:II.某校化学课外小组为了鉴别
 和
和 两种白色固体。用不同的方法做了以下实验,如图所示:
两种白色固体。用不同的方法做了以下实验,如图所示:
(4)方法I中逐滴加入
 溶液
溶液 和
和 。
。(5)方法II能鉴别
 和
和 的现象是
的现象是(6)方法III、IV均能鉴别这两种物质,其中加热试管发生反应的化学方程式为
A.IV比III复杂
B.IV比III安全
C.IV比III操作简便
D.IV可以做到用一套装置同时进行两个实验,而III不行
(7)若用方法IV验证
 和
和 的稳定性,则试管B中装入的固体是
的稳定性,则试管B中装入的固体是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图是一些常见含氯产品,根据情况回答下列问题。

(1)下列有关氯单质和氯水的说法正确的是________ (填序号)。
①液氯是纯净物,氯水是混合物
②氯气可使湿润的红色布条褪色,所以氯气具有漂白性
③过量的铁在少量的氯气中燃烧生成FeCl2
④新制氯水可使蓝色石蕊试纸先变红后褪色
⑤新制氯水放置数天后酸性将减弱
(2)用化学方程式表示漂白粉的漂白原理________________________ ;
(3)向FeSO4溶液中滴加氯水,溶液变为黄色,写出反应的离子方程式_____
(4)据报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分为稀盐酸)与“84”消毒液(有效成分NaClO),而发生氯气中毒事件,请从氧化还原的角度分析原因________________________ (用离子方程式表示)。
(5)一定量铁粉与氯气充分反应后,加适量水,完全溶解后无固体剩余,此时所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等,则已反应的Fe3+和未反应的Fe3+的质量之比是________________________

(1)下列有关氯单质和氯水的说法正确的是
①液氯是纯净物,氯水是混合物
②氯气可使湿润的红色布条褪色,所以氯气具有漂白性
③过量的铁在少量的氯气中燃烧生成FeCl2
④新制氯水可使蓝色石蕊试纸先变红后褪色
⑤新制氯水放置数天后酸性将减弱
(2)用化学方程式表示漂白粉的漂白原理
(3)向FeSO4溶液中滴加氯水,溶液变为黄色,写出反应的离子方程式
(4)据报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分为稀盐酸)与“84”消毒液(有效成分NaClO),而发生氯气中毒事件,请从氧化还原的角度分析原因
(5)一定量铁粉与氯气充分反应后,加适量水,完全溶解后无固体剩余,此时所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等,则已反应的Fe3+和未反应的Fe3+的质量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列问题
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ 。

(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用_______ 溶液吸收多余的氯气,原理是(用化学方程式表示)_______ 。
(3)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_______ (填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_______ (用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
(4)据“北方网”报道,2004年4月15日至16日,位于重庆市江北区的天原化工总厂相继发生氯气泄漏和爆炸事故,造成多人在事故中失踪、死伤,数十万人被紧急疏散。当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是_______(用字母代号填)。
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是

(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用
(3)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
A.O2 B.Cl2 C.CO2 D.HClO
(4)据“北方网”报道,2004年4月15日至16日,位于重庆市江北区的天原化工总厂相继发生氯气泄漏和爆炸事故,造成多人在事故中失踪、死伤,数十万人被紧急疏散。当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是_______(用字母代号填)。
| A.NaOH | B.NaCl | C.KBr | D.Na2CO3 |
您最近一年使用:0次



