(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,下图能正确表示该反应中能量变化的是_______ 。

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
则生成1molH2O(g)可以放出热量_______ kJ。
(2)下列反应中,属于放热反应的是_______ ,属于吸热反应的是_______ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D 四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向_______ 极(填“A”或“B”)。
②装置乙中正极的电极反应式为_______ 。
③四种金属活动性由强到弱的顺序是_______ 。

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
| 化学键 | H—H | O=O | H—O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D 四种金属按下表中装置进行实验。
| 装置 | 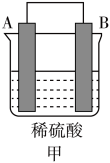 | 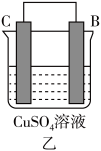 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
更新时间:2021-04-12 17:04:05
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题
(1)向某体积固定的密闭容器中加入0.3 A、0.1
A、0.1 C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的压强没有变化。请回答:
C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的压强没有变化。请回答:
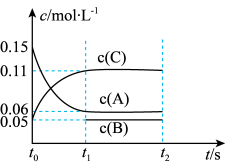
①该密闭容器的体积为_______ 升。
②若t1=15,则t0-t1内用C表示反应速率v(C) =_______ ;
③写出该反应的化学方程式:_______ 。
(2)已知断裂几种化学键要吸收的能量如下:
已知CO2、O2、H2O的结构式分别为O=C=O,O=O,H-O-H。1molCH4在O2中完全燃烧生成气态CO2和气态水时_______ (填“吸收”或 “放出”)热量。
(3)燃料电池是一种高效、环境友好的供电装置,如图为氢气燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从_______ 口通入(填“A”或“B”);
②a极的电极反应为:_______ 。
(1)向某体积固定的密闭容器中加入0.3
 A、0.1
A、0.1 C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的压强没有变化。请回答:
C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的压强没有变化。请回答:
①该密闭容器的体积为
②若t1=15,则t0-t1内用C表示反应速率v(C) =
③写出该反应的化学方程式:
(2)已知断裂几种化学键要吸收的能量如下:
| 化学键 | C-H | O=O | C=O | H-O |
| 断裂1mol键吸收的能量/kJ | 415 | 497 | 745 | 463 |
(3)燃料电池是一种高效、环境友好的供电装置,如图为氢气燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从
②a极的电极反应为:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】人们常常利用化学反应中的能量变化为人类服务。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如图所示:

根据上图可知,在化学反应中,不仅存在物质的变化,而且伴随着_______ 变化,1mol 完全燃烧生成1molH2O(气态)时,释放的能量是
完全燃烧生成1molH2O(气态)时,释放的能量是_______ kJ。
(2)下列化学反应在理论上可以设计成原电池的是_______ 。
A.CO2+C=2COB.
C.CH4+2O2 CO2+2H2OD.
CO2+2H2OD.
(3)某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验。实验结果记录加表:
根据表中记录的实验现象,回答下列问题。
①实验1中铝为_______ 极(填正或负)
②实验4中铝为_______ 极(填正或负),写出铝电极的电极反应式:_______ 。
③根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响?___ 。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如图所示:

根据上图可知,在化学反应中,不仅存在物质的变化,而且伴随着
 完全燃烧生成1molH2O(气态)时,释放的能量是
完全燃烧生成1molH2O(气态)时,释放的能量是(2)下列化学反应在理论上可以设计成原电池的是
A.CO2+C=2COB.

C.CH4+2O2
 CO2+2H2OD.
CO2+2H2OD.
(3)某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验。实验结果记录加表:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
①实验1中铝为
②实验4中铝为
③根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响?
您最近一年使用:0次
【推荐3】完成下列各题:
(1)已知下列热化学方程式:

 ;
;
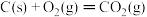
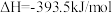 ;
;
回答下列问题:
① 的燃烧热为
的燃烧热为___________ ;
②燃烧1gC生成 ,放出的热量为
,放出的热量为___________ 。
(2)已知拆开1 氢气中的化学键需要消耗436
氢气中的化学键需要消耗436 能量,拆开1
能量,拆开1 氧气中的化学键需要消耗498
氧气中的化学键需要消耗498 能量,根据图中的能量图,回答下列问题:
能量,根据图中的能量图,回答下列问题:

①写出①②的数值:__________  ;
;__________  。
。
②已知:
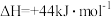 ,试写出2
,试写出2 氢气在足量氧气中完全燃烧生成液态水的热化学方程式
氢气在足量氧气中完全燃烧生成液态水的热化学方程式________________________________________ 。
(1)已知下列热化学方程式:

 ;
;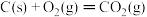
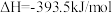 ;
;回答下列问题:
①
 的燃烧热为
的燃烧热为②燃烧1gC生成
 ,放出的热量为
,放出的热量为(2)已知拆开1
 氢气中的化学键需要消耗436
氢气中的化学键需要消耗436 能量,拆开1
能量,拆开1 氧气中的化学键需要消耗498
氧气中的化学键需要消耗498 能量,根据图中的能量图,回答下列问题:
能量,根据图中的能量图,回答下列问题:
①写出①②的数值:
 ;
; 。
。②已知:

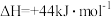 ,试写出2
,试写出2 氢气在足量氧气中完全燃烧生成液态水的热化学方程式
氢气在足量氧气中完全燃烧生成液态水的热化学方程式
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。 请回答下列问题。
(1)某同学做如下实验,以检验反应中的能量变化。___________ 热反应;(b)中温度降低,由此可以判断(b)中反应是___________ 热反应。
②写出铝与盐酸反应的离子方程式___________ 。
③根据能量守恒定律,(b)中反应物的总能量应该___________ 其生成物的总能量。(填“大于”、“小于”、“等于”)
(2)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。
①当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为___________ ,当电路中有0.2mol电子通过时,负极的质量减少___________ g。
②当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置___________ (填“能”或“不能”)形成原电池。
③将锌片和银片浸入硫酸铜溶液中组成原电池,两电极间连接一个电流表。
锌片上发生的电极反应为___________ ;
银片上发生的电极反应为___________ 。
(1)某同学做如下实验,以检验反应中的能量变化。
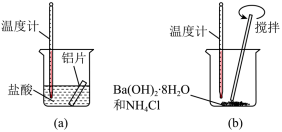
②写出铝与盐酸反应的离子方程式
③根据能量守恒定律,(b)中反应物的总能量应该
(2)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。
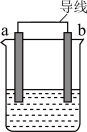
①当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为
②当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置
③将锌片和银片浸入硫酸铜溶液中组成原电池,两电极间连接一个电流表。
锌片上发生的电极反应为
银片上发生的电极反应为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】室温下将40 g已磨成粉末的Ba(OH)2•8H2O和20 g NH4Cl置于250 mL锥形瓶中,迅速搅拌将固体药品混合均匀,20 s后用带有玻璃管的单孔橡皮塞塞紧瓶口,玻璃管口悬挂一湿润的红色石蕊试纸,如图所示。试回答:
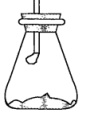
(1)湿润的红色石蕊试纸的变化是________ ,用化学方程式作出相关解释_______ 。
(2)若将锥形瓶中的Ba(OH)2•8H2O和NH4Cl换成__________ ,也可出现装置内温度降低的现象。

(1)湿润的红色石蕊试纸的变化是
(2)若将锥形瓶中的Ba(OH)2•8H2O和NH4Cl换成
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】反应 过程中的能量变化如下图所示,回答下列问题。
过程中的能量变化如下图所示,回答下列问题。_______ 热反应(填“吸”、“放”)。
②在反应体系中加入催化剂,反应速率增大,
_______ ,
_______ (填增大”、“减小”或“不变”)。
③当反应达到平衡时,升高温度,A的转化率_______ (填“增大”、“减小”或“不变”)。
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
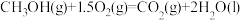
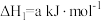
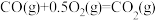
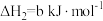
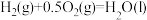
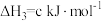
则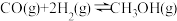

_______  (用a、b、c表示)。
(用a、b、c表示)。
(3)一定压强下,在容积为 的密闭容器中充入
的密闭容器中充入 与
与 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: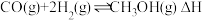 ,平衡转化率与温度、压强的关系如图所示。则
,平衡转化率与温度、压强的关系如图所示。则
_______  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
 过程中的能量变化如下图所示,回答下列问题。
过程中的能量变化如下图所示,回答下列问题。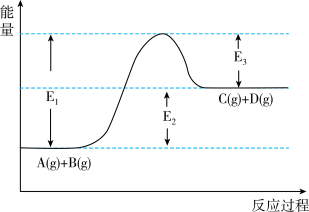
②在反应体系中加入催化剂,反应速率增大,


③当反应达到平衡时,升高温度,A的转化率
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
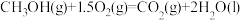
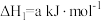
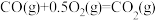
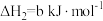
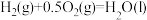
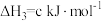
则
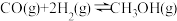

 (用a、b、c表示)。
(用a、b、c表示)。(3)一定压强下,在容积为
 的密闭容器中充入
的密闭容器中充入 与
与 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: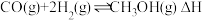 ,平衡转化率与温度、压强的关系如图所示。则
,平衡转化率与温度、压强的关系如图所示。则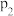
 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);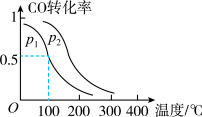
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】化学反应中的能量变化和化学反应条件的控制与人类的生产、生活密切相关。回答下列问题:
Ⅰ.已知在25℃和101kPa时,断裂1molH-H键吸收的能量为436kJ,断裂1molN-H键吸收的能量为391kJ,断裂1mol 键吸收的能量为945.6kJ。
键吸收的能量为945.6kJ。
(1)根据以上数据判断氨分解反应 是
是_______ (填“吸热”或“放热”)反应。
(2)在25℃时,取1mol 和3mol
和3mol 放入一密闭容器中,加入催化剂进行合成氨反应,理论上完全反应放出或吸收的热量为Q1,则Q1为
放入一密闭容器中,加入催化剂进行合成氨反应,理论上完全反应放出或吸收的热量为Q1,则Q1为_______ kJ。实际生产中,放出或吸收的热量为Q2,则Q1与Q2的大小关系为:Q1_______ Q2 (填“>”“<”或“=”)。
Ⅱ.微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇( )微生物燃料电池(如图所示)中,电解质溶液呈酸性。
)微生物燃料电池(如图所示)中,电解质溶液呈酸性。

(3)该电池中,外电路电流的流动方向为_______ (填“从A到B”或“从B到A”)。
(4)B电极附近氧气发生的电极反应为_______ 。
(5)该燃料电池的总反应为_______ 。
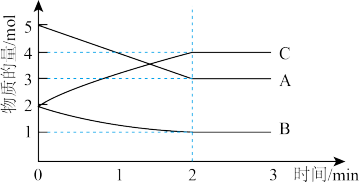
Ⅲ.某可逆反应在体积为2L的恒温恒容密闭容器中进行,0~3min各物质的物质的量的变化情况如图所示(A、C均为气体,B为固体)。
(6)该反应的化学方程式为_______ 。
(7)下列说法错误的是_______(填标号)。
Ⅰ.已知在25℃和101kPa时,断裂1molH-H键吸收的能量为436kJ,断裂1molN-H键吸收的能量为391kJ,断裂1mol
 键吸收的能量为945.6kJ。
键吸收的能量为945.6kJ。(1)根据以上数据判断氨分解反应
 是
是(2)在25℃时,取1mol
 和3mol
和3mol 放入一密闭容器中,加入催化剂进行合成氨反应,理论上完全反应放出或吸收的热量为Q1,则Q1为
放入一密闭容器中,加入催化剂进行合成氨反应,理论上完全反应放出或吸收的热量为Q1,则Q1为Ⅱ.微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇(
 )微生物燃料电池(如图所示)中,电解质溶液呈酸性。
)微生物燃料电池(如图所示)中,电解质溶液呈酸性。
(3)该电池中,外电路电流的流动方向为
(4)B电极附近氧气发生的电极反应为
(5)该燃料电池的总反应为
Ⅲ.某可逆反应在体积为2L的恒温恒容密闭容器中进行,0~3min各物质的物质的量的变化情况如图所示(A、C均为气体,B为固体)。

(6)该反应的化学方程式为
(7)下列说法错误的是_______(填标号)。
A.2min内A表示的反应速率为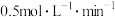 |
| B.增加B的物质的量,可使反应速率加快 |
| C.当容器内混合气体的密度保持不变时,该反应达到平衡状态 |
| D.当容器内压强保持不变时,该反应达到平衡状态 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】研究化学反应时,既要考虑物质变化与能量变化,又要关注反应的快慢与限度。回答下列问题:
I.能源是现代生产生活、科学研究和社会发展的重要支柱。化学反应中的能量变化,主要表现为化学能、热能、电能等的变化。
(1)下列反应中,既属于放热反应,在一定条件下又能设计成原电池反应的是_____ (填字母)。
(2)Fe-Cu原电池的装置如图所示。

①铁作____ (填“正极”或“负极”),溶液中H+向_____ (填“铁”或“铜”)电极方向移动。
②正极的现象是_____ ,负极的电极反应式为_____ 。
③若反应过程中有0.2mol电子发生转移,则生成的氢气在标准状况下的体积为____ L。
II.恒容密闭容器中发生反应NH2COONH4(s) 2NH3(g)+CO2(g),生成物氨气的浓度c(NH3)随反应时间的变化情况如表所示。
2NH3(g)+CO2(g),生成物氨气的浓度c(NH3)随反应时间的变化情况如表所示。
(3)在8~16s内,以CO2表示的平均反应速率v(CO2)=_____ mol•L-1•min-1,对于该反应,下列说法一定正确的是____ (填字母)。
A.加入合适的催化剂可加快该反应的速率,但并不改变其限度
B.32s时c(NH3)不再改变,说明此时该反应恰好到达平衡状态
C.将NH2COONH4研成粉末,可以缩短反应达到平衡的时间
D.当氨气的体积分数φ(NH3)不再改变时,说明该反应已达到化学平衡
I.能源是现代生产生活、科学研究和社会发展的重要支柱。化学反应中的能量变化,主要表现为化学能、热能、电能等的变化。
(1)下列反应中,既属于放热反应,在一定条件下又能设计成原电池反应的是
| A.NH4Cl与Ba(OH)2∙8H2O混合 | B.2C+O2 2CO 2CO |
C.C+CO2 2CO 2CO | D.H2SO4溶液与Ba(OH)2溶液中和 |

①铁作
②正极的现象是
③若反应过程中有0.2mol电子发生转移,则生成的氢气在标准状况下的体积为
II.恒容密闭容器中发生反应NH2COONH4(s)
 2NH3(g)+CO2(g),生成物氨气的浓度c(NH3)随反应时间的变化情况如表所示。
2NH3(g)+CO2(g),生成物氨气的浓度c(NH3)随反应时间的变化情况如表所示。| 时间/s | 0 | 8 | 16 | 24 | 32 | 400 |
| c(NH3)/(mol•L-1) | 0 | 1.3 | 1.8 | 2.1 | 2.2 | 2.2 |
A.加入合适的催化剂可加快该反应的速率,但并不改变其限度
B.32s时c(NH3)不再改变,说明此时该反应恰好到达平衡状态
C.将NH2COONH4研成粉末,可以缩短反应达到平衡的时间
D.当氨气的体积分数φ(NH3)不再改变时,说明该反应已达到化学平衡
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】在人类生产、生活对能量的需求日益增长的今天,研究化学反应及其能量变化,合理利用常规能源和开发新能源具有十分重要的意义。热能与电能都是人类赖以生存和发展不可缺少的因素。请回答下列问题:
表中的数据是破坏1mol物质中的化学键所消耗的能量,回答下列问题:
(1)下列氢化物中最稳定的是______ (填标号)。
A.HCl B.HBr C.HI
(2)按照反应I2+H2=2HI,生成2molHI_______ (填“吸收”或“放出”)的热量为______ kJ。
(3)绿色电源“直接二甲醚(CH3OCH3)燃料电池”的工作原理如图所示。
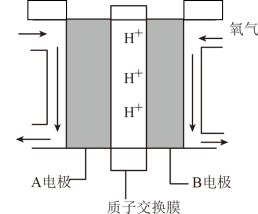
H+的移动方向为由______ 电极到_____ 电极(填“A”或“B”)。B电极的电极反应式______ 。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①放电时,正极发生_____ (填“氧化”或“还原”)反应。已知负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2,则正极的电极反应式为______ 。
②放电时,______ (填“正”或“负”)极附近溶液的碱性增强。
表中的数据是破坏1mol物质中的化学键所消耗的能量,回答下列问题:
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 键能/kJ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
A.HCl B.HBr C.HI
(2)按照反应I2+H2=2HI,生成2molHI
(3)绿色电源“直接二甲醚(CH3OCH3)燃料电池”的工作原理如图所示。

H+的移动方向为由
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。①放电时,正极发生
②放电时,
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】化学反应与能量变化是化学研究的重要问题,根据相关材料分析回答:
(1)已知断开1mol下列物质中的化学键需要吸收的能量如下表:
根据以上数据判断:N2 + O2 = 2NO属于___________ 反应(填“放热”或“吸热”)。
(2)符合某些特征的化学反应理论上都可以设计成原电池。下列化学反应___________ (填字母)不能设计成原电池,原因是___________ 。
A.CH4+2O2=CO2+2H2O
B.Fe+CuSO4=FeSO4+Cu
C.2NaOH + H2SO4 = Na2SO4 + 2H2O
D.Pb+PbO2+2H2SO4=2PbSO4+2H2O
(3)把A、B、C、D四种金属按表中装置进行实验。
根据表中信息判断四种金属活动性由大到小的顺序是___________ ;写出装置乙中正极的电极反应式:___________ 。
(4)锂离子电池已经成为新一代实用的蓄电池,它具有能量密度大、电压高的特性。某锂离子电池放电时电极反应如下:
负极Li-e-= Li+,
正极Li1-xMnO2+xLi++xe-=LiMnO2
该锂离子电池放电时电池的反应方程式为___________ 。
(1)已知断开1mol下列物质中的化学键需要吸收的能量如下表:
| 物质 | N2 | O2 | NO |
| 吸收的能量 | 946kJ | 498 kJ | 632kJ |
根据以上数据判断:N2 + O2 = 2NO属于
(2)符合某些特征的化学反应理论上都可以设计成原电池。下列化学反应
A.CH4+2O2=CO2+2H2O
B.Fe+CuSO4=FeSO4+Cu
C.2NaOH + H2SO4 = Na2SO4 + 2H2O
D.Pb+PbO2+2H2SO4=2PbSO4+2H2O
(3)把A、B、C、D四种金属按表中装置进行实验。
| 装置 | 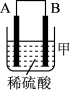 | 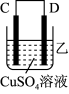 | 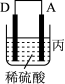 |
| 电子从A到B | C电极的质量增加 | 二价金属D不断溶解 |
根据表中信息判断四种金属活动性由大到小的顺序是
(4)锂离子电池已经成为新一代实用的蓄电池,它具有能量密度大、电压高的特性。某锂离子电池放电时电极反应如下:
负极Li-e-= Li+,
正极Li1-xMnO2+xLi++xe-=LiMnO2
该锂离子电池放电时电池的反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________ 。
(2)装置乙中正极的电极反应式是_______________________________________ 。
(3)装置丙中溶液的pH________ (填“变大”、“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是___________________________________ 。
| 装置 |  |  |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中负极的电极反应式是
(2)装置乙中正极的电极反应式是
(3)装置丙中溶液的pH
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】Ⅰ: 元素的金属活动性递变规律是元素周期表学习的重要内容之一。某校研究性学习小组查阅课外资料,看到第IVA族的三种金属锗、锡、铅的性质:“锗、锡在空气中不反应,铅在空气中表面生成一层氧化铅,请解释发生上述变化的原因是___________________________________________________________ 。
Ⅱ: 另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在下侧方框内画出原电池装置图。并写出正极的反应现象及电极反应式。
现象_______________________________ ;电极反应式___________________________ ;装置图:________________________

(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序。你的设计方法是___________________________________________________________________________
Ⅱ: 另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在下侧方框内画出原电池装置图。并写出正极的反应现象及电极反应式。
现象

(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序。你的设计方法是
您最近一年使用:0次



