已知: 。不同情况下反应过程的能量变化如图。下列结论正确的是
。不同情况下反应过程的能量变化如图。下列结论正确的是
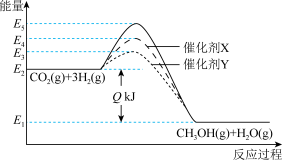
 。不同情况下反应过程的能量变化如图。下列结论正确的是
。不同情况下反应过程的能量变化如图。下列结论正确的是
A.1mol  (g)和3mol (g)和3mol  (g)混合后反应,放出Q kJ热量 (g)混合后反应,放出Q kJ热量 |
| B.催化剂可以改变反应途径,缩短达到平衡的时间 |
| C.当生成的水为液态时,Q值减小 |
| D.催化剂不同,反应的热效应不同 |
更新时间:2021-04-20 15:02:44
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】通过以下反应均可获取H2:
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g)∆H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g)∆H3=+206.1kJ•mol-1
下列有关说法错误的是
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g)∆H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g)∆H3=+206.1kJ•mol-1
下列有关说法错误的是
| A.反应①中光能转化为化学能 |
| B.反应②为吸热反应 |
| C.反应③使用催化剂,∆H3变小 |
| D.反应C(s)+2H2(g)=CH4(g)的∆H=-74.8kJ•mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】已知下列热化学方程式:
(1)CH4(g) + 2O2(g)=CO2(g) + 2H2O(l) △H= - 890.0kJ/mol
(2)2C2H6(g) + 7O2(g )=4CO2 (g)+ 6H2O(l) △H= - 3119.6kJ/mol
(3) C2H4(g) + 3O2(g) =2CO2(g) + 2H2O(l) △H= - 1411.0kJ/mol
(4) 2C2H2(g) + 5O2(g)=4CO2(g) + 2H2O(l) △H= - 2599.2kJ/mol
(5)C3H8(g) + 5O2(g)=3CO2(g) + 4H2O(l) △H= - 2219.9kJ/mol
现有由上述五种烃中的两种组合成的混合气体2mol,经充分燃烧后放出2970.8kJ热量,则下列哪些组合是不可能的
(1)CH4(g) + 2O2(g)=CO2(g) + 2H2O(l) △H= - 890.0kJ/mol
(2)2C2H6(g) + 7O2(g )=4CO2 (g)+ 6H2O(l) △H= - 3119.6kJ/mol
(3) C2H4(g) + 3O2(g) =2CO2(g) + 2H2O(l) △H= - 1411.0kJ/mol
(4) 2C2H2(g) + 5O2(g)=4CO2(g) + 2H2O(l) △H= - 2599.2kJ/mol
(5)C3H8(g) + 5O2(g)=3CO2(g) + 4H2O(l) △H= - 2219.9kJ/mol
现有由上述五种烃中的两种组合成的混合气体2mol,经充分燃烧后放出2970.8kJ热量,则下列哪些组合是不可能的
| A.CH4和C3H8 | B.C2H4和C3H8 | C.C2H6和C3H8 | D.C2H6和CH4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】甲烷与氯气在光照条件下取代反应的部分反应历程和能量变化如下:
链引发:Cl2(g) → 2Cl·(g) ΔH1=+242.7 kJ/mol
链增长
①:CH4(g) + Cl·(g) → CH3·(g) + HCl(g) ΔH2=+7.5 kJ/mol
②:CH3·(g) + Cl2(g) → CH3Cl(g) + Cl·(g) ΔH3=-129 kJ/mol
……
链终止:Cl·(g) + CH3·(g) → CH3Cl(g) ΔH4=-371.7 kJ/mol
(其中CH3·表示甲基,Cl·表示氯原子)下列说法错误的是
链引发:Cl2(g) → 2Cl·(g) ΔH1=+242.7 kJ/mol
链增长
①:CH4(g) + Cl·(g) → CH3·(g) + HCl(g) ΔH2=+7.5 kJ/mol
②:CH3·(g) + Cl2(g) → CH3Cl(g) + Cl·(g) ΔH3=-129 kJ/mol
……
链终止:Cl·(g) + CH3·(g) → CH3Cl(g) ΔH4=-371.7 kJ/mol
(其中CH3·表示甲基,Cl·表示氯原子)下列说法错误的是
| A.在链终止的过程中,还可能会生成少量的乙烷 |
| B.CH3Cl(g)中C-Cl键的键能小于Cl2(g)中Cl-Cl键的键能 |
| C.CH4(g) + Cl2(g) → CH3Cl(g) + HCl(g) ΔH=-121.5 kJ/mol |
| D.若是CH4与Br2(g)发生取代反应,则链增长①反应的ΔH>+7.5 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知2H2(g)+ O2(g)=2H2O(g) △H= ─484KJ/moL,则反应H2O(g)= H2(g)+ 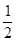 O2(g) 的△H为
O2(g) 的△H为
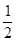 O2(g) 的△H为
O2(g) 的△H为| A.─484kJ/mol | B.+484kJ/mol | C.─242kJ/mol | D.+242kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】可逆反应2SO2+O2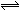 2SO3在密闭容器中进行。下列说法正确的是
2SO3在密闭容器中进行。下列说法正确的是
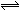 2SO3在密闭容器中进行。下列说法正确的是
2SO3在密闭容器中进行。下列说法正确的是| A.使用催化剂不能改变反应速率 |
| B.达平衡时SO2与SO3的浓度相等 |
| C.增大压强能加快反应速率 |
| D.SO2与O2反应能完全转化为SO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】以反应 5H2C2O4+2MnO4+6H=10CO2↑+2Mn+8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
下列说法不正确的是
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
| A.实验①和实验②是探究温度对化学反应速率的影响,实验②和实验③是探究浓度对化学反应速率的影响 |
| B.实验①②③所加的H2C2O4溶液均要过量 |
| C.若实验①测得 KMnO4 溶液的褪色时间为40s,则这段时间内平均反应速率υ (KMnO4)=1.7×10-4mol/(L·s) |
| D.实验①和实验②起初反应均很慢,过一会儿反应速率突然增大,可能是生成的Mn2+对反应起催化作用 |
您最近一年使用:0次

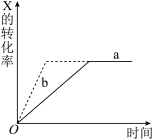
 2Z(g)+W(g)(正反应为放热反应)的反应过程。若使a曲线变为b曲线,
2Z(g)+W(g)(正反应为放热反应)的反应过程。若使a曲线变为b曲线,