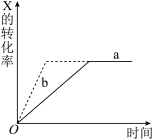
如图所示,a曲线表示一定条件可逆反应X(g)+Y(g) 2Z(g)+W(g)(正反应为放热反应)的反应过程。若使a曲线变为b曲线,
2Z(g)+W(g)(正反应为放热反应)的反应过程。若使a曲线变为b曲线,可 采取的措施是( )
 2Z(g)+W(g)(正反应为放热反应)的反应过程。若使a曲线变为b曲线,
2Z(g)+W(g)(正反应为放热反应)的反应过程。若使a曲线变为b曲线,
| A.加入催化剂 | B.增大Y的浓度 |
| C.降低温度 | D.增大体系压强 |
更新时间:2020-11-02 17:17:01
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知
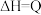 kJ⋅mol
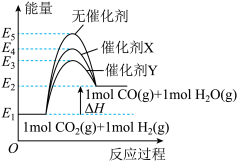
kJ⋅mol 。不同条件下反应过程的能量变化如图,下列说法正确的是
。不同条件下反应过程的能量变化如图,下列说法正确的是

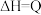 kJ⋅mol
kJ⋅mol 。不同条件下反应过程的能量变化如图,下列说法正确的是
。不同条件下反应过程的能量变化如图,下列说法正确的是
A. |
| B.改变催化剂不仅改变了反应过程也改变了反应的焓变 |
| C.催化剂Y的效果比催化剂X的更好 |
D.无催化剂时,断开反应物中所有化学键需要吸收能量 kJ kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】氮及其化合物的转化过程如下图所示。下列说法不正确的是
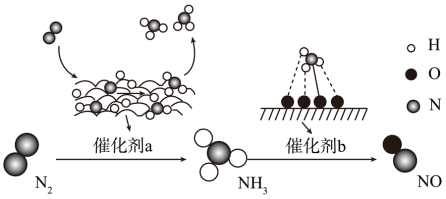

| A.催化剂a表面发生了共价键的断裂和形成 |
| B.催化剂a、b都能加快该反应的速率 |
| C.氨的催化氧化反应中还原剂为NH3,还原产物为NO和H2O |
| D.取0.5 mol N2经过上述两个反应后生成NO,共转移电子的物质的量为8mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列实验现象不能 用平衡移动原理解释的是
 将  球浸泡在冷水和热水中 球浸泡在冷水和热水中 |  将20mL  吸入注射器,活塞拉到不同位置 吸入注射器,活塞拉到不同位置 |
| A | B |
 |  |
| C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】对于已达化学平衡的下列反应:2 X (g) + Y (g)  2 Z (g) ,减小压强时,对反应产生的影响是
2 Z (g) ,减小压强时,对反应产生的影响是
 2 Z (g) ,减小压强时,对反应产生的影响是
2 Z (g) ,减小压强时,对反应产生的影响是| A.正反应速率增大,逆反应速率减小,平衡向逆反应方向移动 |
| B.正反应速率减小,逆反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
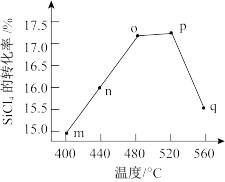
【推荐1】SiCl4是一种重要的化工原料,SiCl4氢化为SiHCl3的反应方程式为:3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g),其转化率随温度变化如图所示。下列说法错误的是
4SiHCl3(g),其转化率随温度变化如图所示。下列说法错误的是
 4SiHCl3(g),其转化率随温度变化如图所示。下列说法错误的是
4SiHCl3(g),其转化率随温度变化如图所示。下列说法错误的是
| A.n点v正>v逆 |
| B.m点v逆大于q点v逆 |
| C.p点后,转化率下降可能是平衡左移 |
| D.加压有利于提高混合气体中SiHCl3的体积分数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】工业制硫酸工艺的催化氧化反应原理是:2SO2(g)+O2(g) 2SO3(g)ΔH<0,起始以相同的物质的量进行投料,测得SO2在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
2SO3(g)ΔH<0,起始以相同的物质的量进行投料,测得SO2在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是

 2SO3(g)ΔH<0,起始以相同的物质的量进行投料,测得SO2在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
2SO3(g)ΔH<0,起始以相同的物质的量进行投料,测得SO2在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
| A.温度:T1>T2>T3 |
| B.正反应速率:υ(a)>υ(c)、υ(b)>υ(d) |
| C.平均摩尔质量:M(a)>M(c)、M(b)>M(d) |
| D.平衡常数:K(a)>K(c)、K(b)>K(d) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】一定条件下,通过下列反应可以制备特种陶瓷的原料 MgO, MgSO4(s) + CO(g) ⇌ MgO(s) + CO2(g) + SO2(g) ΔH > 0。该反应在恒容的密闭容器中达到平衡后(A 点),若仅改变图中横坐标 x 的值, 重新达到平衡后,纵坐标 y 随 x 变化趋势合理的是( )(忽略固体物质所占有的体积)
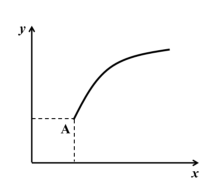

| A.x 为温度,y 为容器内混合气体的密度 |
| B.x 为 MgSO4的质量,y 为 CO 的平衡转化率 |
| C.x 为 CO2的物质的量,y 为 CO 的平衡转化率 |
| D.x 为 SO2的浓度,y 为 CO2的平衡浓度 |
您最近一年使用:0次

 “仿生递送”治疗白血病
“仿生递送”治疗白血病 排放
排放 催化下实现
催化下实现 的高效氧化
的高效氧化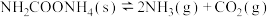 。不同温度下的平衡数据如下表:
。不同温度下的平衡数据如下表: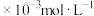 )
)
 体积分数不变时,该反应达到平衡状态
体积分数不变时,该反应达到平衡状态



