下表标出的是元素周期表的一部分元素,回答下列问题:
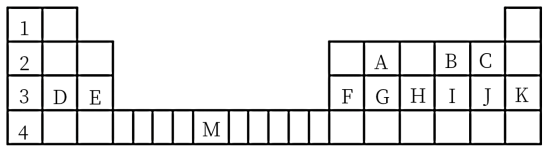
(1)除稀有气体外第三周期中原子半径最大的是___________ (填元素符号)
(2)表中用字母标出的12种元素中,化学性质最不活泼的是___________ (用元素符号表示,下同),非金属性最强的是___________ (用元素符号表示),属于过渡元素的是___________ (用表中的字母表示)。
(3)化合物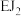 中含有的化学键为
中含有的化学键为___________ 。(填“离子键’”、“极性共价键”、“非极性共价键”)
(4)用电子式表示A的简单气态氢化物的形成过程___________ 。
(5)D、F元素最高价氧化物对应水化物相互反应的离子方程式为___________

(1)除稀有气体外第三周期中原子半径最大的是
(2)表中用字母标出的12种元素中,化学性质最不活泼的是
(3)化合物
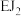 中含有的化学键为
中含有的化学键为(4)用电子式表示A的简单气态氢化物的形成过程
(5)D、F元素最高价氧化物对应水化物相互反应的离子方程式为
更新时间:2021-04-25 22:35:43
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C、D四种元素,A元素的原子有三个电子层,最外层上有一个电子;B元素负2价阴离子的电子层结构与氩原子相同;C元素的原子核内无中子;D原子核外电子数比A原子核外电子总数多6个。
(1)C与D形成化合物的化学式_______ ,其在水中的电离方程式为_______ 。
(2)B离子的电子式_______ ,A离子的电子式_______ 。
(3)B原子的结构示意图_______ ,D离子的结构示意图_______ 。
(1)C与D形成化合物的化学式
(2)B离子的电子式
(3)B原子的结构示意图
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(一)
(1)化学组成为BDF2的电子式为:__________ ,A、C、F三种元素形成的化合物CA4F为___________ 化合物(填“离子”或“共价”)。
(2)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:____________________ 。
(3)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是_________ (用元素离子符号表示)。
(4)元素B和F的非金属性强弱,B的非金属性________ 于F(填“强”或“弱”),并用化学方程式证明上述结论________________________ 。
(二)以CA3代替氢气研发燃料电池是当前科研的一个热点。
(1)CA3燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4 A3+3O2=2C2+6H2O.该电池负极的电极反应式为________ ;每消耗3.4g CA3转移的电子数目为__________ 。

(2)用CA3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为_________ ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为________ L。
(一)
(1)化学组成为BDF2的电子式为:
(2)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:
(3)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是
(4)元素B和F的非金属性强弱,B的非金属性
(二)以CA3代替氢气研发燃料电池是当前科研的一个热点。
(1)CA3燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4 A3+3O2=2C2+6H2O.该电池负极的电极反应式为

(2)用CA3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F是原子序数依次递增的前四周期元素。A是宇宙中含量最丰富的元素;D与E同主族,且E的原子序数是D的两倍;B与D组成的化合物是一种温室气体;C元素原子最外层p能级比s能级多1个电子;F原子的最外层电子数与A相同,其余各层均充满。据此回答下列问题。
(1)F元素形成的高价基态离子的价电子排布图为_______ 。
(2)E的一种具有强还原性的氧化物分子的VSEPR模型为_______ 。
(3)C、D、E元素的第一电离能由大到小顺序是_______ (用元素符号表示)。
(4)A和D形成的18电子化合物难溶于BE2,其理由是_______ ,此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为_______ 。
(5)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L甲气体与0.5 L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是_______ 。
(6)F与C形成化合物的晶胞如图所示,该化合物的化学式为_______ ,C离子的配位数是_______ 。F离子在水溶液中形成的离子中共价键共_______ 。

(1)F元素形成的高价基态离子的价电子排布图为
(2)E的一种具有强还原性的氧化物分子的VSEPR模型为
(3)C、D、E元素的第一电离能由大到小顺序是
(4)A和D形成的18电子化合物难溶于BE2,其理由是
(5)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L甲气体与0.5 L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是
(6)F与C形成化合物的晶胞如图所示,该化合物的化学式为

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在周期表中的位置_____ ,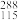 Mc 的中子数为
Mc 的中子数为_____ 。已知存在P(S,红磷)、P(S,黑磷) 、P(S,白磷),它们互称为_____ 。
(2)热稳定性:NH3_____ PH3(填“>”或“<”),砷的最高价氧化物对应水化物的化学式为_____ 是一种_____ 酸(填“强”或“弱”) 。
(3)PH3 和卤化氢反应与 NH3 相似,产物的结构和性质也相似。写出 PH3 和 HI 反应的化学方程式_____ 。
(4)SbCl3 能发生较强烈的水解,生成难溶的 SbOCl,写出该反应的化学方程式_____ ,因此,配制 SbCl3溶液时应注意_________ 。
(1)砷在周期表中的位置
 Mc 的中子数为
Mc 的中子数为(2)热稳定性:NH3
(3)PH3 和卤化氢反应与 NH3 相似,产物的结构和性质也相似。写出 PH3 和 HI 反应的化学方程式
(4)SbCl3 能发生较强烈的水解,生成难溶的 SbOCl,写出该反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有短周期主族元素X、Y、Z、R、W、T,R原子最外层电子数是电子层数的2倍,Z是金属元素,Y与Z能形成Z2Y、Z2Y2型化合物,W元素形成的氧化物具有两性,TY2是一种新型高效自来水消毒杀菌剂,五种元素的原子半径与原子序数的关系如图所示,按要求回答下列问题:
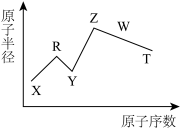
(1)X在元素周期表中的位置是_______ ;T的离子结构示意图为_______ .
(2) Z2Y2的电子式为_______ ,属于_______ 化合物(离子或共价),写出该物质与水反应的离子方程式_______ 。
(3)Y、Z、W、T简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(4)Z最高价氧化物对应水化物与W元素氧化物反应的化学方程式为_______
(5)下列说法正确且能证明元素金属性Z大于W的是_______(填标号)。

(1)X在元素周期表中的位置是
(2) Z2Y2的电子式为
(3)Y、Z、W、T简单离子半径由大到小的顺序为
(4)Z最高价氧化物对应水化物与W元素氧化物反应的化学方程式为
(5)下列说法正确且能证明元素金属性Z大于W的是_______(填标号)。
| A.Z元素单质的熔点比W元素单质的熔点低 |
| B.Z元素的单质能置换出WT3溶液中W元素的单质 |
| C.Z、W最高价氧化物对应水化物的碱性:Z>W |
| D.等物质的量的Z、W元素单质分别与酸反应失去电子数目:Z<W |
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】几种主族元素在周期表中的位置如表:
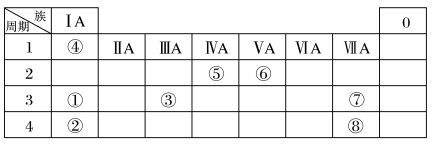
根据表回答下列问题:
(1)⑥元素的氢化物的结构式是_____ 、⑤的最高价氧化物电子式_____ 。
(2)①③⑦三种元素原子半径由大到小的顺序是____ (用元素符号表示)。
(3)表中8种元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_____ ,该元素在周期表中的位置是____ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_____ (填化学式),①与③最高价氧化物对应水化物反应的离子方程式为_____ 。
(5)非金属性强弱比较⑦_____ ⑧(填写“大于”或“小于”)下列表述中能证明这一事实的是_____ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
(6)①的最高价氧化物的水化物是_____ (填“离子”或“共价”)化合物。

根据表回答下列问题:
(1)⑥元素的氢化物的结构式是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中8种元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)非金属性强弱比较⑦
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
(6)①的最高价氧化物的水化物是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表为周期表的一部分,其中的字母代表对应的元素,请针对这些元素回答下列问题.
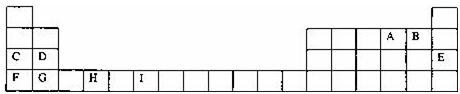
请回答下列问题:
(1)元素I的元素符号 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族.
(2)表中元素第一电离能最小的是 (填元素符号,下同),电负性最大的是 ,化学性质最稳定的是 .
(3)表中元素处于d区的是 (填元素符号).
(4)请举出F的金属性比C强的实验事实: ,并用原子结构理论解释其原因: .

请回答下列问题:
(1)元素I的元素符号 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族.
(2)表中元素第一电离能最小的是 (填元素符号,下同),电负性最大的是 ,化学性质最稳定的是 .
(3)表中元素处于d区的是 (填元素符号).
(4)请举出F的金属性比C强的实验事实: ,并用原子结构理论解释其原因: .
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,T元素为地壳中含量最多的金属元素。
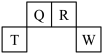
请回答下列问题:
(1)T的离子结构示意图为______________ ;
(2)元素的非金属性为:Q_____________ R(填“强于”或“弱于”);
(3)R元素的氢化物的电子式为________________ ;
(4)T的单质与同周期金属性最强元素最高价氧化物对应的水化物反应的离子方程式为______________________________________ ;
(5)T的单质与W的最高价氧化物的水化物浓溶液共热,一段时间后发现固态表面有大量无色气泡冒出,同时还异常地嗅到了一股刺激性气味。你猜想该气体是_________ (填化学式),请你设计一个简单的实验方案证明你的猜想___________________________________ 。

请回答下列问题:
(1)T的离子结构示意图为
(2)元素的非金属性为:Q
(3)R元素的氢化物的电子式为
(4)T的单质与同周期金属性最强元素最高价氧化物对应的水化物反应的离子方程式为
(5)T的单质与W的最高价氧化物的水化物浓溶液共热,一段时间后发现固态表面有大量无色气泡冒出,同时还异常地嗅到了一股刺激性气味。你猜想该气体是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E三种原子最外层共有10个电子,且这三种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:A_______ ,B_______ ,C_______ ,D_______ 。
(2)C单质的常见用途:_______ 。(写一种)
(3)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:_______ 。
(4)写出A、B两元素的最高价氧化物的水化物之间相互反应的化学方程式:_______ 。
(1)写出下列元素符号:A
(2)C单质的常见用途:
(3)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(4)写出A、B两元素的最高价氧化物的水化物之间相互反应的化学方程式:
您最近半年使用:0次



