化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。
(1)下列变化属于放热反应的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.碳酸氢钠固体溶于盐酸
d.铜溶于浓硝酸 e.氯化铵固体与氢氧化钡晶体混合搅拌 f.过氧化钠溶于水
(2)H2O2分解时的能量变化关系如图所示,则H2O2分解反应为___________ 反应 (选填:吸热、放热)。
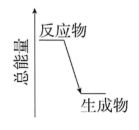
查阅资料得知:将作为催化剂的Fe2(SO4)3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是:2Fe3++H2O2=2Fe2++O2↑+2H+和___________ 。
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置:
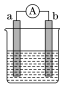
①当电极a为镁,电极b为铝,电解质溶液为氢氧化钠溶液时,该电池的负极为___________ (填名称)。
②燃料电池的工作原理是将燃料和氧化剂(O2)反应所产生的化学能直接转化为电能。现设计一燃料电池,电极a通入氢气燃料,采用氢氧化钠溶液为电解液,b极的电极反应式为___________ 。
③质量相同的铜棒和铁棒用导线连接后插入CuSO4溶液中,一段时间后,取出洗净、干燥、称量,二者质量差为12 g,则导线中通过的电子的数目为___________ 。
(1)下列变化属于放热反应的是
a.生石灰溶于水 b.浓硫酸稀释 c.碳酸氢钠固体溶于盐酸
d.铜溶于浓硝酸 e.氯化铵固体与氢氧化钡晶体混合搅拌 f.过氧化钠溶于水
(2)H2O2分解时的能量变化关系如图所示,则H2O2分解反应为

查阅资料得知:将作为催化剂的Fe2(SO4)3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是:2Fe3++H2O2=2Fe2++O2↑+2H+和
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置:

①当电极a为镁,电极b为铝,电解质溶液为氢氧化钠溶液时,该电池的负极为
②燃料电池的工作原理是将燃料和氧化剂(O2)反应所产生的化学能直接转化为电能。现设计一燃料电池,电极a通入氢气燃料,采用氢氧化钠溶液为电解液,b极的电极反应式为
③质量相同的铜棒和铁棒用导线连接后插入CuSO4溶液中,一段时间后,取出洗净、干燥、称量,二者质量差为12 g,则导线中通过的电子的数目为
更新时间:2021-05-11 16:42:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】实验室可以根据下列方程式制备氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;根据反应回答下列问题:
MnCl2+Cl2↑+2H2O;根据反应回答下列问题:
(1)反应①的离子方程式为(MnCl2为易溶易电离的物质)_________ 。
(2)用双线桥法表示该反应中电子转移的方向和数目_________ 。
(3)浓盐酸在该反应中的作用是(填序号)_________ ①氧化性②还原性③酸性,若在标准状况下,制得氯气的体积为2.24L,则被氧化的氯化氢的物质的量为_________ 。
 MnCl2+Cl2↑+2H2O;根据反应回答下列问题:
MnCl2+Cl2↑+2H2O;根据反应回答下列问题:(1)反应①的离子方程式为(MnCl2为易溶易电离的物质)
(2)用双线桥法表示该反应中电子转移的方向和数目
(3)浓盐酸在该反应中的作用是(填序号)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在反应2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O中,氧化剂是________ ,氧化产物是________ ,氧化产物与还原产物的物质的量之比为________ ,被氧化与未被氧化的HCl的质量之比为________ ,若有73 g HCl被氧化,电子转移的总数为________ (用NA表示阿伏加德罗),标准状况生成Cl2的体积为________ L。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】北京时间2022年12月4日20时09分,神舟十四号载人飞船返回舱在东风着陆场成功着陆。搭载神舟十四号载人飞船的是长征二号F遥十四运载火箭。
燃料主要有:①煤油 ②液氢 ③肼( ) ④固态铝粉
) ④固态铝粉
氧化剂主要有:⑤液氧 ⑥ ⑦高氯酸铵(
⑦高氯酸铵( )
)
(1)16g肼中含有H原子数目约为___________ 个。
(2)同温同压下,氧气与氢气的密度之比为___________ 。
(3)飞船以铝粉与高氨酸铵的混合物为固体燃料,其中高氯酸铵发生分解反应生成: 、
、 、
、 、和
、和 。请写出该反应的化学方程式:
。请写出该反应的化学方程式:___________ ,其中被氧化的元素是______ ,还原产物是______ 。
(4)空间站中可利用过氧化钠与人体代谢的 、
、 反应制备呼吸必需的
反应制备呼吸必需的 。过氧化钠的颜色为
。过氧化钠的颜色为_______ ,其中阴离子与阳离子的个数比为______ 。写出 与
与 反应的化学方程式
反应的化学方程式_______ 。在25℃和101 的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为_______ L,转移电子数目为_______ 个。
燃料主要有:①煤油 ②液氢 ③肼(
 ) ④固态铝粉
) ④固态铝粉氧化剂主要有:⑤液氧 ⑥
 ⑦高氯酸铵(
⑦高氯酸铵( )
)(1)16g肼中含有H原子数目约为
(2)同温同压下,氧气与氢气的密度之比为
(3)飞船以铝粉与高氨酸铵的混合物为固体燃料,其中高氯酸铵发生分解反应生成:
 、
、 、
、 、和
、和 。请写出该反应的化学方程式:
。请写出该反应的化学方程式:(4)空间站中可利用过氧化钠与人体代谢的
 、
、 反应制备呼吸必需的
反应制备呼吸必需的 。过氧化钠的颜色为
。过氧化钠的颜色为 与
与 反应的化学方程式
反应的化学方程式 的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
的条件下,若有78g过氧化钠参加反应,生成氧气的体积约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】减少交通事故除遵守交通法规正确驾驶外,安全措施也极为重要。汽车的安全气嚢内一般充入的是叠氮化钠(NaN3)、硝酸铵(NH4NO3)、硝酸钾(KNO3)等物质。当汽车在高速行驶中受到猛烈撞击时,这些物质会迅速发生分解或发生反应,产生大量气体,充满气囊,从而保护驾驶员和乘客的安全。请回答下列问题:
(1)下列判断正确的是_______。
(2)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:
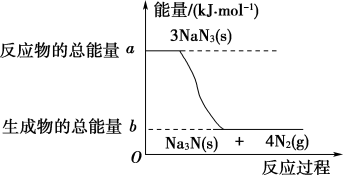
①叠氮化钠的爆炸反应属于_______ (填“吸热”或“放热”)反应。
②若爆炸过程中有30mol非极性键生成(一个共用电子对为一个化学键),则反应的能量变化为_______ kJ(用含a、b的代数式表示),消耗叠氮化钠的质量为_______ g。
(3)若安全气囊内充的是叠氮酸钠和硝酸钾,撞击时发生的反应是10NaN3+2KNO3=K2O+5Na2O+16N2↑。当该反应的氧化产物比还原产物多1.4mol时,转移电子的物质的量是_______ mol;同时气囊内还必须充入一定量的SiO2粉末,其在安全气囊内所起的作用可能是_______ 。
(1)下列判断正确的是_______。
| A.道路起雾与H2O分子的化学键断裂有关 |
| B.NH4NO3、KNO3中均含有离子键和共价键 |
| C.NaN3不会和酸性高锰酸钾或次氯酸钠溶液反应 |
| D.NaN3、NH4NO3固体在储存和使用时都必须格外小心,以免发生爆炸 |

①叠氮化钠的爆炸反应属于
②若爆炸过程中有30mol非极性键生成(一个共用电子对为一个化学键),则反应的能量变化为
(3)若安全气囊内充的是叠氮酸钠和硝酸钾,撞击时发生的反应是10NaN3+2KNO3=K2O+5Na2O+16N2↑。当该反应的氧化产物比还原产物多1.4mol时,转移电子的物质的量是
您最近一年使用:0次
【推荐2】20世纪初德国化学家哈伯(F.Haber)发明工业合成氨,人工制出氮肥,粮食产量显著提高,为解决人类温饱做出重大贡献。回答下列问题:
(1)合成氨的原料H2主要来源于煤的综合利用,如煤的气化: (吸热反应),煤的气化反应过程中能量变化可表示为
(吸热反应),煤的气化反应过程中能量变化可表示为_______ (填字母)。 纳米复合物)能以太阳光为能源,使水分解获得
纳米复合物)能以太阳光为能源,使水分解获得 ,其原理如图所示。反应①的化学方程式是
,其原理如图所示。反应①的化学方程式是_______ 。_______ (填“极性键”或“非极性键”,下同),形成的化学键是_______ 。
②生成17gNH3时,该反应_______ (填“吸收”或“放出”)的能量为_______ kJ。
(1)合成氨的原料H2主要来源于煤的综合利用,如煤的气化:
 (吸热反应),煤的气化反应过程中能量变化可表示为
(吸热反应),煤的气化反应过程中能量变化可表示为
 纳米复合物)能以太阳光为能源,使水分解获得
纳米复合物)能以太阳光为能源,使水分解获得 ,其原理如图所示。反应①的化学方程式是
,其原理如图所示。反应①的化学方程式是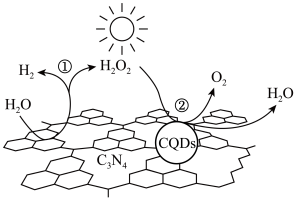
②生成17gNH3时,该反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
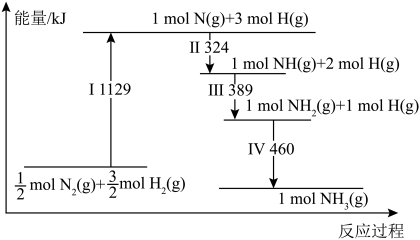
【推荐3】I.化学反应中伴随着能量变化,根据相关知识回答下列问题:
(1)下列过程吸热的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为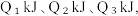 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是___________ (填序号)。
①.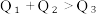 ②.
②. 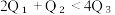 ③.
③. 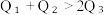 ④.
④. 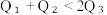
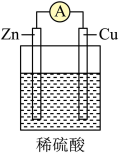
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。___________ 。
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)___________ 。
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为___________ ,___________ (填“电子”或“电流”)是由锌片经导线流向铜片。标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为___________ L。
(6)某同学想利用反应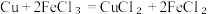 设计一个原电池请在下图
设计一个原电池请在下图___________ (共2处)标出使用的用品。
(1)下列过程吸热的是
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为
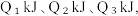 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是①.
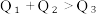 ②.
②. 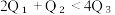 ③.
③. 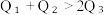 ④.
④. 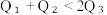
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为
(6)某同学想利用反应
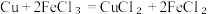 设计一个原电池请在下图
设计一个原电池请在下图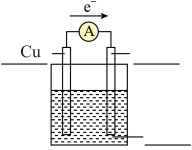
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图为原电池的装置示意图。
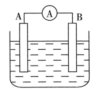
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成原电池,这两个原电池中,作负极的分别是_______ (填字母)。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:____ 。
(2)若A、B均为铂片,电解质溶液为NaOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:____ 。该电池在工作一段时间后,溶液的碱性将____ (填“增强”、“减弱”或“不变”)
(3)若A、B均为铂片,电解质溶液为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:___ 。若该电池反应消耗了6.4gCH4,则转移电子的数目为____ 。

(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成原电池,这两个原电池中,作负极的分别是
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:
(2)若A、B均为铂片,电解质溶液为NaOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:
(3)若A、B均为铂片,电解质溶液为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按图所示装置进行实验,装置中电解质溶液为0.5mol·L-1的稀硫酸。
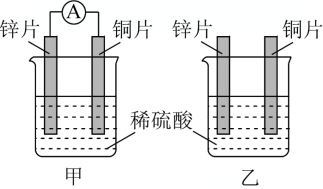
(1)对于甲乙装置,下列叙述正确的是_______ 。
(2)甲装置中SO 向
向_______ 极(填“正”或“负”)移动,正极的电极反应式为_______ 。
(3)若将甲装置中稀硫酸换成CuSO4溶液,一段时间后测得某电极增重12.8g,此时该电池反应共转移电子数为_______ 。

(1)对于甲乙装置,下列叙述正确的是
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片作正极,乙中铜片作负极 |
| C.两烧杯溶液中H+浓度均减小 |
| D.甲产生气泡的速率比乙慢 |
 向
向(3)若将甲装置中稀硫酸换成CuSO4溶液,一段时间后测得某电极增重12.8g,此时该电池反应共转移电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:
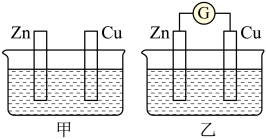
(1)以下叙述中,正确的是________ 。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的pH均增大
D.乙中电子从铜片经导线流向锌片
E.乙溶液中SO 向锌片方向移动
向锌片方向移动
(2)变化过程中能量转化的形式主要是:甲为______ (填写选项字母);乙为_______ (同前)。
A.将化学能转化成热能 B.将电能转化成为化学能 C.将化学能转化成电能
(3)若反应过程中有2mol电子发生转移,则生成的氢气在标况下的体积为_______ ;溶液质量增加_______ g。
(4)原电池在工作时,下列反应可以作为原电池工作时发生的反应的是:_______ 。
(5)化学反应速率的研究对工农业生产和日常生活有着十分重要的意义,下列操作不能加快化学反应速率的是:_______ 。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的pH均增大
D.乙中电子从铜片经导线流向锌片
E.乙溶液中SO
 向锌片方向移动
向锌片方向移动(2)变化过程中能量转化的形式主要是:甲为
A.将化学能转化成热能 B.将电能转化成为化学能 C.将化学能转化成电能
(3)若反应过程中有2mol电子发生转移,则生成的氢气在标况下的体积为
(4)原电池在工作时,下列反应可以作为原电池工作时发生的反应的是:
| A.Cu+2AgNO3=Cu(NO3)2+2Ag |
| B.H2SO4+Na2SO3=Na2SO4+SO2+H2O |
| C.NaOH+HCl=NaCl+H2O |
| D.2H2+O2=2H2O |
(5)化学反应速率的研究对工农业生产和日常生活有着十分重要的意义,下列操作不能加快化学反应速率的是:
| A.低温冷藏食物 |
| B.燃煤发电时用煤粉代替煤块 |
| C.用H2O2制备O2时,使用MnO2作催化剂 |
| D.用70%的硫酸溶液代替98%的浓硫酸与Na2SO3粉末反应制备SO2 |
您最近一年使用:0次



