某化学兴趣小组为了探究SO2的性质以及硫酸型酸雨的形成设计了如图的实验。
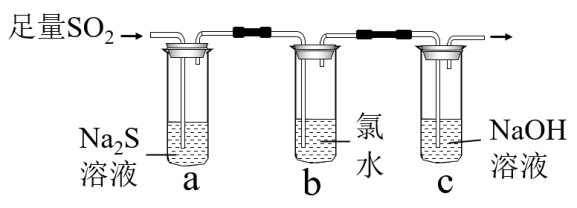
请回答下列问题:
(1)装置a中可观察到的现象为___ ,说明SO2具有的性质是___ 。
(2)装置b中产生的现象为___ ,写出其反应的离子方程式:___ 。
(3)装置c的作用是___ 。
(4)SO2形成酸雨的另一途径为SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4,则在此过程中的飘尘是作为___ (填“催化剂”或“氧化剂”)。

请回答下列问题:
(1)装置a中可观察到的现象为
(2)装置b中产生的现象为
(3)装置c的作用是
(4)SO2形成酸雨的另一途径为SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4,则在此过程中的飘尘是作为
更新时间:2021/05/07 15:01:40
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
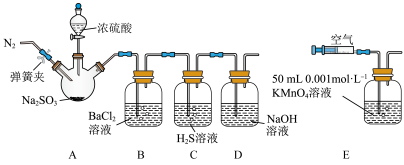
【推荐1】某研究性学习小组利用下列有关装置,对二氧化硫的性质及空气中二氧化硫的含量进行探究(装置的气密性已检查): 中反应的化学方程式是
中反应的化学方程式是___________ 。
(2)滴加浓硫酸之前,打开弹簧夹,通入一段时间 ,再关闭弹簧夹,此操作的目的是:
,再关闭弹簧夹,此操作的目的是:___________ 。
(3)实验过程中装置 中没有明显变化。实验结束后取下装置
中没有明显变化。实验结束后取下装置 ,从中取少量溶液于洁净试管中,向试管中滴加适量氨水出现白色沉淀
,从中取少量溶液于洁净试管中,向试管中滴加适量氨水出现白色沉淀___________ (填化学式)。
(4)装置 中的溶液中出现
中的溶液中出现___________ 浑浊,该实验证明二氧化硫具有___________ 性。
(5)装置 的作用是
的作用是___________ 。
 中反应的化学方程式是
中反应的化学方程式是(2)滴加浓硫酸之前,打开弹簧夹,通入一段时间
 ,再关闭弹簧夹,此操作的目的是:
,再关闭弹簧夹,此操作的目的是:(3)实验过程中装置
 中没有明显变化。实验结束后取下装置
中没有明显变化。实验结束后取下装置 ,从中取少量溶液于洁净试管中,向试管中滴加适量氨水出现白色沉淀
,从中取少量溶液于洁净试管中,向试管中滴加适量氨水出现白色沉淀(4)装置
 中的溶液中出现
中的溶液中出现(5)装置
 的作用是
的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室里研究不同价态硫元素之间的转化

(1)A中发生反应的化学方程式为___________ 。
(2)B中的现象是___________ 。
(3)C中出现淡黄色沉淀,反应中Na2S做___________ (填“氧化剂”或“还原剂”)。
(4)D中溴水褪色,该反应S元素的价态变化是由+4价变为___________ 价。
(5)E的作用是吸收多余的SO2,离子方程式为___________ 。
(6)上述实验D体现SO2的性质是___________ 。

(1)A中发生反应的化学方程式为
(2)B中的现象是
(3)C中出现淡黄色沉淀,反应中Na2S做
(4)D中溴水褪色,该反应S元素的价态变化是由+4价变为
(5)E的作用是吸收多余的SO2,离子方程式为
(6)上述实验D体现SO2的性质是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】六种短周期元素在周期表中的相对位置如下所示,其中E元素原子核外电子总数是其最外层电子数的3倍。关于元素周期表及这六种元素性质,请回答:

(1)这六种元素的氢化物中,最稳定的是__________ .(写化学式);
(2)AC2的电子式为____________ .
(3)在一定条件下,由B单质与H2反应生成1 molG时,放出的热量为46.2 kJ,写出该反应的热化学方程式:____________________ .
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式_________________________ ,该反应中被氧化的G与参与反应的G的质量之比_________ .
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:_________ .

(1)这六种元素的氢化物中,最稳定的是
(2)AC2的电子式为
(3)在一定条件下,由B单质与H2反应生成1 molG时,放出的热量为46.2 kJ,写出该反应的热化学方程式:
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
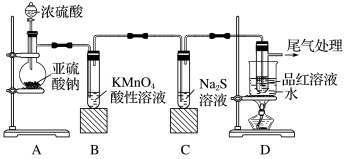
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是_______ ,其中发生反应的化学方程式为_______ 。
(2)实验过程中,装置B、C中发生的现象分别是_______ 、_______ ;这些现象分别说明SO2具有的性质是_______ 和_______ 。
(3)装置D的目的是探究SO2与品红反应的可逆性,请写出实验操作及现象_______ 。
(4)尾气可采用_______ 溶液吸收。有关化学方程式为:_______ 。

请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是
(2)实验过程中,装置B、C中发生的现象分别是
(3)装置D的目的是探究SO2与品红反应的可逆性,请写出实验操作及现象
(4)尾气可采用
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】研究性学习小组的同学们按下图装置进行SO2的制备及性质探究实验。(查阅资料得到SO2气体的制备原理:Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O),回答问题:
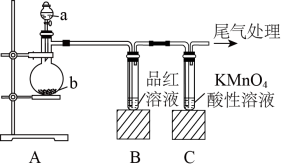
(1)图中a的仪器名称是_______ , 亚硫酸钠应放在_________ (填“a”或“b”)中。
(2)实验过程中,可以观察到装置B中品红溶液_______ (填实验现象),该现象说明SO2具有_____ 性(填“氧化”、“还原”或“漂白”)。
(3)酸性条件下,SO2与KMnO4在发生如下反应:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,使溶液褪色。反应中SO2是________ (填“氧化”、“还原”剂)。
(4)尾气可采用________ 溶液吸收。

(1)图中a的仪器名称是
(2)实验过程中,可以观察到装置B中品红溶液
(3)酸性条件下,SO2与KMnO4在发生如下反应:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,使溶液褪色。反应中SO2是
(4)尾气可采用
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】现欲设计一个实验,验证红热的炭与浓硫酸发生反应所生成的各种产物。有一个同学按气体的流动方向设计了一个实验流程,其所使用的试剂次序可表示为:气体产物→无水硫酸铜→品红溶液→溴水→品红溶液→澄清石灰水
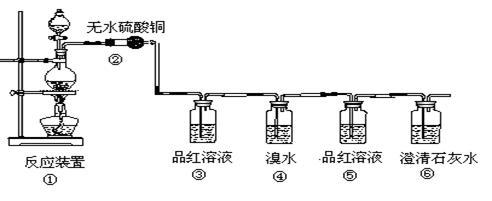
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气______ 。
(2)①中反应的化学方程为______ ;
(3)②处的现象是:______ 。
(4)品红溶液使用了两次,第二次使用时的作用是______ 。
(5)④表现了二氧化硫的______ 性。(“还原”、“漂白”)反应的化学方程式为:______ 。
(6)根据______ 现象,可证明产物中一定有CO2气体。

(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气
(2)①中反应的化学方程为
(3)②处的现象是:
(4)品红溶液使用了两次,第二次使用时的作用是
(5)④表现了二氧化硫的
(6)根据
您最近一年使用:0次



