在2 L的密闭容器中,SO2和足量的O2在催化剂500℃的条件下发生反应。SO2和SO3的物质的量随时间变化的关系曲线如图所示。
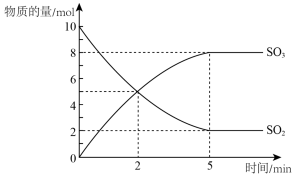
回答下列问题。
(1)该反应的化学方程式是_______ 。
(2)在前5 min内,以SO2的浓度变化表示的速率是_______ mol/(L·min)。
(3)反应达到平衡状态的依据是_______ 。
A.单位时间内消耗1 mol SO2,同时生成1 mol SO3
B.SO2的浓度与SO3浓度相等
C.SO2的浓度与SO3浓度均不再变化

回答下列问题。
(1)该反应的化学方程式是
(2)在前5 min内,以SO2的浓度变化表示的速率是
(3)反应达到平衡状态的依据是
A.单位时间内消耗1 mol SO2,同时生成1 mol SO3
B.SO2的浓度与SO3浓度相等
C.SO2的浓度与SO3浓度均不再变化
更新时间:2021/05/12 21:14:53
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.氢能对环境无污染,请根据下列信息:
键能:指1 mol断裂AB化学键形成原子A和B所需要的能量或A和B形成AB化学键所放出的能量。
(1)判断氢气燃烧生成1 mol H2O(g)时可放出的能量为_______ kJ。
(2)据报道,国产液氢技术取得重大突破,液氢储运渗透率或将逐步提升。等质量液氢与氢气分别与氧气完全燃烧时生成液态水释放出的能量前者_______ 后者(填“>”“<”或“=”)。
Ⅱ.在生产和生活中,人们关注化学反应进行的快慢和程度,以提高生产效率和调控反应条件。 是工业制硫酸的主要反应之一。
是工业制硫酸的主要反应之一。
(3)在2 L密闭容器内,500℃时,测得 随时间的变化如下表:
随时间的变化如下表:
①用 表示从0~2 s内该反应的平均速率
表示从0~2 s内该反应的平均速率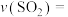
_______ 。
②下图中表示 的变化的曲线是
的变化的曲线是_______ (填字母)。
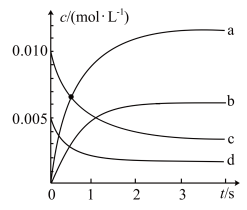
③1 s时,v(正)_______ (填“>”、“<”或“=”)v(逆)。
(4)以下操作可以提高化学反应速率的是_______(填写序号)。
(5)保持密闭容器体积不变,下列能说明该反应已达化学平衡状态的是_______(填写序号)。
| 化学键 | H-H | O=O | H-O |
| 键能/(kJ/mol) | 436 | 498 | 465 |
(1)判断氢气燃烧生成1 mol H2O(g)时可放出的能量为
(2)据报道,国产液氢技术取得重大突破,液氢储运渗透率或将逐步提升。等质量液氢与氢气分别与氧气完全燃烧时生成液态水释放出的能量前者
Ⅱ.在生产和生活中,人们关注化学反应进行的快慢和程度,以提高生产效率和调控反应条件。
 是工业制硫酸的主要反应之一。
是工业制硫酸的主要反应之一。(3)在2 L密闭容器内,500℃时,测得
 随时间的变化如下表:
随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
 (mol) (mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
 表示从0~2 s内该反应的平均速率
表示从0~2 s内该反应的平均速率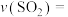
②下图中表示
 的变化的曲线是
的变化的曲线是
③1 s时,v(正)
(4)以下操作可以提高化学反应速率的是_______(填写序号)。
| A.选择更高效催化剂 | B.增大 气体的浓度 气体的浓度 |
| C.恒容下充入Ne | D.适当降低温度 |
A.单位时间内消耗2 mol  的同时消耗1 mol 的同时消耗1 mol  |
| B.容器中气体密度保持不变 |
| C.容器中气体的平均摩尔质量保持不变 |
D. |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】将4mol A气体和2mol B气体在2L容器中混合并在一定条件下发生如下反应:2A(g)+B(g)=2C(g),若经2s后测得C的浓度为0.6 mol∙L−1,请回答下列问题:
(1)用物质C表示的反应的平均速率为_______
(2)用物质B表示的反应的平均速率为_______
(3)2s时物质A的转化率为_______
(4)2s时物质B的浓度为_______
(1)用物质C表示的反应的平均速率为
(2)用物质B表示的反应的平均速率为
(3)2s时物质A的转化率为
(4)2s时物质B的浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=________________ 。已知 >
>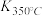 ,则该反应是
,则该反应是_____ 热反应。
(2)用NO表示从0~2 s内该反应的平均速率v=______________ 。
(3)能说明该反应已达到平衡状态的是 。
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的措施是__________ 。
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=
 >
>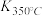 ,则该反应是
,则该反应是(2)用NO表示从0~2 s内该反应的平均速率v=
(3)能说明该反应已达到平衡状态的是 。
| A.v(NO2)=2v(O2) | B.容器内压强保持不变 |
| C.v逆(NO)=2v正(O2) | D.容器内密度保持不变 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】在 的恒容密闭容器中充入
的恒容密闭容器中充入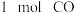 和
和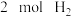 ,一定条件下发生反应:
,一定条件下发生反应: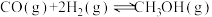 ,测得
,测得 和
和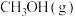 的物质的量变化如图
的物质的量变化如图 所示,反应过程中的能量变化如图
所示,反应过程中的能量变化如图 所示。
所示。 表示的反应的平均反应速率
表示的反应的平均反应速率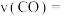
___________ 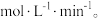
(2)下列描述中能说明上述反应达到平衡状态的是___________ 。
A. 、
、 和
和 三种物质的浓度相等
三种物质的浓度相等
B. 、
、 和
和 三种物质的浓度不再改变
三种物质的浓度不再改变
C. 、
、 和
和 三种物质的浓度之比等于1∶2∶1
三种物质的浓度之比等于1∶2∶1
D. 、
、 和
和 三种物质的速率之比等于1∶2∶1
三种物质的速率之比等于1∶2∶1
E.单位时间内消耗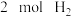 的同时生成
的同时生成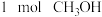
(3)平衡时 的体积分数为
的体积分数为___________  保留
保留 位有效数字
位有效数字 。
。
(4)该反应是___________ 反应 填“吸热”或“放热”
填“吸热”或“放热” ,已知断开
,已知断开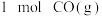 和
和 中的化学键需要吸收的能量为
中的化学键需要吸收的能量为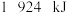 ,则断开
,则断开 中的化学键所需要吸收
中的化学键所需要吸收___________ 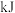 的能量。
的能量。
(5)一定条件下,在密闭容器中充入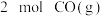 与
与 ,二者充分反应后生成
,二者充分反应后生成 的物质的量
的物质的量___________  填“
填“ ”“
”“ ”或“
”或“ ”
” 。
。
 的恒容密闭容器中充入
的恒容密闭容器中充入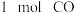 和
和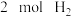 ,一定条件下发生反应:
,一定条件下发生反应: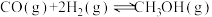 ,测得
,测得 和
和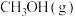 的物质的量变化如图
的物质的量变化如图 所示,反应过程中的能量变化如图
所示,反应过程中的能量变化如图 所示。
所示。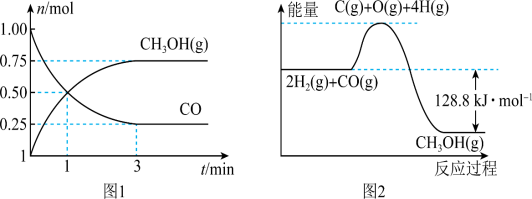
 表示的反应的平均反应速率
表示的反应的平均反应速率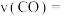
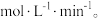
(2)下列描述中能说明上述反应达到平衡状态的是
A.
 、
、 和
和 三种物质的浓度相等
三种物质的浓度相等B.
 、
、 和
和 三种物质的浓度不再改变
三种物质的浓度不再改变C.
 、
、 和
和 三种物质的浓度之比等于1∶2∶1
三种物质的浓度之比等于1∶2∶1D.
 、
、 和
和 三种物质的速率之比等于1∶2∶1
三种物质的速率之比等于1∶2∶1E.单位时间内消耗
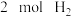 的同时生成
的同时生成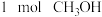
(3)平衡时
 的体积分数为
的体积分数为 保留
保留 位有效数字
位有效数字 。
。(4)该反应是
 填“吸热”或“放热”
填“吸热”或“放热” ,已知断开
,已知断开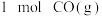 和
和 中的化学键需要吸收的能量为
中的化学键需要吸收的能量为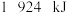 ,则断开
,则断开 中的化学键所需要吸收
中的化学键所需要吸收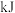 的能量。
的能量。(5)一定条件下,在密闭容器中充入
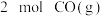 与
与 ,二者充分反应后生成
,二者充分反应后生成 的物质的量
的物质的量 填“
填“ ”“
”“ ”或“
”或“ ”
” 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】根据化学反应速率和化学反应限度的知识回答下列问题:
Ⅰ.某温度时,在2 L容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示:_______ 。
(2)反应开始至4 min时,A的平均反应速率为_______ 。
(3)4 min时,反应是否达平衡状态?_______ (填“是”或“否”),8 min时,v正_______ (填“>”“<”或“=”)v逆。
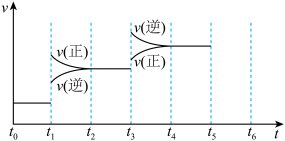
Ⅱ.氢气是合成氨的重要原料,合成氨反应的化学方程式为N2(g)+3H2(g)⇌2NH3(g),该反应为放热反应,且每生成2 mol NH3,放出92.4 kJ的热量。当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。图中表示反应处于化学平衡状态的时间段(t1时刻后)为_______ 。
①N2的转化率为_______ 。
②反应达到平衡时,放出的热量_______ (填字母,下同)。
A.小于92.4 kJ
B.等于92.4 kJ
C.大于92.4 kJ
D.可能大于、小于或等于92.4 kJ
(3)若该反应在绝热条件下进行,下列能证明反应已达化学平衡的为_______ 。
A.压强不变
B.体系的温度不变
C.N2、H2、NH3的分子数之比为1:3:2
D.混合气体的质量不变
Ⅰ.某温度时,在2 L容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示:
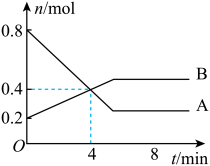
(2)反应开始至4 min时,A的平均反应速率为
(3)4 min时,反应是否达平衡状态?
Ⅱ.氢气是合成氨的重要原料,合成氨反应的化学方程式为N2(g)+3H2(g)⇌2NH3(g),该反应为放热反应,且每生成2 mol NH3,放出92.4 kJ的热量。当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。图中表示反应处于化学平衡状态的时间段(t1时刻后)为
①N2的转化率为
②反应达到平衡时,放出的热量
A.小于92.4 kJ
B.等于92.4 kJ
C.大于92.4 kJ
D.可能大于、小于或等于92.4 kJ
(3)若该反应在绝热条件下进行,下列能证明反应已达化学平衡的为
A.压强不变
B.体系的温度不变
C.N2、H2、NH3的分子数之比为1:3:2
D.混合气体的质量不变
您最近一年使用:0次
【推荐3】甲醇是一种重要的化工原料又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
①A、B两点对应的压强大小关系是PA_______ PB(填“>、<、=”)。
②在压强为P2时B、C两点的正反应速率大小关系是______________
③下列叙述能说明上述反应已达到化学平衡状态的是__________
A.H2的消耗速率是CH3OH生成速率的2倍 B.CH3OH的体积分数不再改变
C.混合气体的密度不再改变 D.CO和CH3OH的物质的量之比保持不变
(2)在压强为P1、温度为T1℃时,H2的平衡转化率为__________ (计算出结果),再加入1.0 mol CO后重新到达平衡,则CO的转化率___________ (填“增大”、“不变”或“减小”)。
(3) 在压强为P1、温度为T1℃时,1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.05 mol、H2:0.1mol、CH3OH:0.05mol。此时v(正)________ v(逆)(填“>”、“<”或“=”)。
(1)在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。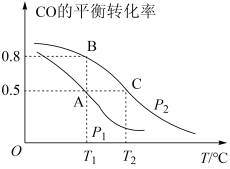
①A、B两点对应的压强大小关系是PA
②在压强为P2时B、C两点的正反应速率大小关系是
③下列叙述能说明上述反应已达到化学平衡状态的是
A.H2的消耗速率是CH3OH生成速率的2倍 B.CH3OH的体积分数不再改变
C.混合气体的密度不再改变 D.CO和CH3OH的物质的量之比保持不变
(2)在压强为P1、温度为T1℃时,H2的平衡转化率为
(3) 在压强为P1、温度为T1℃时,1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.05 mol、H2:0.1mol、CH3OH:0.05mol。此时v(正)
您最近一年使用:0次



