将4mol A气体和2mol B气体在2L容器中混合并在一定条件下发生如下反应:2A(g)+B(g)=2C(g),若经2s后测得C的浓度为0.6 mol∙L−1,请回答下列问题:
(1)用物质C表示的反应的平均速率为_______
(2)用物质B表示的反应的平均速率为_______
(3)2s时物质A的转化率为_______
(4)2s时物质B的浓度为_______
(1)用物质C表示的反应的平均速率为
(2)用物质B表示的反应的平均速率为
(3)2s时物质A的转化率为
(4)2s时物质B的浓度为
更新时间:2022-12-06 09:25:37
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】氢气是理想的能源,可由天然气和水反应制备,其主要反应为 ,反应过程中能量变化如图1所示:
,反应过程中能量变化如图1所示:
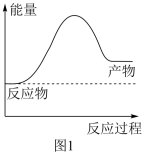
(1)该反应是___________ (填“吸热”或“放热”)反应。
(2)某温度下,在 恒容密闭容器中充入
恒容密闭容器中充入 和
和 制备氢气,反应中
制备氢气,反应中 的物质的量变化如图2所示。
的物质的量变化如图2所示。
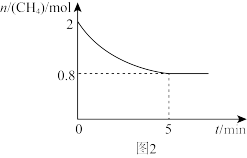
① 前,该反应的正反应速率
前,该反应的正反应速率___________ (填“大于”、“小于”或“等于”)逆反应速率,逆反应速率不断___________ (填“增大”或“减小”)。
②下列能说明该反应已达到化学平衡状态的是___________ (填字母)。
a.容器内混合气体的密度不再发生变化
b.容器内气体原子总数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.单位时间内, 键断裂的同时有
键断裂的同时有 键断裂
键断裂
③ 内,以
内,以 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为___________  ,
, 时,混合气体中
时,混合气体中 的体积分数为
的体积分数为___________  (精确到
(精确到 )。
)。
④若要加快化学反应速率,可采用的方法是___________ (填“升高”或“降低”)温度。
 ,反应过程中能量变化如图1所示:
,反应过程中能量变化如图1所示:
(1)该反应是
(2)某温度下,在
 恒容密闭容器中充入
恒容密闭容器中充入 和
和 制备氢气,反应中
制备氢气,反应中 的物质的量变化如图2所示。
的物质的量变化如图2所示。
①
 前,该反应的正反应速率
前,该反应的正反应速率②下列能说明该反应已达到化学平衡状态的是
a.容器内混合气体的密度不再发生变化
b.容器内气体原子总数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.单位时间内,
 键断裂的同时有
键断裂的同时有 键断裂
键断裂③
 内,以
内,以 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为 ,
, 时,混合气体中
时,混合气体中 的体积分数为
的体积分数为 (精确到
(精确到 )。
)。④若要加快化学反应速率,可采用的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】为了研究在MnO2存在下H2O2的分解速率,某学生将少许MnO2粉末加入50mL密度为1.1g•cm-3的过氧化氢溶液中,通过实验测定,在标准状况下放出气体的体积和时间的关系如图所示。请据图回答下列问题:
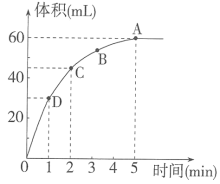
(1)放出一半气体所需要的时间为_____ 。
(2)A、B、C、D各点反应速率大小的顺序是_____ 。
(3)过氧化氢溶液的初始物质的量浓度为____ 。

(1)放出一半气体所需要的时间为
(2)A、B、C、D各点反应速率大小的顺序是
(3)过氧化氢溶液的初始物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】用纯净的锌粒与100mL2mol/L稀盐酸反应制取氢气,请回答:
(1)实验过程如图所示,图中______ 段化学反应速率最快。若经过10分钟的反应时间共消耗锌0.65克(忽略溶液体积的变化),则用盐酸表示的反应速率______ 。
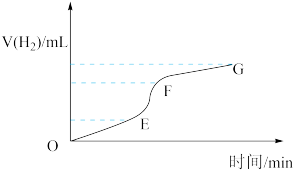
(2)为了加快上述反应的速率,欲向溶液中加入少量下列物质,你认为可行的是_____ 。
A.蒸馏水 B.氯化铜固体
C.氯化钠溶液 D.浓盐酸
(1)实验过程如图所示,图中

(2)为了加快上述反应的速率,欲向溶液中加入少量下列物质,你认为可行的是
A.蒸馏水 B.氯化铜固体
C.氯化钠溶液 D.浓盐酸
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
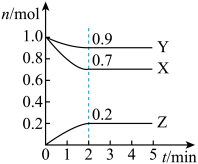
(1)该反应的化学方程式为______ 。
(2)反应开始至2min,以气体Z表示的平均反应速率为______ 。平衡时X的转化率为______ 。
(3) 2min反应达到平衡,容器内混合气体的平均相对分子质量比起始时______  填“大”、“小”或“相等”,下同
填“大”、“小”或“相等”,下同 ,混合气体密度比起始时
,混合气体密度比起始时______ 。
(4)下列叙述能证明该反应已经达到化学平衡状态的是 填序号
填序号
______ 。
A.Y的体积分数不再变化 B.容器内气体压强不再变化
C.υ(X) :υ(Y) = 3:1 D.单位时间内消耗3n mol X同时生成2n mol Z

(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3) 2min反应达到平衡,容器内混合气体的平均相对分子质量比起始时
 填“大”、“小”或“相等”,下同
填“大”、“小”或“相等”,下同 ,混合气体密度比起始时
,混合气体密度比起始时(4)下列叙述能证明该反应已经达到化学平衡状态的是
 填序号
填序号
A.Y的体积分数不再变化 B.容器内气体压强不再变化
C.υ(X) :υ(Y) = 3:1 D.单位时间内消耗3n mol X同时生成2n mol Z
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题
(1)甲烷可以和氯气在光照条件下发生反应,反应类型为:_____ ,产物之一CCl4的空间构型为:________ 。
(2)比较锌粒与不同浓度硫酸反应时的速率,可通过如下装置,测定收集等体积H2需要的时间来实现。该实验装置在加入试剂前需进行__________ ,该装置中仪器a的名称:__________ 。
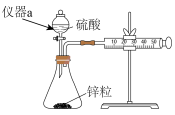
(3)在酸性KMnO4与H2C2O4(草酸,一种弱酸)反应时,可通过测定褪色时间来确定反应速率,请写出该反应的离子方程式:_________________ 。
(4)在地壳内SiO2和HF存在以下平衡: SiO2(s) +4HF(g) SiF4(g)+ 2H2O(g) ,若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
SiF4(g)+ 2H2O(g) ,若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为_________ mol·Lˉ1·minˉ1。
(1)甲烷可以和氯气在光照条件下发生反应,反应类型为:
(2)比较锌粒与不同浓度硫酸反应时的速率,可通过如下装置,测定收集等体积H2需要的时间来实现。该实验装置在加入试剂前需进行

(3)在酸性KMnO4与H2C2O4(草酸,一种弱酸)反应时,可通过测定褪色时间来确定反应速率,请写出该反应的离子方程式:
(4)在地壳内SiO2和HF存在以下平衡: SiO2(s) +4HF(g)
 SiF4(g)+ 2H2O(g) ,若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
SiF4(g)+ 2H2O(g) ,若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题。
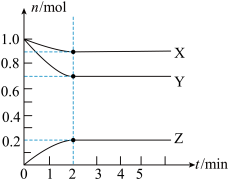
(1)反应开始至2min,Y的平均反应速率____________________ .
(2)分析有关数据,写出X、Y、Z的反应方程式____________________ .
(3)写出提高Y的转化率的两个措施____________________ ,____________________ 。

(1)反应开始至2min,Y的平均反应速率
(2)分析有关数据,写出X、Y、Z的反应方程式
(3)写出提高Y的转化率的两个措施
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/L。反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L。则2min内反应的平均速率v(A)=__________ ,v(B)=_____________ ,v(C)=___________ ;该反应的化学反应方程式为___________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】t℃时,将2mol气体A和1mol气体B充入容积为2L的恒容密闭容器中,发生如下反应:2A(g)+B(g) xC(g),2min时化学反应达到平衡(温度仍为t℃),此时B还有 0.6mol,并测得C的浓度为0.6mol/L。请回答下列问题:
xC(g),2min时化学反应达到平衡(温度仍为t℃),此时B还有 0.6mol,并测得C的浓度为0.6mol/L。请回答下列问题:
(1)判断该反应达到平衡的标志是______ 。
a.容器中的压强保持不变 b.A的生成速率与B的消耗速率之比为2:1
c.容器内混合气体的密度保持不变 d.A的百分含量保持不变
e.B和C的物质的量浓度之比为1:x
(2)x=___ , 从反应开始到达到平衡时,用B表示该反应的平均反应速率v(B)=____ ;
(3)化学反应达到平衡时,A的转化率为_____ 。
(4)某化学兴趣小组同学为了研究上述反应的反应速率,他们将A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的曲线。
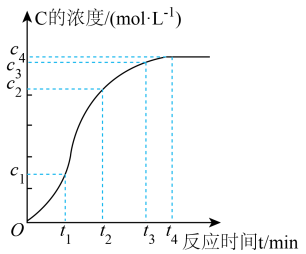
在O~t1、t1~t2、t2~t3各相同的时间段里,反应速率最大的时间段是____ ,从反应速率的变化可看出该反应可能是____ (填“放热”或“吸热”)反应。
 xC(g),2min时化学反应达到平衡(温度仍为t℃),此时B还有 0.6mol,并测得C的浓度为0.6mol/L。请回答下列问题:
xC(g),2min时化学反应达到平衡(温度仍为t℃),此时B还有 0.6mol,并测得C的浓度为0.6mol/L。请回答下列问题:(1)判断该反应达到平衡的标志是
a.容器中的压强保持不变 b.A的生成速率与B的消耗速率之比为2:1
c.容器内混合气体的密度保持不变 d.A的百分含量保持不变
e.B和C的物质的量浓度之比为1:x
(2)x=
(3)化学反应达到平衡时,A的转化率为
(4)某化学兴趣小组同学为了研究上述反应的反应速率,他们将A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的曲线。

在O~t1、t1~t2、t2~t3各相同的时间段里,反应速率最大的时间段是
您最近一年使用:0次
填空题
|
较易
(0.85)
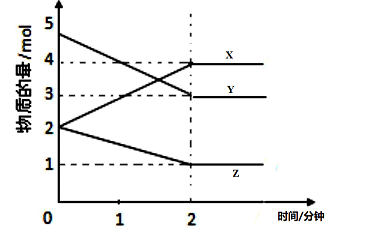
【推荐3】某可逆反应(X、Y、Z均为气体)从0—2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示。则该反应的的反应物是___________ ,生成物是___________ ,化学方程式为___________ ;反应开始至2分钟时,能否用Z表示该反应的反应速率?___________ (填“能”或“不能”)若能,其反应速率为多少,若不能,则其原因为___________ ;2分钟后X、Y、Z各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了___________ 状态。

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
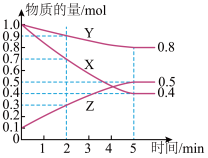
(1)反应的化学方程式是___________ 。
(2)2min内Y的转化率为___________ 。

(1)反应的化学方程式是
(2)2min内Y的转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定温度下,在2 L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
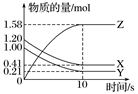
(1)从反应开始到10 s时,用Z表示的反应速率为________________________ ,X的物质的量浓度减少了_________________ ,Y的转化率为__________ 。
(2)该反应的化学方程式为________________________________________ 。

(1)从反应开始到10 s时,用Z表示的反应速率为
(2)该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】丙烷脱氢是工业生产丙烯的重要途径,其热化学方程式为:C3H8(g)  C3H6(g)+H2(g)。请回答下列相关问题。
C3H6(g)+H2(g)。请回答下列相关问题。
(1)一定温度下,向2 L的密闭容器中充入2 mol C3H8发生脱氢反应,经过10min达到平衡状态,测得平衡时气体压强是开始的1.4倍。
①0~10 min内氢气的生成速率υ(H2)=_________ ,C3H8的平衡转化率为_________ 。
②下列情况能说明该反应达到平衡状态的是___________ 。
A.混合气体的平均分子量保持不变
B.C3H6与H2的物质的量之比保持不变
C.混合气体的密度保持不变
D.C3H8的分解速率与C3H6的消耗速率相等
(2)脱氢反应分别在压强为p1和p2时发生,丙烷及丙烯的平衡物质的量分数随温度变化如图所示。
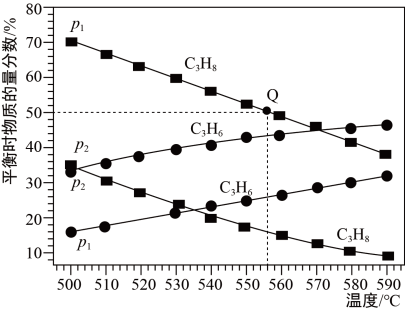
①压强:p1______ p2(填“>”或“<”)。
②为了同时提高反应速率和反应物的平衡转化率,可采取的措施是_________ 。
③若p1=0.1 MPa,起始时充入丙烷发生反应,则Q点对应温度下,反应的平衡常数Kp=________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
④在恒温、恒压的密闭容器中充入丙烷和氩气发生脱氢反应,起始n(氩气)/n(丙烷)越大,丙烷的平衡转化率越大,其原因是_________ 。
 C3H6(g)+H2(g)。请回答下列相关问题。
C3H6(g)+H2(g)。请回答下列相关问题。(1)一定温度下,向2 L的密闭容器中充入2 mol C3H8发生脱氢反应,经过10min达到平衡状态,测得平衡时气体压强是开始的1.4倍。
①0~10 min内氢气的生成速率υ(H2)=
②下列情况能说明该反应达到平衡状态的是
A.混合气体的平均分子量保持不变
B.C3H6与H2的物质的量之比保持不变
C.混合气体的密度保持不变
D.C3H8的分解速率与C3H6的消耗速率相等
(2)脱氢反应分别在压强为p1和p2时发生,丙烷及丙烯的平衡物质的量分数随温度变化如图所示。

①压强:p1
②为了同时提高反应速率和反应物的平衡转化率,可采取的措施是
③若p1=0.1 MPa,起始时充入丙烷发生反应,则Q点对应温度下,反应的平衡常数Kp=
④在恒温、恒压的密闭容器中充入丙烷和氩气发生脱氢反应,起始n(氩气)/n(丙烷)越大,丙烷的平衡转化率越大,其原因是
您最近一年使用:0次



