用纯净的锌粒与100mL2mol/L稀盐酸反应制取氢气,请回答:
(1)实验过程如图所示,图中______ 段化学反应速率最快。若经过10分钟的反应时间共消耗锌0.65克(忽略溶液体积的变化),则用盐酸表示的反应速率______ 。
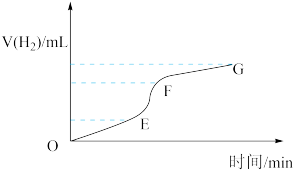
(2)为了加快上述反应的速率,欲向溶液中加入少量下列物质,你认为可行的是_____ 。
A.蒸馏水 B.氯化铜固体
C.氯化钠溶液 D.浓盐酸
(1)实验过程如图所示,图中

(2)为了加快上述反应的速率,欲向溶液中加入少量下列物质,你认为可行的是
A.蒸馏水 B.氯化铜固体
C.氯化钠溶液 D.浓盐酸
更新时间:2020-09-27 19:23:48
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】利用工业废气中的CO2可以制取气态甲醇和水蒸气,一定条件下,往2L恒容密闭容器中充入lmolCO2和3molH2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,测得5min时CO2的转化率随温度变化如图所示:
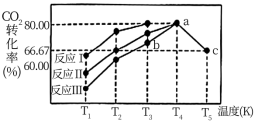
T4温度下,反应Ⅲ的在0~5min内平均反应速率v(H2)=___________ 。

T4温度下,反应Ⅲ的在0~5min内平均反应速率v(H2)=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。

(1)由图中的数据分析,该反应的化学方程式为_____________________ ;
(2)反应开始至5min Z的平均反应速率为______ , X的转化率为________ ;
(3)5min后Z的生成速率比5min末Z的生成速率__________ (大、小、相等)。

(1)由图中的数据分析,该反应的化学方程式为
(2)反应开始至5min Z的平均反应速率为
(3)5min后Z的生成速率比5min末Z的生成速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】CO2的综合利用有利于碳达峰、“碳中和”目标的最终实现。催化CO2和H2能够制取甲醇。在催化剂作用下,CO2、H2同时发生如下反应:
反应1(主反应):CO2(g)+3H2(g)=CH3OH(l)+H2O(g)△H=-86.9kJ·mol-1
反应2(副反应):CO2(g)+H2(g)=CO(g)+H2O(g)△H=+41.2kJ·mol-1
(1)反应2的发生不利于反应1中CH3OH(l)生成的原因是_______ ;一定温度、压强下,为了提高反应速率和CH3OH(1)的选择性,应当_______ 。
(2)假设某温度下,反应1的速率大于反应2的速率,则下列反应过程中的能量变化示意图正确的是_______(填字母)。
反应1(主反应):CO2(g)+3H2(g)=CH3OH(l)+H2O(g)△H=-86.9kJ·mol-1
反应2(副反应):CO2(g)+H2(g)=CO(g)+H2O(g)△H=+41.2kJ·mol-1
(1)反应2的发生不利于反应1中CH3OH(l)生成的原因是
(2)假设某温度下,反应1的速率大于反应2的速率,则下列反应过程中的能量变化示意图正确的是_______(填字母)。
A. | B. | C. | D.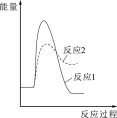 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】t℃时,将2mol气体A和1mol气体B充入容积为2L的恒容密闭容器中,发生如下反应:2A(g)+B(g) xC(g),2min时化学反应达到平衡(温度仍为t℃),此时B还有 0.6mol,并测得C的浓度为0.6mol/L。请回答下列问题:
xC(g),2min时化学反应达到平衡(温度仍为t℃),此时B还有 0.6mol,并测得C的浓度为0.6mol/L。请回答下列问题:
(1)判断该反应达到平衡的标志是______ 。
a.容器中的压强保持不变 b.A的生成速率与B的消耗速率之比为2:1
c.容器内混合气体的密度保持不变 d.A的百分含量保持不变
e.B和C的物质的量浓度之比为1:x
(2)x=___ , 从反应开始到达到平衡时,用B表示该反应的平均反应速率v(B)=____ ;
(3)化学反应达到平衡时,A的转化率为_____ 。
(4)某化学兴趣小组同学为了研究上述反应的反应速率,他们将A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的曲线。
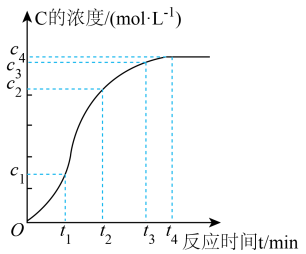
在O~t1、t1~t2、t2~t3各相同的时间段里,反应速率最大的时间段是____ ,从反应速率的变化可看出该反应可能是____ (填“放热”或“吸热”)反应。
 xC(g),2min时化学反应达到平衡(温度仍为t℃),此时B还有 0.6mol,并测得C的浓度为0.6mol/L。请回答下列问题:
xC(g),2min时化学反应达到平衡(温度仍为t℃),此时B还有 0.6mol,并测得C的浓度为0.6mol/L。请回答下列问题:(1)判断该反应达到平衡的标志是
a.容器中的压强保持不变 b.A的生成速率与B的消耗速率之比为2:1
c.容器内混合气体的密度保持不变 d.A的百分含量保持不变
e.B和C的物质的量浓度之比为1:x
(2)x=
(3)化学反应达到平衡时,A的转化率为
(4)某化学兴趣小组同学为了研究上述反应的反应速率,他们将A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的曲线。

在O~t1、t1~t2、t2~t3各相同的时间段里,反应速率最大的时间段是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】图Ⅰ、Ⅱ依次表示在酶浓度一定时,反应速率与反应物浓度、温度的关系。请据图回答下列问题:

(1)图Ⅰ中,反应物达到某一浓度时,反应速率不再上升,其原因是___________ 。
(2)图Ⅱ中,催化效率最高的温度为___________ (填“ ”或“
”或“ ”)点所对应的温度。
”)点所对应的温度。
(3)图Ⅱ中, 点到
点到 点曲线急剧下降,其原因是
点曲线急剧下降,其原因是___________ 。
(4)将装有酶、足量反应物的甲、乙两试管分别放入12℃和75℃的水浴锅内, 后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为___________ (填“甲”或“乙”)。

(1)图Ⅰ中,反应物达到某一浓度时,反应速率不再上升,其原因是
(2)图Ⅱ中,催化效率最高的温度为
 ”或“
”或“ ”)点所对应的温度。
”)点所对应的温度。(3)图Ⅱ中,
 点到
点到 点曲线急剧下降,其原因是
点曲线急剧下降,其原因是(4)将装有酶、足量反应物的甲、乙两试管分别放入12℃和75℃的水浴锅内,
 后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
后取出,转入25℃的水浴锅中保温,试管中反应速率加快的为
您最近一年使用:0次
【推荐1】请阅读下列材料,完成下面小题。
硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸的关键一步是将SO2氧化为SO3,该反应为2SO2+O2 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
1. SO2与O2在一定条件下反应生成SO3,该反应属于( )
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
2. 上述材料中的反应是氧化还原反应,下列有关该反应的说法正确的是( )
A. O2是还原剂 B. SO2被氧化
C. O2失去电子 D. SO2发生还原反应
3. 上述材料中的反应在密闭容器中进行,下列关于该反应的说法正确的是( )
A. 升高温度能减慢反应速率
B. SO2与O2能100%转化为SO3
C. 减小O2的浓度能加快反应速率
D. 使用恰当的催化剂能加快反应速率
4. 上述材料中的反应为放热反应,下列说法正确的是( )
A. 断开化学键放出能量
B. 放热反应都不需要加热
C. 该反应的逆反应是吸热反应
D. 该反应的反应物总能量小于生成物的总能量
硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸的关键一步是将SO2氧化为SO3,该反应为2SO2+O2
 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。1. SO2与O2在一定条件下反应生成SO3,该反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
2. 上述材料中的反应是氧化还原反应,下列有关该反应的说法正确的是
A. O2是还原剂 B. SO2被氧化
C. O2失去电子 D. SO2发生还原反应
3. 上述材料中的反应在密闭容器中进行,下列关于该反应的说法正确的是
A. 升高温度能减慢反应速率
B. SO2与O2能100%转化为SO3
C. 减小O2的浓度能加快反应速率
D. 使用恰当的催化剂能加快反应速率
4. 上述材料中的反应为放热反应,下列说法正确的是
A. 断开化学键放出能量
B. 放热反应都不需要加热
C. 该反应的逆反应是吸热反应
D. 该反应的反应物总能量小于生成物的总能量
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一、某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值) :
①哪一段时间内反应速率最大:___________ min。(填“0~ 1” “1~2”“2~3”“3~4”或“4~ 5”)
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是___________ 。(填字母序号)
A. KCl溶液 B.浓盐酸 C.蒸馏水 D. CuSO4溶液
③该反应还伴随着化学能与热能的转化,是___________ 反应 (填“放热”或“吸热”)
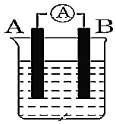
(2)如图为原电池装置示意图。A为Cu, B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2.写出A的电极名称___________ , B 电极反应式:___________ ,该电池在工作时,溶液中Fe3+向___________ (填“A”、“B” )移动,A电极的质量将___________ 。 (填“增加”、“减小”或“不变”)
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一、某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值) :
| 时间 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL (标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是
A. KCl溶液 B.浓盐酸 C.蒸馏水 D. CuSO4溶液
③该反应还伴随着化学能与热能的转化,是
(2)如图为原电池装置示意图。A为Cu, B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2.写出A的电极名称

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】探究化学反应的快慢和限度具有十分重要的意义。某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)要加快上述实验中气体产生的速率,还可采取的措施有_________ (任答两种);
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到 6 个盛有过量 Zn 粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
①请完成此实验设计,其中:V1=______ ,V6= _________ ,V9= __________ ;
②该同学最后得出的结论为:当加入少量 CuSO4 溶液时,生成氢气的速率会大大提高。但当加入的 CuSO4 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因__________________ 。
(1)要加快上述实验中气体产生的速率,还可采取的措施有
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到 6 个盛有过量 Zn 粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol/L H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4 溶液 /mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O /mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=
②该同学最后得出的结论为:当加入少量 CuSO4 溶液时,生成氢气的速率会大大提高。但当加入的 CuSO4 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
您最近一年使用:0次




