某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
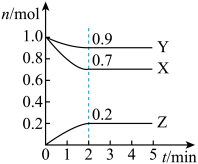
(1)该反应的化学方程式为______ 。
(2)反应开始至2min,以气体Z表示的平均反应速率为______ 。平衡时X的转化率为______ 。
(3) 2min反应达到平衡,容器内混合气体的平均相对分子质量比起始时______  填“大”、“小”或“相等”,下同
填“大”、“小”或“相等”,下同 ,混合气体密度比起始时
,混合气体密度比起始时______ 。
(4)下列叙述能证明该反应已经达到化学平衡状态的是 填序号
填序号
______ 。
A.Y的体积分数不再变化 B.容器内气体压强不再变化
C.υ(X) :υ(Y) = 3:1 D.单位时间内消耗3n mol X同时生成2n mol Z

(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3) 2min反应达到平衡,容器内混合气体的平均相对分子质量比起始时
 填“大”、“小”或“相等”,下同
填“大”、“小”或“相等”,下同 ,混合气体密度比起始时
,混合气体密度比起始时(4)下列叙述能证明该反应已经达到化学平衡状态的是
 填序号
填序号
A.Y的体积分数不再变化 B.容器内气体压强不再变化
C.υ(X) :υ(Y) = 3:1 D.单位时间内消耗3n mol X同时生成2n mol Z
更新时间:2019-11-28 20:15:39
|
相似题推荐
【推荐1】CH4、CH3OH、CO等都是重要的能源,也是重要的化工原料。
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式___________ 。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
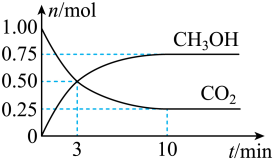
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
②达到平衡时,H2的转化率为___________ 。
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的转化率为
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气器材的消毒,可由乙酸与 在硫酸催化下反应制得,热化学方程式为:
在硫酸催化下反应制得,热化学方程式为: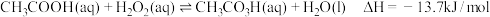
(1)市售过氧乙酸的浓度一般不超过21%,原因是___________ 。
(2)以下措施中能提高乙酸平衡转化率的措施有___________。
(3)取质量相等的冰醋酸和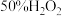 溶液混合均匀,在一定量硫酸催化下进行如下实验。
溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在 下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
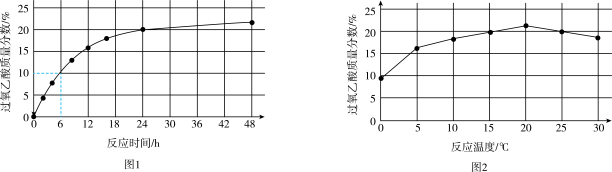
①实验1中,若反应混合液的总质量为 ,依据图1数据计算,在
,依据图1数据计算,在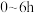 间,
间,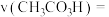
___________ 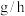 。(用含m的代数式表示)
。(用含m的代数式表示)
②综合图1、图2分析,与 相比,
相比, 时过氧乙酸产率降低的可能原因是
时过氧乙酸产率降低的可能原因是___________ (写出2条)。
(4)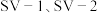 是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同
是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同 下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
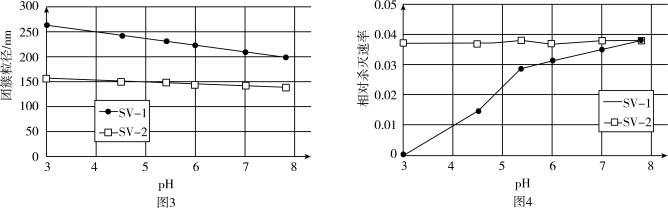
依据图3、图4分析,过氧乙酸对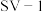 的杀灭速率随
的杀灭速率随 增大而增大的原因可能是
增大而增大的原因可能是___________ 。
 在硫酸催化下反应制得,热化学方程式为:
在硫酸催化下反应制得,热化学方程式为: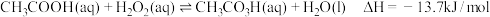
(1)市售过氧乙酸的浓度一般不超过21%,原因是
(2)以下措施中能提高乙酸平衡转化率的措施有___________。
| A.降低温度 | B.增加 用量(溶液体积不变) 用量(溶液体积不变) |
| C.加水稀释溶液 | D.增加乙酸的用量(溶液体积不变) |
(3)取质量相等的冰醋酸和
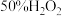 溶液混合均匀,在一定量硫酸催化下进行如下实验。
溶液混合均匀,在一定量硫酸催化下进行如下实验。实验1:在
 下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。

①实验1中,若反应混合液的总质量为
 ,依据图1数据计算,在
,依据图1数据计算,在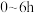 间,
间,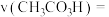
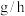 。(用含m的代数式表示)
。(用含m的代数式表示)②综合图1、图2分析,与
 相比,
相比, 时过氧乙酸产率降低的可能原因是
时过氧乙酸产率降低的可能原因是(4)
 是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同
是两种常用于实验研究的病毒,病毒在水中可能会聚集成团簇。不同 下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
依据图3、图4分析,过氧乙酸对
 的杀灭速率随
的杀灭速率随 增大而增大的原因可能是
增大而增大的原因可能是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】为倡导“节能减排”和“低碳经济”,降低大气中CO2含量及有效地开发利用CO2,工业上可用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入1molCO2、3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
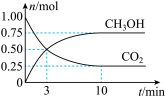
(1)写出该反应的化学平衡常数表达式:K=________ 。
(2)在3min末,反应速率v(正)________ v(逆)(选填>、<或=)。
(3)从反应开始到平衡,平均反应速率v(CO2)=_________ 。达到平衡时,H2的转化率为________ 。
(4)下列措施可以加快反应速率的是________ 。
(5)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为:甲:v(H2)=0.45mol•L-1•s-1;乙:v(CO2)=0.2mol•L-1•s-1;丙:v(CH3OH)=6mol•L-1•min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为________ 。
 CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
(1)写出该反应的化学平衡常数表达式:K=
(2)在3min末,反应速率v(正)
(3)从反应开始到平衡,平均反应速率v(CO2)=
(4)下列措施可以加快反应速率的是
| A.升高温度 | B.加入催化剂 | C.增大压强 | D.及时分离出CH3OH |
(5)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为:甲:v(H2)=0.45mol•L-1•s-1;乙:v(CO2)=0.2mol•L-1•s-1;丙:v(CH3OH)=6mol•L-1•min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某温度时,在2L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:
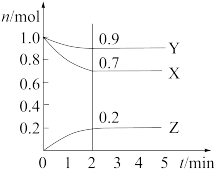
(1)该反应的化学方程式为___________ 。反应进行到2min时,正反应速率和逆反应速率___________ (填“相等”或“不相等”)
(2)反应开始至2min,用Y表示的平均反应速率为___________ ,X的转化率为___________ 。混合气中Y的体积分数为___________ 。
(3)在密闭容器里,通入amolA(g)和bmolB(g),发生反应A(g)+B(g)=2C(g),当改变下列条件时,会加快反应速率的是___________ (填序号)。
①降低温度②保持容器的体积不变,充入氦气
③加入催化剂④保持容器的体积不变,增加A(g)的物质的量

(1)该反应的化学方程式为
(2)反应开始至2min,用Y表示的平均反应速率为
(3)在密闭容器里,通入amolA(g)和bmolB(g),发生反应A(g)+B(g)=2C(g),当改变下列条件时,会加快反应速率的是
①降低温度②保持容器的体积不变,充入氦气
③加入催化剂④保持容器的体积不变,增加A(g)的物质的量
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在0.5L的密闭容器中,一定量的氮气和氢气进行
如下化学反应:N2(g)+3H2(g) 2NH3(g) ⊿H<0,其化学平衡常数K与温度t的关系如右表:
2NH3(g) ⊿H<0,其化学平衡常数K与温度t的关系如右表:
请完成下列问题;
(1)试比较K1、K2的大小,K1 K2(填写“>”、“=”或“<”)
(2)下列各项能作为判断该反应达到化学平衡状态的依据是 (填序号字母)
a.容器内N2、H2、NH3的浓度之比为1∶3∶2 b.υ(N2)正=3υ(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)400℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数的值为 。
N2(g)+3H2(g)的化学平衡常数的值为 。
当测得NH3和N2、H2的物质的量分别为3 mol和2 mol、1 mol时,则该反应的
υ(N2)正 υ(N2)逆 (填写“>”、“=”或“<”)
(4)(3)中反应平衡时,升高温度,NH3转化率 (填“变大”、“变小”、“不变”)
如下化学反应:N2(g)+3H2(g)
 2NH3(g) ⊿H<0,其化学平衡常数K与温度t的关系如右表:
2NH3(g) ⊿H<0,其化学平衡常数K与温度t的关系如右表:| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
请完成下列问题;
(1)试比较K1、K2的大小,K1 K2(填写“>”、“=”或“<”)
(2)下列各项能作为判断该反应达到化学平衡状态的依据是 (填序号字母)
a.容器内N2、H2、NH3的浓度之比为1∶3∶2 b.υ(N2)正=3υ(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)400℃时,反应2NH3(g)
 N2(g)+3H2(g)的化学平衡常数的值为 。
N2(g)+3H2(g)的化学平衡常数的值为 。当测得NH3和N2、H2的物质的量分别为3 mol和2 mol、1 mol时,则该反应的
υ(N2)正 υ(N2)逆 (填写“>”、“=”或“<”)
(4)(3)中反应平衡时,升高温度,NH3转化率 (填“变大”、“变小”、“不变”)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】完成下列填空
(1)工业上常以水煤气(CO和H2)为原料合成甲醇。已知: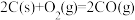
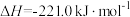 ;
;
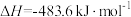 ,则C(s)与H2O(g)制备水煤气的热化学方程式为
,则C(s)与H2O(g)制备水煤气的热化学方程式为_______ 。
(2)一定条件下,在2L密闭容器中充入1 mol CO2和3 mol H2,发生反应:xCO2(g)+3H2(g) CH3OH(g)+H2O(g)。测得CO2(g)和CH3OH(g)的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。测得CO2(g)和CH3OH(g)的物质的量随时间变化如图所示。

①x=_______ ;0~10min内CO2的平均反应速率v(CO2)=_______ mol/(L·min),平衡时H2的转化率为_______ 。
②下列措施能提高正反应速率的是_______ (填正确答案的字母)。
A.降低温度 B.增加CO2的量 C. 使用催化剂 D.及时分离出甲醇
(1)工业上常以水煤气(CO和H2)为原料合成甲醇。已知:
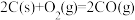
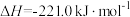 ;
;
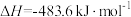 ,则C(s)与H2O(g)制备水煤气的热化学方程式为
,则C(s)与H2O(g)制备水煤气的热化学方程式为(2)一定条件下,在2L密闭容器中充入1 mol CO2和3 mol H2,发生反应:xCO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。测得CO2(g)和CH3OH(g)的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。测得CO2(g)和CH3OH(g)的物质的量随时间变化如图所示。
①x=
②下列措施能提高正反应速率的是
A.降低温度 B.增加CO2的量 C. 使用催化剂 D.及时分离出甲醇
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
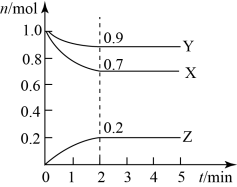
根据图中数据填空:
(1)该反应的化学方程式为___ 。
(2)若X、Y、Z均为气体,2min时反应达到平衡,此时体系内压强与开始时的压强之比为___ 。
(3)若X、Y、Z均为气体,则达平衡时,容器内混合气体的平均相对分子质量比起始投料时___ (填“增大”“减小”或“相等”)。

根据图中数据填空:
(1)该反应的化学方程式为
(2)若X、Y、Z均为气体,2min时反应达到平衡,此时体系内压强与开始时的压强之比为
(3)若X、Y、Z均为气体,则达平衡时,容器内混合气体的平均相对分子质量比起始投料时
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学平衡状态的建立
(1)化学平衡状态的建立过程
在一定条件下向反应容器中加入SO2和O2发生反应:2SO2+O2 2SO3
2SO3
(2)用速率变化图象表示化学平衡状态的建立

(1)化学平衡状态的建立过程
在一定条件下向反应容器中加入SO2和O2发生反应:2SO2+O2
 2SO3
2SO3| 浓度 | 速率变化 | v正、v逆关系 | |
| 开始 | 反应物浓度 | v正 | v正 |
| 生成物浓度 | v逆 | ||
| 变化 | 反应物浓度 | v正 | v正 |
| 生成物浓度 | v逆 | ||
| 平衡 | 反应物浓度 | v正 | v正 |
| 生成物浓度 | v逆 |
(2)用速率变化图象表示化学平衡状态的建立

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某温度时,在2L容器中X、Y、Z三种气体的物质的量(n)随着时间(t)变化的曲线如图所示。由图中数据分析:
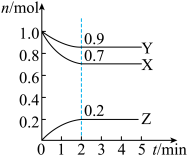
(1)该反应的化学方程式为 ,
(2)反应开始至2min,用Z表示的平均反应速率为____________________
(3)下列叙述中能说明上述反应达到平衡状态的是_______ (双项选)
A.X、Y、Z的物质的量之比为3:1:2
B.混合气体的总质量不随时间的变化而变化
C.单位时间内每消耗3mol X,同时生成2mol Z
D.混合气体的压强不随时间的变化而变化
E.X、Y、Z的浓度不随时间的变化而变化。

(1)该反应的化学方程式为 ,
(2)反应开始至2min,用Z表示的平均反应速率为
(3)下列叙述中能说明上述反应达到平衡状态的是
A.X、Y、Z的物质的量之比为3:1:2
B.混合气体的总质量不随时间的变化而变化
C.单位时间内每消耗3mol X,同时生成2mol Z
D.混合气体的压强不随时间的变化而变化
E.X、Y、Z的浓度不随时间的变化而变化。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
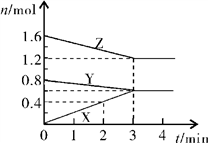
(1)该反应的化学方程式为_______________ 。
(2)反应开始至2min末,X的反应速率为________________ mol·L-1·min-1。

(1)该反应的化学方程式为
(2)反应开始至2min末,X的反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】分在2L密闭容器,800℃时发生如下反应:
2CuO(s)+CO(g) Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
(1)写出该反应的平衡常数表达式______________ 。
已知:K(400℃)>K(350℃),则该反应是___________ 热反应。
(2)右图中表示Cu2O的物质的量随时间变化的曲线是____________ (选填“A”或“B”),800℃时,0~3min内该反应的平均速率v (CO2)=__________ 。
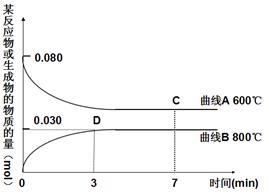
(3) 能说明该反应已达到平衡状态的是__________ 。
a.v(CO)=v(CO2) b.容器内压强保持不变
c.v逆(CO)=v正(CO2) d.容器内气体的密度保持不变
(4)能使该反应的正反应速率增大,且平衡向正反应方向移动的是____________ 。
A.增加CuO的量
B.适当升高温度
C.及时移去CO2
D.增大CO的浓度
E.选择高效催化剂
F.增大压强
2CuO(s)+CO(g)
 Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CuO)(mol) | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
(1)写出该反应的平衡常数表达式
已知:K(400℃)>K(350℃),则该反应是
(2)右图中表示Cu2O的物质的量随时间变化的曲线是

(3) 能说明该反应已达到平衡状态的是
a.v(CO)=v(CO2) b.容器内压强保持不变
c.v逆(CO)=v正(CO2) d.容器内气体的密度保持不变
(4)能使该反应的正反应速率增大,且平衡向正反应方向移动的是
A.增加CuO的量
B.适当升高温度
C.及时移去CO2
D.增大CO的浓度
E.选择高效催化剂
F.增大压强
您最近一年使用:0次

 2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol·L-1,试计算:(写出简单的计算过程)
2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol·L-1,试计算:(写出简单的计算过程)

