为倡导“节能减排”和“低碳经济”,降低大气中CO2含量及有效地开发利用CO2,工业上可用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入1molCO2、3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
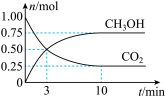
(1)写出该反应的化学平衡常数表达式:K=________ 。
(2)在3min末,反应速率v(正)________ v(逆)(选填>、<或=)。
(3)从反应开始到平衡,平均反应速率v(CO2)=_________ 。达到平衡时,H2的转化率为________ 。
(4)下列措施可以加快反应速率的是________ 。
(5)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为:甲:v(H2)=0.45mol•L-1•s-1;乙:v(CO2)=0.2mol•L-1•s-1;丙:v(CH3OH)=6mol•L-1•min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为________ 。
 CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
(1)写出该反应的化学平衡常数表达式:K=
(2)在3min末,反应速率v(正)
(3)从反应开始到平衡,平均反应速率v(CO2)=
(4)下列措施可以加快反应速率的是
| A.升高温度 | B.加入催化剂 | C.增大压强 | D.及时分离出CH3OH |
(5)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为:甲:v(H2)=0.45mol•L-1•s-1;乙:v(CO2)=0.2mol•L-1•s-1;丙:v(CH3OH)=6mol•L-1•min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
更新时间:2023-10-08 14:07:56
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
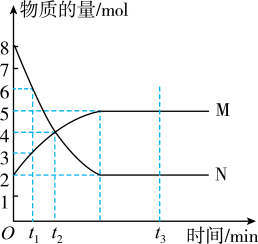
(1)此反应的化学方程式中a/b=___________ ;
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为_________________ ;
(3) N的平衡转化率为_______________ ;
(4)下列叙述中能说明上述反应达到平衡状态的是___________ (填字母)。
a.反应中M与N的物质的量之比为1︰1
b.混合气体的总质量不随时间的变化而变化
c.混合气体的总物质的量不随时间的变化而变化
d.单位时间内每消耗a mol N,同时生成b mol M
e.混合气体的压强不随时间的变化而变化
f.N的质量分数在混合气体中保持不变
Ⅱ.研究性学习小组为探究铁与稀盐酸反应,取同质量、体积的铁片、同浓度的盐酸做了下列平行实验:
实验①:把纯铁片投入到盛有稀盐酸的试管中,发现放出氢气的速率变化如图所示:
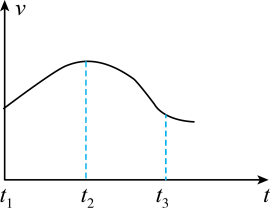
实验②:把铁片投入到含FeCl3的同浓度稀盐酸中,发现放出氢气的量减少。
实验③:在稀盐酸中滴入几滴CuCl2溶液,用铁片做实验,发现生成氢气的速率加快。
试回答下列问题:
(1)分析实验①中t1~t2速率变化的主要原因是_______ ,t2~t3速率变化的主要原因是______ 。
(2)实验②放出氢气的量减少的原因是___________________ (用离子方程式表示)。
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?请选择下列相应的a或b作答。a.若不正确,请说明原因_____________________________________ 。b.若正确,则写出实验③中原电池的正极电极反应式_______________________ 。
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中a/b=
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为
(3) N的平衡转化率为
(4)下列叙述中能说明上述反应达到平衡状态的是
a.反应中M与N的物质的量之比为1︰1
b.混合气体的总质量不随时间的变化而变化
c.混合气体的总物质的量不随时间的变化而变化
d.单位时间内每消耗a mol N,同时生成b mol M
e.混合气体的压强不随时间的变化而变化
f.N的质量分数在混合气体中保持不变
Ⅱ.研究性学习小组为探究铁与稀盐酸反应,取同质量、体积的铁片、同浓度的盐酸做了下列平行实验:
实验①:把纯铁片投入到盛有稀盐酸的试管中,发现放出氢气的速率变化如图所示:

实验②:把铁片投入到含FeCl3的同浓度稀盐酸中,发现放出氢气的量减少。
实验③:在稀盐酸中滴入几滴CuCl2溶液,用铁片做实验,发现生成氢气的速率加快。
试回答下列问题:
(1)分析实验①中t1~t2速率变化的主要原因是
(2)实验②放出氢气的量减少的原因是
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?请选择下列相应的a或b作答。a.若不正确,请说明原因
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】T ℃时,在0.5 L的密闭容器中,反应过程中A、B、C的浓度变化如图所示:

(1)10s内v(B)=_______ 。
(2)该反应的化学方程式为_______ 。

(1)10s内v(B)=
(2)该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】化学在生活、科研中有重要的作用。
(1)将 转化为甲醇是实现碳中和途径之一,原理为:
转化为甲醇是实现碳中和途径之一,原理为: 。在恒温恒容条件下反应
。在恒温恒容条件下反应 ,能说明反应一定达到平衡状态的是_______。
,能说明反应一定达到平衡状态的是_______。
(2)在一定温度下,体积为1L的密闭容器中,充入2mol 和6mol
和6mol ,测得
,测得 和
和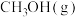 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。

①2min时的
_______  (填写“大于”、“小于”、“等于”);
(填写“大于”、“小于”、“等于”);
②2min~5min的平均反应速率
_______ 。
(3)汽车尾气中含有的NO是造成城市空气污染的主要因素之一,通过NO传感器可监测汽车尾气中NO含量,其工作原理如图所示:

①NiO电极为_______ (填“正极”或“负极”)。
②Pt电极上发生的电极反应式为_______ 。
(4)一种新型催化剂能使NO和CO发生反应 。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
①a=_______ ,b=_______ 。
②能验证温度对化学反应速率影响规律的实验是_______ (填实验编号)。
(1)将
 转化为甲醇是实现碳中和途径之一,原理为:
转化为甲醇是实现碳中和途径之一,原理为: 。在恒温恒容条件下反应
。在恒温恒容条件下反应 ,能说明反应一定达到平衡状态的是_______。
,能说明反应一定达到平衡状态的是_______。| A.氢气的浓度保持不变 |
| B.气体的压强不变 |
| C.体系的密度不变 |
D.生成1mol 同时反应1mol 同时反应1mol |
 和6mol
和6mol ,测得
,测得 和
和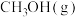 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
①2min时的

 (填写“大于”、“小于”、“等于”);
(填写“大于”、“小于”、“等于”);②2min~5min的平均反应速率

(3)汽车尾气中含有的NO是造成城市空气污染的主要因素之一,通过NO传感器可监测汽车尾气中NO含量,其工作原理如图所示:

①NiO电极为
②Pt电极上发生的电极反应式为
(4)一种新型催化剂能使NO和CO发生反应
 。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。| 实验编号 | T(℃) | NO初始浓度 (  ) ) | CO初始浓度( ) ) | 催化剂的比表面积(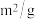 ) ) |
| I | 280 |  |  | 82 |
| II | 280 |  | b | 124 |
| III | 35 | a |  | 82 |
②能验证温度对化学反应速率影响规律的实验是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求填空或计算,(1)(2)小题为判断题。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。___________ (填“×”或“√”)
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。___________ (填“×”或“√”)
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性。
(4)Na与水反应,增大水的用量:反应速率___________ (选填“加快”、“减慢”、“不变”)。
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=___________ mol·L-1·min-1。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出(4)Na与水反应,增大水的用量:反应速率
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大________ min(填“0~1”,“1~2”,“2~3”,“3~4”或“4~5”),原因是______________________________ 。
②求3~4min时间段以盐酸的浓度变化来表示的该反应速率________ (设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是________ (填字母)。
A.蒸馏水 B.KCl溶液
C.KNO3溶液 D.Na2SO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
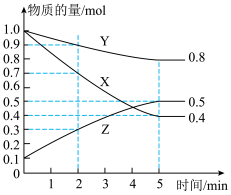
①该反应的化学方程式是_______________ 。
②该反应达到平衡状态的标志是________ (填字母)。
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1molY的同时消耗2molZ
③2min内Y的转化率为________ 。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 100 | 240 | 464 | 576 | 620 |
②求3~4min时间段以盐酸的浓度变化来表示的该反应速率
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是
A.蒸馏水 B.KCl溶液
C.KNO3溶液 D.Na2SO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②该反应达到平衡状态的标志是
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1molY的同时消耗2molZ
③2min内Y的转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】湿法炼锌产生的铜镉渣主要含锌、镉(Cd)、铜、铁、钴(Co)等金属单质。利用铜镉渣可生产Cu、Cd及ZnSO4·7H2O 等,其生产流程如图:
提高铜镉渣的“浸出”速率的措施有___________ (写出1条即可)

| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.9 | 7.0 | 7.2 | 5.4 |
| 沉淀完全的pH | 3.2 | 9.0 | 9.5 | 8.2 |
您最近一年使用:0次
【推荐1】科学家研制出了一种高效催化剂,可以将NO转化为无污染的气体,反应的化学方程式为 。在
。在 下,向
下,向 某恒容密闭容器中充入
某恒容密闭容器中充入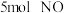 和
和 发生上述反应,起始时压强为
发生上述反应,起始时压强为 ,
,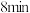 末,反应达到平衡,此时压强
末,反应达到平衡,此时压强 ,回答下列问题:
,回答下列问题:
(1)经测得,每消耗 的同时放出
的同时放出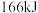 的热量,则
的热量,则
___________  。
。
(2)反应达平衡后:
① 内,
内,
___________  。
。
② 的转化率为
的转化率为___________  ,
,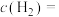
___________  ,
, 的物质的量分数为
的物质的量分数为___________  (保留三位有效数字)。
(保留三位有效数字)。
③该反应的平衡常数
___________ (用含p的代数式表示,以分压表示平衡常数,分压=总压×该气体的物质的量分数,不用化简,列出计算式即可)。
(3)下列说法正确的是___________(填标号)。
 。在
。在 下,向
下,向 某恒容密闭容器中充入
某恒容密闭容器中充入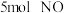 和
和 发生上述反应,起始时压强为
发生上述反应,起始时压强为 ,
,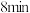 末,反应达到平衡,此时压强
末,反应达到平衡,此时压强 ,回答下列问题:
,回答下列问题:(1)经测得,每消耗
 的同时放出
的同时放出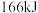 的热量,则
的热量,则
 。
。(2)反应达平衡后:
①
 内,
内,
 。
。②
 的转化率为
的转化率为 ,
,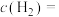
 ,
, 的物质的量分数为
的物质的量分数为 (保留三位有效数字)。
(保留三位有效数字)。③该反应的平衡常数

(3)下列说法正确的是___________(填标号)。
| A.当混合气体的密度不再发生变化时,该反应达到平衡 |
B.无论反应进行到何种程度, 保持不变 保持不变 |
| C.降低温度,反应速率减小,平衡常数增大 |
D.反应达到平衡后,保持其他条件不变,再充入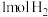 和 和 ,此时 ,此时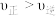 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某温度时,在2 L恒容密闭容器中充入0.9 mol A(g)、0.6 mol B(g)、0.3 mol C(g),发生反应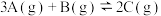 ,各物质物质的量的变化关系如图所示,回答下列问题:
,各物质物质的量的变化关系如图所示,回答下列问题:___________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
(2)0~5 min内,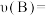
___________ mol∙L−1∙min−1。
(3)反应达到平衡时,
___________ mol∙L−1。
(4)若仅改变下列一个条件,推测该反应的速率发生的变化 (填“增大”、“减小”或“不变”):
①降低温度,化学反应速率___________ ;
②充入少量不参加反应的稀有气体,化学反应速率___________ ;
③将容器的体积压缩至原来的一半,化学反应速率___________ 。
(5) min时,反应
min时,反应___________ (填“达到”或“没有达到”)化学平衡;5 min时,υ(正)___________ (填“>”、“<”或“=”) υ(逆)。
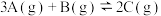 ,各物质物质的量的变化关系如图所示,回答下列问题:
,各物质物质的量的变化关系如图所示,回答下列问题: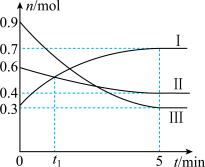
(2)0~5 min内,
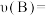
(3)反应达到平衡时,

(4)若仅改变下列一个条件,推测该反应的速率发生的变化 (填“增大”、“减小”或“不变”):
①降低温度,化学反应速率
②充入少量不参加反应的稀有气体,化学反应速率
③将容器的体积压缩至原来的一半,化学反应速率
(5)
 min时,反应
min时,反应
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】升高温度绝大多数的化学反应速率增大,但是2NO(g)+O2(g) 2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g)
2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
i:2NO(g) N2O2(g)(快),v1正=k1正·c2(NO) v1逆=k1逆·c(N2O2) ΔH1<0
N2O2(g)(快),v1正=k1正·c2(NO) v1逆=k1逆·c(N2O2) ΔH1<0
ii:N2O2(g)+O2(g) 2NO2(g)(慢),v2正=k2正·c(N2O2)·c(O2) v2逆=k2逆·c2(NO2) ΔH2<0
2NO2(g)(慢),v2正=k2正·c(N2O2)·c(O2) v2逆=k2逆·c2(NO2) ΔH2<0
一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=______ 。
 2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g)
2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:i:2NO(g)
 N2O2(g)(快),v1正=k1正·c2(NO) v1逆=k1逆·c(N2O2) ΔH1<0
N2O2(g)(快),v1正=k1正·c2(NO) v1逆=k1逆·c(N2O2) ΔH1<0ii:N2O2(g)+O2(g)
 2NO2(g)(慢),v2正=k2正·c(N2O2)·c(O2) v2逆=k2逆·c2(NO2) ΔH2<0
2NO2(g)(慢),v2正=k2正·c(N2O2)·c(O2) v2逆=k2逆·c2(NO2) ΔH2<0一定温度下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在一个容积不变的密闭容器中发生反应CO2(g)+H2(g)  CO(g)+H2O(g)其平衡常数K和温度的关系如下表所示:
CO(g)+H2O(g)其平衡常数K和温度的关系如下表所示:
请填写下列空白。
(1)该反应的平衡常数表达式K=___________ ,该反应为___________ 反应(填“吸热”或“放热”)
(2)在830℃时,向容器中充入1molCO、5molH2O,保持温度不变,反应达到平衡后,其平衡常数___________ 1.0(填“大于”或“等于”或“小于”)
(3)在1200℃时,在某时刻反应混合物中CO2、H2、CO、H2O浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时平衡移动方向为___________ (填“正反应方向”或“逆反应方向”或“不移动”)
 CO(g)+H2O(g)其平衡常数K和温度的关系如下表所示:
CO(g)+H2O(g)其平衡常数K和温度的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的平衡常数表达式K=
(2)在830℃时,向容器中充入1molCO、5molH2O,保持温度不变,反应达到平衡后,其平衡常数
(3)在1200℃时,在某时刻反应混合物中CO2、H2、CO、H2O浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时平衡移动方向为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】羧基硫(COS)是一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在容积不变的密闭容器中,将CO和 混合加热并达到下列平衡:
混合加热并达到下列平衡: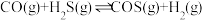
(1)若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1,下列说法正确的是___________ (填字母)。
a.升高温度, 的浓度增大,表明该反应是吸热反应
的浓度增大,表明该反应是吸热反应
b.通入CO后,正反应速率逐渐增大
c.反应前 的物质的量为7mol
的物质的量为7mol
d.达到平衡时CO的转化率为80%
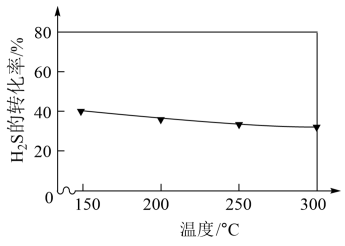
(2)在不同温度下达到化学平衡时, 的转化率如图所示,则该反应是
的转化率如图所示,则该反应是___________ 反应(填“吸热”或“放热”)。
(3)在某温度下,向1L的密闭容器中通入10molCO和10mol ,平衡时测得CO的转化率为40%,则该温度下反应的平衡常数为
,平衡时测得CO的转化率为40%,则该温度下反应的平衡常数为___________ 。
 混合加热并达到下列平衡:
混合加热并达到下列平衡: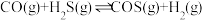
(1)若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1,下列说法正确的是
a.升高温度,
 的浓度增大,表明该反应是吸热反应
的浓度增大,表明该反应是吸热反应b.通入CO后,正反应速率逐渐增大
c.反应前
 的物质的量为7mol
的物质的量为7mold.达到平衡时CO的转化率为80%
(2)在不同温度下达到化学平衡时,
 的转化率如图所示,则该反应是
的转化率如图所示,则该反应是
(3)在某温度下,向1L的密闭容器中通入10molCO和10mol
 ,平衡时测得CO的转化率为40%,则该温度下反应的平衡常数为
,平衡时测得CO的转化率为40%,则该温度下反应的平衡常数为
您最近一年使用:0次



