某温度时,在2 L恒容密闭容器中充入0.9 mol A(g)、0.6 mol B(g)、0.3 mol C(g),发生反应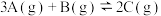 ,各物质物质的量的变化关系如图所示,回答下列问题:
,各物质物质的量的变化关系如图所示,回答下列问题:___________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
(2)0~5 min内,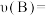
___________ mol∙L−1∙min−1。
(3)反应达到平衡时,
___________ mol∙L−1。
(4)若仅改变下列一个条件,推测该反应的速率发生的变化 (填“增大”、“减小”或“不变”):
①降低温度,化学反应速率___________ ;
②充入少量不参加反应的稀有气体,化学反应速率___________ ;
③将容器的体积压缩至原来的一半,化学反应速率___________ 。
(5) min时,反应
min时,反应___________ (填“达到”或“没有达到”)化学平衡;5 min时,υ(正)___________ (填“>”、“<”或“=”) υ(逆)。
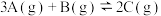 ,各物质物质的量的变化关系如图所示,回答下列问题:
,各物质物质的量的变化关系如图所示,回答下列问题: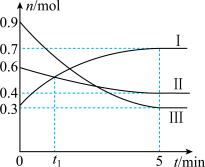
(2)0~5 min内,
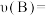
(3)反应达到平衡时,

(4)若仅改变下列一个条件,推测该反应的速率发生的变化 (填“增大”、“减小”或“不变”):
①降低温度,化学反应速率
②充入少量不参加反应的稀有气体,化学反应速率
③将容器的体积压缩至原来的一半,化学反应速率
(5)
 min时,反应
min时,反应
更新时间:2023-04-18 21:57:09
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】一定条件下,将amolA与15molB的混合气体通入一固定体积为5L的密闭容器中,发生如下反应:A(g)+3B(g) 2C(g)
2C(g)
(1)若反应进行到10min时达到平衡,n1(A)=13mol,n1(C)=6mol,;计算a的值___ ;这段时间内的C平均反应速率为___ 。
(2)反应达平衡时,B的转化率为分别为___ ;A的体积分数为___ 。
(3)下列操作能使该反应的反应速率增大的是___ 。
A.向密闭容器中通入氦气增大压强
B.增大A的浓度
C.适当升高温度
D.将容器的体积扩大至10L
(4)反应过程中容器内气体的密度是___ (填“增大”、“减小”或“不变”,下同),平均相对分子质量是___ 。
 2C(g)
2C(g)(1)若反应进行到10min时达到平衡,n1(A)=13mol,n1(C)=6mol,;计算a的值
(2)反应达平衡时,B的转化率为分别为
(3)下列操作能使该反应的反应速率增大的是
A.向密闭容器中通入氦气增大压强
B.增大A的浓度
C.适当升高温度
D.将容器的体积扩大至10L
(4)反应过程中容器内气体的密度是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在恒温恒压下,向体积为2 L密闭容器中充入4mol SO2和2mol O2,生如下反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0。2min后,反应达到平衡,生成SO3为2mol。则0~2 min内v(SO3)__________________ ,平衡后容器中SO2的浓度________________ ,SO2的转化率为___________________ ,在此温度下该反应的平衡常数____________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某温度下,在2L密闭容器中充入4molA气体和3molB气体,发生下列反应:2A(g)+B(g) C(g)+xD(g),5s达到平衡。达到平衡时,生成了1molC,测定D的浓度为1mol/L。
C(g)+xD(g),5s达到平衡。达到平衡时,生成了1molC,测定D的浓度为1mol/L。
(1)求x=__ 。
(2)下列叙述能说明上述反应达到平衡状态的是__ 。
A.单位时间内每消耗2molA,同时生成1molC
B.单位时间内每生成1molB,同时生成1molC
C.D的体积分数不再变化
D.混合气体的压强不再变化
E.B、C的浓度之比为1∶1
 C(g)+xD(g),5s达到平衡。达到平衡时,生成了1molC,测定D的浓度为1mol/L。
C(g)+xD(g),5s达到平衡。达到平衡时,生成了1molC,测定D的浓度为1mol/L。(1)求x=
(2)下列叙述能说明上述反应达到平衡状态的是
A.单位时间内每消耗2molA,同时生成1molC
B.单位时间内每生成1molB,同时生成1molC
C.D的体积分数不再变化
D.混合气体的压强不再变化
E.B、C的浓度之比为1∶1
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】某实验小组欲探究影响化学反应速率的因素,设计实验方案如下:
利用 和
和 (草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用
(草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用 溶液已加入稀硫酸酸化)
溶液已加入稀硫酸酸化)
(1)用离子方程式表示该反应的原理:_______
实验设计方案如下:
(2)该实验探究的是_______ 对化学反应速率的影响。褪色时间由小到大的顺序是_______ (填实验序号)。
(3)实验①测得 溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率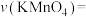
_______ 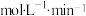 。
。
利用
 和
和 (草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用
(草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用 溶液已加入稀硫酸酸化)
溶液已加入稀硫酸酸化)(1)用离子方程式表示该反应的原理:
实验设计方案如下:
| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1mol/L  (aq) (aq) | 3mL 0.01mol/L  (aq) (aq) |
| ② | 2mL 0.2mol/L  (aq) (aq) | 3mL 0.01mol/ L  (aq) (aq) |
| ③ | 2mL 0.2mol/L  (aq) (aq) | 3mL 0.01mol/L  (aq)+ (aq)+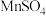 (少量) (少量) |
(3)实验①测得
 溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率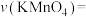
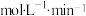 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】化学反应速率及平衡在生产生活中有重要作用。
已知反应
(1)小组同学发现反应速率总是如下图所示,其中 时间内速率变快的主要原因可能是:①该反应放热②
时间内速率变快的主要原因可能是:①该反应放热②___________

(2) 后反应速率逐渐减小的原因是
后反应速率逐渐减小的原因是___________ 。
已知反应

(1)小组同学发现反应速率总是如下图所示,其中
 时间内速率变快的主要原因可能是:①该反应放热②
时间内速率变快的主要原因可能是:①该反应放热②
(2)
 后反应速率逐渐减小的原因是
后反应速率逐渐减小的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g) 2HI(g) ΔH<0.(用“加快”、“减慢”、“不变”填空)
2HI(g) ΔH<0.(用“加快”、“减慢”、“不变”填空)
(1)保持容器容积不变,再向其中充入1molH2,反应速率_____ 。
(2)保持容器容积不变,再向其中充入1molN2(不参加反应),反应速率_____ 。
(3)保持容器内气体的压强不变,再向其中充入1molN2,反应速率_____ 。
(4)保持容器容积不变,再向其中充入1molH2和1molI2,反应速率_____ 。
(5)保持容器内气体的压强不变,再向其中充入1molH2和1molI2,反应速率_____ 。
 2HI(g) ΔH<0.(用“加快”、“减慢”、“不变”填空)
2HI(g) ΔH<0.(用“加快”、“减慢”、“不变”填空)(1)保持容器容积不变,再向其中充入1molH2,反应速率
(2)保持容器容积不变,再向其中充入1molN2(不参加反应),反应速率
(3)保持容器内气体的压强不变,再向其中充入1molN2,反应速率
(4)保持容器容积不变,再向其中充入1molH2和1molI2,反应速率
(5)保持容器内气体的压强不变,再向其中充入1molH2和1molI2,反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在密闭容器中进行如下反应: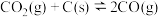
 ,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
(1)增加 的量,则平衡
的量,则平衡___________ (填“逆移”“正移”或“不移”,下同),
___________ (填“增大”“减小”或“不变”,下同)。
(2)恒温条件,增大反应容器的容积,则平衡___________ ,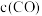
___________ (填“增大”“减小”或“不变”,下同)
(3)保持反应容器的容积和温度不变,通入He气,则平衡___________ ,
___________ 。
(4)保持反应容器的压强不变,通入Ar气,则平衡___________ ,
___________ 。
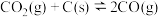
 ,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。(1)增加
 的量,则平衡
的量,则平衡
(2)恒温条件,增大反应容器的容积,则平衡
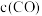
(3)保持反应容器的容积和温度不变,通入He气,则平衡

(4)保持反应容器的压强不变,通入Ar气,则平衡

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】某温度时,在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。由图中数据分析,完成(1)-(2)小题:
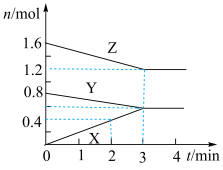
(1)该反应的化学方程式:______ ;
(2)如果第4min时,将密闭容器体积压缩为1L,X、Y、Z的物质的量分别为______ .

(1)该反应的化学方程式:
(2)如果第4min时,将密闭容器体积压缩为1L,X、Y、Z的物质的量分别为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某温度时,在2 L的密闭容器中,X、Y、Z 三种物质的物质的量随时间的变化曲线如图所示。
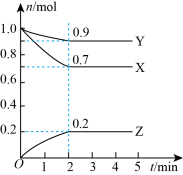
(1)由图中数据分析,该反应的化学方程式_____________ 。
(2)从反应开始至2 min,Z的平均反应速率为________ 。
(3)第5 min时,Z的生成速率________ (填“大于”“小于”或“等于”)Z的消耗速率。
(4)第_______ 分钟时,反应达到平衡。

(1)由图中数据分析,该反应的化学方程式
(2)从反应开始至2 min,Z的平均反应速率为
(3)第5 min时,Z的生成速率
(4)第
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ.(1)在反应A(g)+3B(g)===2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1,则以物质B的化学反应速率为__________ mol·L-1·min-1。
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的此化学反应速率为vB=_________ mol·L-1·s-1。
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有______ mol A,此时C的物质的量浓度为________ ,若此后各物质的量均不再变化,则证明此可逆反应达到了______ 的程度。
A.反应彻底 B.反应终止 C.化学平衡 D.无法判断
Ⅱ. 已知:①2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1;②N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH =________ 。
Ⅲ. 下列热化学方程式书写正确的是(ΔH的绝对值均正确)________ 。
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)ΔH=-57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)===SO2(g)ΔH=-296.8 kJ·mol-1(燃烧热)
D.2NO2===O2+2NOΔH=+116.2 kJ·mol-1(反应热)
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的此化学反应速率为vB=
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)
 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有A.反应彻底 B.反应终止 C.化学平衡 D.无法判断
Ⅱ. 已知:①2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1;②N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH =
Ⅲ. 下列热化学方程式书写正确的是(ΔH的绝对值均正确)
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)ΔH=-57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)===SO2(g)ΔH=-296.8 kJ·mol-1(燃烧热)
D.2NO2===O2+2NOΔH=+116.2 kJ·mol-1(反应热)
您最近一年使用:0次

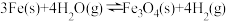 ,在一密闭容器中达到平衡,改变下列条件,判断其正反应速率变化情况。
,在一密闭容器中达到平衡,改变下列条件,判断其正反应速率变化情况。 的量,其正反应速率
的量,其正反应速率 使体系压强增大,其正反应速率
使体系压强增大,其正反应速率

