在恒温恒压下,向体积为2 L密闭容器中充入4mol SO2和2mol O2,生如下反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0。2min后,反应达到平衡,生成SO3为2mol。则0~2 min内v(SO3)__________________ ,平衡后容器中SO2的浓度________________ ,SO2的转化率为___________________ ,在此温度下该反应的平衡常数____________________________ 。
更新时间:2017-11-17 15:28:12
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】CO2催化加氢制甲醇(CH3OH)是实现碳达峰、碳中和的途径之一,其反应可表示为 。
。
(1)该反应分两步进行,反应过程能量变化如图所示,所有物质均为气态。

总反应
___________ 。第①步反应的热化学方程式为___________ 。
(2)一定条件下,向体积为1L的恒容密闭容器中通入2molCO2和6molH2发生反应生成甲醇,每次反应10分钟,测得CO2转化率随温度变化关系如图所示。
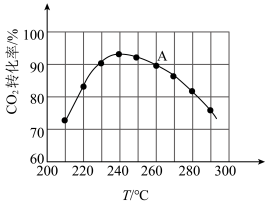
①CO2催化加氢制甲醇的平衡常数表达式K=___________ 。
②已知A点为平衡状态。260℃时从反应开始到恰好平衡CO2的平均反应速率v(CO2)=___________ 。该温度下的平衡常数
___________  。
。
③260℃时,某时刻反应混合物中CO2、H2、CH3OH、H2O的浓度分别为0.1mol/L、0.3mol/L、1mol/L、1mol/L,此时反应进行的方向为___________ (填“正反应方向”“逆反应方向”或“平衡状态”)。
(3)210℃~240℃时,CO2的转化率逐渐增大的原因是___________ 。
 。
。(1)该反应分两步进行,反应过程能量变化如图所示,所有物质均为气态。

总反应

(2)一定条件下,向体积为1L的恒容密闭容器中通入2molCO2和6molH2发生反应生成甲醇,每次反应10分钟,测得CO2转化率随温度变化关系如图所示。

①CO2催化加氢制甲醇的平衡常数表达式K=
②已知A点为平衡状态。260℃时从反应开始到恰好平衡CO2的平均反应速率v(CO2)=

 。
。③260℃时,某时刻反应混合物中CO2、H2、CH3OH、H2O的浓度分别为0.1mol/L、0.3mol/L、1mol/L、1mol/L,此时反应进行的方向为
(3)210℃~240℃时,CO2的转化率逐渐增大的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某温度时,在3L密闭容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:

(1)该反应的化学方程式为:____
(2)反应开始至2min,用X表示的平均反应速率为:__ ;平衡时,Y的浓度为__ ;
(3)在密闭容器里,通入a mol X(s)和b mol Y(g),发生反应X(s)+Y (g) 2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
①增加X(s)的质量:_______ ②增大容器的体积:_______ 。

(1)该反应的化学方程式为:
(2)反应开始至2min,用X表示的平均反应速率为:
(3)在密闭容器里,通入a mol X(s)和b mol Y(g),发生反应X(s)+Y (g)
 2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)①增加X(s)的质量:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某温度下,将H2(g)和I2(g)各1 mol的气态混合物充入2 L的密闭容器中,充分反应,5 min后达到平衡,测得c(HI)=0.2 mol·L-1。
(1)计算从反应开始至达到平衡,用H2(g)表示的反应速率_________ 。
(2)求该反应的平衡常数_________ 。
(1)计算从反应开始至达到平衡,用H2(g)表示的反应速率
(2)求该反应的平衡常数
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】科学家一直致力于“人工固氮”新方法的研究。
(1)传统“人工固氮”的反应为N2(g)+3H2(g) 2NH3(g)。一定温度下,将1molN2和3molH2通入体积为0.5L的密闭容器中,达到平衡状态时H2的转化率为50%,该温度下该反应的平衡常数K=
2NH3(g)。一定温度下,将1molN2和3molH2通入体积为0.5L的密闭容器中,达到平衡状态时H2的转化率为50%,该温度下该反应的平衡常数K=___________ (保留两位有效数字)。
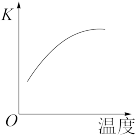
(2)最新“人工固氮”的研究报道,常温常压、光照条件下,N2在催化剂表面与水发生反应:2N2(g)+6H2O(l) 4NH3(g)+3O2(g) ΔH=QkJ·mol-1.已知该反应的平衡常数K与温度的关系如图所示,则此反应为
4NH3(g)+3O2(g) ΔH=QkJ·mol-1.已知该反应的平衡常数K与温度的关系如图所示,则此反应为___________ (填“放热”或“吸热”)反应。
(3)氨催化氧化法制硝酸的主要反应为4NH3(g)+5O2(g)⇋4NO(g)+6H2O(g) ΔH<0;在容积为1L的密闭容器中发生该反应,容器内部分物质的含量如下表:
①反应在第2min到第4min时,NH3的平均反应速率为___________ mol·(L·min)-1。
②下列对于上述反应的判断,正确的是___________ (填序号,下列选项中X%表示X的物质的量百分含量)。
A.若升高反应体系的温度,平衡时体系中NH3%将减小
B.若增大反应体系的压强,平衡时体系中NO%将增大
C.若升高反应体系的温度,平衡时体系中H2O(g)%将增大
D.加入催化剂,平衡时体系中O2%保持不变
(1)传统“人工固氮”的反应为N2(g)+3H2(g)
 2NH3(g)。一定温度下,将1molN2和3molH2通入体积为0.5L的密闭容器中,达到平衡状态时H2的转化率为50%,该温度下该反应的平衡常数K=
2NH3(g)。一定温度下,将1molN2和3molH2通入体积为0.5L的密闭容器中,达到平衡状态时H2的转化率为50%,该温度下该反应的平衡常数K=
(2)最新“人工固氮”的研究报道,常温常压、光照条件下,N2在催化剂表面与水发生反应:2N2(g)+6H2O(l)
 4NH3(g)+3O2(g) ΔH=QkJ·mol-1.已知该反应的平衡常数K与温度的关系如图所示,则此反应为
4NH3(g)+3O2(g) ΔH=QkJ·mol-1.已知该反应的平衡常数K与温度的关系如图所示,则此反应为(3)氨催化氧化法制硝酸的主要反应为4NH3(g)+5O2(g)⇋4NO(g)+6H2O(g) ΔH<0;在容积为1L的密闭容器中发生该反应,容器内部分物质的含量如下表:
| 物质的量 时间 | n(NH3) (mol) | n(O2) (mol) | n(NO) (mol) |
| 起始 | 1.60 | 3.20 | 0.00 |
| 第2min | a | 2.70 | 0.40 |
| 第4min | 0.60 | 1.95 | 1.00 |
| 第6min | 0.60 | 1.95 | 1.00 |
②下列对于上述反应的判断,正确的是
A.若升高反应体系的温度,平衡时体系中NH3%将减小
B.若增大反应体系的压强,平衡时体系中NO%将增大
C.若升高反应体系的温度,平衡时体系中H2O(g)%将增大
D.加入催化剂,平衡时体系中O2%保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在硫酸工业中,通过下列反应使SO2氧化为SO3:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
(1)从理论上分析,为了使二氧化硫尽可能多地转化为三氧化硫,应选择的条件是___________ 。
(2)在实际生产中,选定的温度为400℃~500℃,原因是___________
(3)在实际生产中,采用的压强为常压,原因是___________
(4)在实际生产中,通入过量的空气,原因是___________
(5)尾气中的SO2必须回收,原因是___________ 。
(6)在550℃、1MPa下,若SO2的起始浓度为2mol/L,O2的起始浓度为1mol/L,试求该条件下的平衡常数K=___________ 。
 2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。
2SO3(g)ΔH=-196.6kJ·mol-1.下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。| 温度/℃ | 平衡时SO2的转化率/% | ||||
| 0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 95.0 | 97.7 | 98.3 |
(2)在实际生产中,选定的温度为400℃~500℃,原因是
(3)在实际生产中,采用的压强为常压,原因是
(4)在实际生产中,通入过量的空气,原因是
(5)尾气中的SO2必须回收,原因是
(6)在550℃、1MPa下,若SO2的起始浓度为2mol/L,O2的起始浓度为1mol/L,试求该条件下的平衡常数K=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某温度时在2L容器中X、Y、Z三种气物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:

(1)0-2分钟期间X的平均反应速率=______ mol/(L·min)。
(2)该反应达到平衡时,X的转化率为__________ 。
(3)该反应的化学方程式为__________ 。
(4)在密闭容器里,通入amolX(g)和bmolY(g),发生上述反应,当改变下列条件时,反应速率可能会发生什么变化(选填“增大”、“减小”或“不变”)?
①降低温度___________ ;
②恒容通入氦气___________ ;
③使用合适的催化剂___________

(1)0-2分钟期间X的平均反应速率=
(2)该反应达到平衡时,X的转化率为
(3)该反应的化学方程式为
(4)在密闭容器里,通入amolX(g)和bmolY(g),发生上述反应,当改变下列条件时,反应速率可能会发生什么变化(选填“增大”、“减小”或“不变”)?
①降低温度
②恒容通入氦气
③使用合适的催化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一定温度下,体积为2L的密闭容器中,X、Y间发生反应。各物质的物质的量随时间变化的关系如图所示。

请回答下列问题:
(1)该反应的化学方程式可表示为_________________ 。在0到1min中内用X表示该反应的速率是________________ ,该反应达最大限度时Y的转化率_______________ 。
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中υ(X)=0.3 mol∙L−1∙min−1,乙中υ(Y)=0.2 mol∙L−1∙min−1,则__________ 中反应更快。
(3)若X、Y均为气体,且X为无色气体,Y为红棕色气体。下列描述能表示反应达平衡状态的是 。
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨Ⅱ电极上生成氧化物Y(N2O5),则石墨I电极是________ (填“正极”或“负极”),石墨Ⅱ的电极反应式为_______ 。


请回答下列问题:
(1)该反应的化学方程式可表示为
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中υ(X)=0.3 mol∙L−1∙min−1,乙中υ(Y)=0.2 mol∙L−1∙min−1,则
(3)若X、Y均为气体,且X为无色气体,Y为红棕色气体。下列描述能表示反应达平衡状态的是 。
| A.容器中X与Y的物质的量相等 |
| B.容器内气体的颜色不再改变 |
| C.2υ(X)=υ(Y) |
| D.容器内气体的平均相对分子质量不再改变 |

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在2 L密闭容器内,800℃时反应2NO(g)+O2(g)⇌2NO2(g)体系中,n(NO)随时间的变化如表:
(1)800℃,反应进行到2s时,NO的转化率是_______ ,反应达到最大限度时,NO的物质的量浓度为_______ mol/L。
(2)如图中表示NO2变化的曲线是_______ (填字母序号a、b、c、d)。用O2表示从0~2 s内该反应的平均速率v=_______ mol/(L·s)。
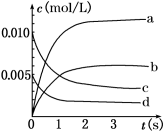
(3)能使该反应的反应速率增大的操作是_______。
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应进行到2s时,NO的转化率是
(2)如图中表示NO2变化的曲线是

(3)能使该反应的反应速率增大的操作是_______。
| A.及时分离出NO2气体 | B.适当升高温度 |
| C.增大O2的浓度 | D.选择高效催化剂 |
您最近一年使用:0次




