某实验小组欲探究影响化学反应速率的因素,设计实验方案如下:
利用 和
和 (草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用
(草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用 溶液已加入稀硫酸酸化)
溶液已加入稀硫酸酸化)
(1)用离子方程式表示该反应的原理:_______
实验设计方案如下:
(2)该实验探究的是_______ 对化学反应速率的影响。褪色时间由小到大的顺序是_______ (填实验序号)。
(3)实验①测得 溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率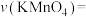
_______ 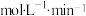 。
。
利用
 和
和 (草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用
(草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用 溶液已加入稀硫酸酸化)
溶液已加入稀硫酸酸化)(1)用离子方程式表示该反应的原理:
实验设计方案如下:
| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1mol/L  (aq) (aq) | 3mL 0.01mol/L  (aq) (aq) |
| ② | 2mL 0.2mol/L  (aq) (aq) | 3mL 0.01mol/ L  (aq) (aq) |
| ③ | 2mL 0.2mol/L  (aq) (aq) | 3mL 0.01mol/L  (aq)+ (aq)+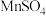 (少量) (少量) |
(3)实验①测得
 溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率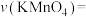
 。
。
更新时间:2022-10-24 16:27:36
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】近日,中国科学院深圳先进技术研究院某研究团队发现,二维铜铟磷硫(CuInP2S6)能作纳米药物,用于未来安全有效的抗SARS-CoV-2治疗,以降低SARS-CoV-2的传染性。
请回答下列问题:
(1)中国科学院张青莲院士主持测定的铟(49In)元素的相对原子质量的新值已被采用为国际新标准。已知铟与铷同周期,则In在元素周期表中的位置为______ ;其最高价氧化物能用于金属反射镜面的保护涂层、光电显示半导体薄膜,则铟元素的最高价氧化物的化学式为______ 。
(2)已知Cu2O在酸性条件下易歧化,据此写出Cu2O与稀硫酸反应的离子方程式:____________ 。
(3)磷、硫元素的最高价氧化物对应水化物的酸性由强到弱的顺序为______ (用化学式表示),结合元素周期律解释其原因:____________ 。
(4)已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测正确的是______ (填序号)。
a.含有离子键和共价键
b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
请回答下列问题:
(1)中国科学院张青莲院士主持测定的铟(49In)元素的相对原子质量的新值已被采用为国际新标准。已知铟与铷同周期,则In在元素周期表中的位置为
(2)已知Cu2O在酸性条件下易歧化,据此写出Cu2O与稀硫酸反应的离子方程式:
(3)磷、硫元素的最高价氧化物对应水化物的酸性由强到弱的顺序为
(4)已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测正确的是
a.含有离子键和共价键
b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氰化钠(NaCN)是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。NaCN的电子式为________ ;实验室用NaCN固体配制NaCN溶液时,应先将其溶于氢氧化钠溶液中,再用蒸馏水稀释。NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是___________________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】为倡导“节能减排”和“低碳经济”,降低大气中CO2含量及有效地开发利用CO2,工业上可用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入1molCO2、3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
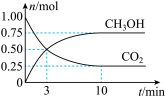
(1)写出该反应的化学平衡常数表达式:K=________ 。
(2)在3min末,反应速率v(正)________ v(逆)(选填>、<或=)。
(3)从反应开始到平衡,平均反应速率v(CO2)=_________ 。达到平衡时,H2的转化率为________ 。
(4)下列措施可以加快反应速率的是________ 。
(5)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为:甲:v(H2)=0.45mol•L-1•s-1;乙:v(CO2)=0.2mol•L-1•s-1;丙:v(CH3OH)=6mol•L-1•min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为________ 。
 CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
(1)写出该反应的化学平衡常数表达式:K=
(2)在3min末,反应速率v(正)
(3)从反应开始到平衡,平均反应速率v(CO2)=
(4)下列措施可以加快反应速率的是
| A.升高温度 | B.加入催化剂 | C.增大压强 | D.及时分离出CH3OH |
(5)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为:甲:v(H2)=0.45mol•L-1•s-1;乙:v(CO2)=0.2mol•L-1•s-1;丙:v(CH3OH)=6mol•L-1•min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某温度时,在2L的密闭容器中,X、Y、Z三种气态物质的量随时间的变化曲线如图所示。
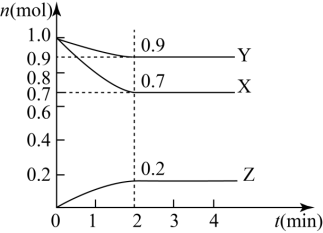
(1)由图中所给数据进行分析,该反应的化学方程式为________ ;
(2)反应从开始至2分钟末,用Y的浓度变化表示的平均反应速率为v(Y)=________ ;
(3)该反应开始时的物质的量与反应平衡时的物质的量之比为________ ;
(4)X的转化率是________ 。

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)反应从开始至2分钟末,用Y的浓度变化表示的平均反应速率为v(Y)=
(3)该反应开始时的物质的量与反应平衡时的物质的量之比为
(4)X的转化率是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】用焦炭生产水煤气的反应为:C(s)+H2O(g) CO(g)+H2(g)。
CO(g)+H2(g)。
(1)一定温度下,在一个固定容积的密闭容器中发生上述反应,下列不能判断该反应达到平衡状态的是___________。(选填编号)
(2)将不同量的 C (s)和 H2O (g)分别加入到体积为 2 L 的恒容密闭容器中,进行反应,得到如下数据:
实验 1 中以 v(H2) 表示的到达平衡时的平均反应速率为___________ 。
 CO(g)+H2(g)。
CO(g)+H2(g)。(1)一定温度下,在一个固定容积的密闭容器中发生上述反应,下列不能判断该反应达到平衡状态的是___________。(选填编号)
| A.容器中的压强不再改变 |
| B.混合气体的密度不再改变 |
| C.v 正(CO)=v 逆(H2O) |
| D.c(CO)=c(H2) |
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | C | H2 | CO | |||
| 1 | 650 | 0.01 | 0.02 | 0.008 | 5 | |
| 2 | 800 | 0.02 | 0.03 | 0.017 | 3 | |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】化学反应速率和限度与生产、生活密切相关。
某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
(1)哪一时间段反应速率最大__ min(填0~1、1~2、2~3、3~4、4~5)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入少量的下列溶液以减慢反应速率,你认为可行的是__ 。
A.NaNO3溶液 B.CuSO4溶液 C.蒸馏水 D.KCl溶液
某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
(1)哪一时间段反应速率最大
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入少量的下列溶液以减慢反应速率,你认为可行的是
A.NaNO3溶液 B.CuSO4溶液 C.蒸馏水 D.KCl溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】T℃时,向体积为1L的恒容密闭容器中通入1molH2和1molCl2,一定条件下发生反应H2(g)+Cl2(g) 2HCl(g), HCl的物质的量随时间变化如图所示。
2HCl(g), HCl的物质的量随时间变化如图所示。

回答下列问题:
(1) tm时,υ正_______ υ逆(填“>”、“<”或“=”)。
(2) 0~tm内H2的平均反应速率υ(H2)=__________ 。
(3)若要增大HCl的生成速率可以采取的措施有____ 、____ 。(填写两种措施)
(4)下列说法能表明该反应已达到平衡状态的是___ (填序号)。
①生成2 mol HCl的同时消耗1 mol H2
②混合气体中HCl的物质的量分数保持不变
③混合气体中各物质的浓度保持不变
④混合气体中H2、Cl2的浓度之比为1∶1
(5)达到平衡后,升高反应温度,再次达到平衡后,测得HCl的物质的量分数为20%。则升高反应温度,该反应向___ (填“正反应”、 “逆反应”或“不移动”)方向发生移动。
 2HCl(g), HCl的物质的量随时间变化如图所示。
2HCl(g), HCl的物质的量随时间变化如图所示。
回答下列问题:
(1) tm时,υ正
(2) 0~tm内H2的平均反应速率υ(H2)=
(3)若要增大HCl的生成速率可以采取的措施有
(4)下列说法能表明该反应已达到平衡状态的是
①生成2 mol HCl的同时消耗1 mol H2
②混合气体中HCl的物质的量分数保持不变
③混合气体中各物质的浓度保持不变
④混合气体中H2、Cl2的浓度之比为1∶1
(5)达到平衡后,升高反应温度,再次达到平衡后,测得HCl的物质的量分数为20%。则升高反应温度,该反应向
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究。
(1)取等物质的量浓度、等体积的 H2O2溶液分别进行 H2O2的分解实验,实验报告如下表所示(现象和结论略)。
①实验 1、2 研究的是_____ 对 H2O2分解速率的影响。
②实验 2、3 的目的是_____ 。
(2)查文献可知:Cu2+对 H2O2分解也有催化作用,为比较 Fe3+、Cu2+对 H2O2 分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

①定性分析:如图甲可通过观察_____ ,先定性比较得出结论。有同学提出 将 CuSO4溶液改为 CuCl2溶液更合理,其理由是_________ 。
②定量分析:如图乙所示,实验时以收集到 40 mL 气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是_____ 。
(1)取等物质的量浓度、等体积的 H2O2溶液分别进行 H2O2的分解实验,实验报告如下表所示(现象和结论略)。
| 序号 | 温度/℃ | 催化剂 | 现象 | 结论 |
| 1 | 40 | FeCl3溶液 | ||
| 2 | 20 | FeCl3溶液 | ||
| 3 | 20 | MnO2 | ||
| 4 | 20 | 无 |
②实验 2、3 的目的是
(2)查文献可知:Cu2+对 H2O2分解也有催化作用,为比较 Fe3+、Cu2+对 H2O2 分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

①定性分析:如图甲可通过观察
②定量分析:如图乙所示,实验时以收集到 40 mL 气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】甲醇蒸气转化为氢气的一种原理是 和
和 反应生成
反应生成 和
和 。
。
图是该过程中的能量变化示意图。若在反应体系中加入催化剂,反应速率增大,正反应活化能 的变化是
的变化是______ (填“增大”“减小”或“不变”),反应热 的变化是
的变化是______ (填“增大”“减小”或“不变”)。请写出 和
和 反应的热化学方程式:
反应的热化学方程式:______ 。
 和
和 反应生成
反应生成 和
和 。
。
图是该过程中的能量变化示意图。若在反应体系中加入催化剂,反应速率增大,正反应活化能
 的变化是
的变化是 的变化是
的变化是 和
和 反应的热化学方程式:
反应的热化学方程式:
您最近一年使用:0次
【推荐3】二氧化碳捕获技术用于去除气流中的二氧化碳或者分离出二氧化碳作为气体产物,其中CO2催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有催化剂时的能量变化。

(1)从图可知,有催化剂存在的是过程_______ (填“Ⅰ”或“Ⅱ”)。
(2)写出图中CO2催化合成甲醇的热化学方程式:_______ 。
(3)已知:1mol液态甲醇完全气化需吸热37.4kJ,1mol液态水完全气化需吸热44.0kJ,由CO2合成1mol液态甲醇和1mol液态水将_______ (填“吸收”或“放出”)_______ kJ热量。
(4)关于CO2催化合成甲醇的反应,下列说法中,合理的是_______(填字母序号)。

(1)从图可知,有催化剂存在的是过程
(2)写出图中CO2催化合成甲醇的热化学方程式:
(3)已知:1mol液态甲醇完全气化需吸热37.4kJ,1mol液态水完全气化需吸热44.0kJ,由CO2合成1mol液态甲醇和1mol液态水将
(4)关于CO2催化合成甲醇的反应,下列说法中,合理的是_______(填字母序号)。
| A.该反应中所有原子都被用于合成甲醇 |
| B.该反应可用于CO2的转化,有助于缓解温室效应 |
| C.使用催化剂可以降低该反应的ΔH,从而使反应放出更多热量 |
| D.降温分离出液态甲醇和水,将剩余气体重新通入反应器,可以提高CO2与H2的利用率 |
您最近一年使用:0次




