一定温度下,在2 L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
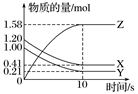
(1)从反应开始到10 s时,用Z表示的反应速率为________________________ ,X的物质的量浓度减少了_________________ ,Y的转化率为__________ 。
(2)该反应的化学方程式为________________________________________ 。

(1)从反应开始到10 s时,用Z表示的反应速率为
(2)该反应的化学方程式为
更新时间:2017-09-21 16:44:49
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】某温度时,在容积为3 L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。
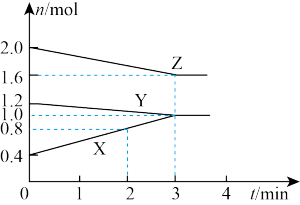
分析图中数据,回答下列问题:
(1)该反应的化学方程式为___________ 。
(2)反应开始至2 min末,X的反应速率为___________ 。

分析图中数据,回答下列问题:
(1)该反应的化学方程式为
(2)反应开始至2 min末,X的反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)恒温恒容条件下,将6molA气体和8molB气体通入体积为10L的密闭容器中发生如下反应:2A(g)+B(g) 4C(g) +2D(s),2min末达平衡,测得平衡时A为2.4mol。
4C(g) +2D(s),2min末达平衡,测得平衡时A为2.4mol。
①从开始至平衡状态,生成C的平均反应速率为____ 。
②B的转化率为____ 。
③该上述反应在三个容器中进行,测的反应速率如下,其中能表明反应速率最快的是____ 。
A.v(A)=0.4mol·L-1·s-1 B.v(B)=1.0mol·L-1·s-1 C.v(C)=2mol·L-1·s-1
④能说明该反应已达到平衡状态的是____ (填字母)。
a.相同时间内消耗A的物质的量与生成D的物质的量相等
b.容器内C的物质的量浓度保持不变
c.2v逆(A)=v正(B)
d.容器内混合气体的质量保持不变
(2)某温度时,在5L容器中X、Y、Z三种物质的物质的量(n)随着时间(t)变化的曲线如图所示。由图中数据分析:
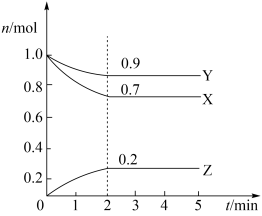
①该反应的化学方程式为____ 。
②在密闭容器里,通入3molX(g)、1molY(g),发生上述反应,当改变下列条件时,反应速率一定会增大的是____ (填序号)。
a.升高温度 b.加入催化剂 c.增大容器体积 d.加入Z
(1)恒温恒容条件下,将6molA气体和8molB气体通入体积为10L的密闭容器中发生如下反应:2A(g)+B(g)
 4C(g) +2D(s),2min末达平衡,测得平衡时A为2.4mol。
4C(g) +2D(s),2min末达平衡,测得平衡时A为2.4mol。①从开始至平衡状态,生成C的平均反应速率为
②B的转化率为
③该上述反应在三个容器中进行,测的反应速率如下,其中能表明反应速率最快的是
A.v(A)=0.4mol·L-1·s-1 B.v(B)=1.0mol·L-1·s-1 C.v(C)=2mol·L-1·s-1
④能说明该反应已达到平衡状态的是
a.相同时间内消耗A的物质的量与生成D的物质的量相等
b.容器内C的物质的量浓度保持不变
c.2v逆(A)=v正(B)
d.容器内混合气体的质量保持不变
(2)某温度时,在5L容器中X、Y、Z三种物质的物质的量(n)随着时间(t)变化的曲线如图所示。由图中数据分析:

①该反应的化学方程式为
②在密闭容器里,通入3molX(g)、1molY(g),发生上述反应,当改变下列条件时,反应速率一定会增大的是
a.升高温度 b.加入催化剂 c.增大容器体积 d.加入Z
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.影响化学反应速率的因素有多种,请在横线上填入与下列各项关系最为密切的影响化学反应速率的因素(填“温度”、“浓度”、“催化剂”、“压强”、“物质本身的性质”或“固体表面积”):
(1)夏天的食品易变霉,在冬天不易发生该现象:_______ 。
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:_______ 。
(3)MnO2加入双氧水中放出气泡加快:__________ 。
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量浓度随时间变化的曲线如图所示。
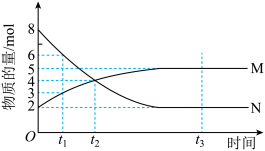
(1)比较t2时刻,正、逆反应速率大小:v(正)________ (填“>”“=”或“<”)v(逆)。
(2)若t2=2 min,反应开始至t2时刻,M的平均化学反应速率v(M)=______ mol·L-1·min-1。
(3)t1、t2、t3三个时刻中处于平衡状态的时刻为_________ (填“t1”“t2”或“t3”)。
(4)如果升高温度,则v(逆)________ (填“增大”“减小”或“不变”)。
(1)夏天的食品易变霉,在冬天不易发生该现象:
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:
(3)MnO2加入双氧水中放出气泡加快:
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量浓度随时间变化的曲线如图所示。

(1)比较t2时刻,正、逆反应速率大小:v(正)
(2)若t2=2 min,反应开始至t2时刻,M的平均化学反应速率v(M)=
(3)t1、t2、t3三个时刻中处于平衡状态的时刻为
(4)如果升高温度,则v(逆)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H1
CH3OH(g)+H2O(g)△H1
②CO2(g)+H2(g) CO(g)+H2O(g)△H2
CO(g)+H2O(g)△H2
③CH3OH(g) CO(g)+2H2(g)△H3
CO(g)+2H2(g)△H3
回答下列问题:
(1)已知反应ⅱ中相关化学键键能数据如下:
由此计算△H2=___ kJ∙mol−1。已知△H1=−63 kJ∙mol−1,则△H3=___ kJ∙mol−1。
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。
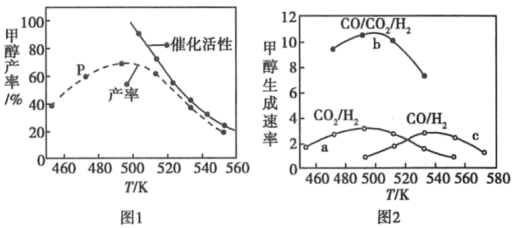
①温度为470K时,图中P点___ (填“是”或“不是”)处于平衡状态。490K之后,甲醇产率下降的原因是___ 。
②提高甲醇产率的措施是___ 。
A.增大压强 B.升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)如图2为一定比例的CO2/H2,CO/H2、CO/CO2/H2条件下甲醇生成速率与温度的关系。当温度为490K时,根据曲线a、c,判断合成甲醇的反应机理是___ (填“I”或“II”)。
Ⅰ.CO2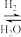 CO
CO CH3OH
CH3OH
Ⅱ.CO CO2
CO2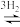 CH3OH+H2O
CH3OH+H2O
(4)490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从平衡移动的角度,并结合反应①、②分析原因___ 。
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H1
CH3OH(g)+H2O(g)△H1②CO2(g)+H2(g)
 CO(g)+H2O(g)△H2
CO(g)+H2O(g)△H2③CH3OH(g)
 CO(g)+2H2(g)△H3
CO(g)+2H2(g)△H3回答下列问题:
(1)已知反应ⅱ中相关化学键键能数据如下:
| 化学键 | H—H | C=O | C≡O | H—O |
| E/( kJ∙mol−1) | 436 | 803 | 1076 | 465 |
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。

①温度为470K时,图中P点
②提高甲醇产率的措施是
A.增大压强 B.升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)如图2为一定比例的CO2/H2,CO/H2、CO/CO2/H2条件下甲醇生成速率与温度的关系。当温度为490K时,根据曲线a、c,判断合成甲醇的反应机理是
Ⅰ.CO2
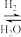 CO
CO CH3OH
CH3OHⅡ.CO
 CO2
CO2 CH3OH+H2O
CH3OH+H2O(4)490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从平衡移动的角度,并结合反应①、②分析原因
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】密闭容器中发生如下反应:A(g)+3B(g) 2C(g)ΔH<0,根据下列速率-时间图象,回答下列问题:
2C(g)ΔH<0,根据下列速率-时间图象,回答下列问题:

(1)下列时刻所改变的外界条件是:t1___________ ;t3___________ ;t4___________ ;
(2)产物C的体积分数最大的时间段是_______________ ;A的物质的量最大的时间段是___________
(3)反应速率最大的时间段是___________ ;
 2C(g)ΔH<0,根据下列速率-时间图象,回答下列问题:
2C(g)ΔH<0,根据下列速率-时间图象,回答下列问题:
(1)下列时刻所改变的外界条件是:t1
(2)产物C的体积分数最大的时间段是
(3)反应速率最大的时间段是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】一定温度下,在容积为V L的密闭容器中进行反应,M、N两种气体的物质的量随时间的变化曲线如图所示:
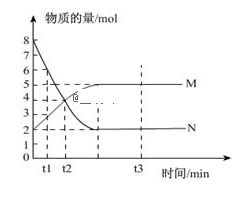
(1)该反应的生成物是___________ ;
(2)该反应的化学反应方程式为_____________ ;
(3)到t2时刻,以M的浓度变化表示的平均反应速率为____________ ;
(4)若达到平衡状态的时间是4 min,N物质在该4 min内的平均反应速率为1.5mol·L-1·min-1,则此容器的容积V=____________ L。
(5)达到平衡状态时,反应物的转化率为____________ ;

(1)该反应的生成物是
(2)该反应的化学反应方程式为
(3)到t2时刻,以M的浓度变化表示的平均反应速率为
(4)若达到平衡状态的时间是4 min,N物质在该4 min内的平均反应速率为1.5mol·L-1·min-1,则此容器的容积V=
(5)达到平衡状态时,反应物的转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】研究化学反应的快慢和限度具有十分重要的意义,已知:反应aA(g)+bB(g)⇌cC(g),某温度下,在2L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示。

(1)经测定,前4s内v(C)=0.05mol·L-1·s-1,4s时容器内C的物质的量为___________ ,则该反应的化学方程式为___________ 。
(2)该反应达到化学反应限度时,A的转化率为___________ 。
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的化学反应速率分别为:
甲:v(A)=0.3mol·L-1·s-1;
乙:v(B)=0.2mol·L-1·s-1;
丙:v(C)=0.6mol·L-1·min-1。
则甲、乙、丙三个容器中化学反应速率由快到慢的顺序为___________ (用甲、乙、丙表示)。
(4)下列条件的改变能减小上述反应的反应速率的是___________ 。
①保持体积不变,充入He
②保持压强不变,充入He
③降低温度
④增大C的浓度
(5)下列叙述能说明该反应达到化学平衡状态的是___________ 。
①混合气体的总质量不随时间变化而变化
②单位时间内每消耗3molA,同时生成1molB
③3v(A)正=v(B)逆
④混合气体的密度不随时间变化而变化
⑤A物质的物质的量分数不随时间变化而变化

(1)经测定,前4s内v(C)=0.05mol·L-1·s-1,4s时容器内C的物质的量为
(2)该反应达到化学反应限度时,A的转化率为
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的化学反应速率分别为:
甲:v(A)=0.3mol·L-1·s-1;
乙:v(B)=0.2mol·L-1·s-1;
丙:v(C)=0.6mol·L-1·min-1。
则甲、乙、丙三个容器中化学反应速率由快到慢的顺序为
(4)下列条件的改变能减小上述反应的反应速率的是
①保持体积不变,充入He
②保持压强不变,充入He
③降低温度
④增大C的浓度
(5)下列叙述能说明该反应达到化学平衡状态的是
①混合气体的总质量不随时间变化而变化
②单位时间内每消耗3molA,同时生成1molB
③3v(A)正=v(B)逆
④混合气体的密度不随时间变化而变化
⑤A物质的物质的量分数不随时间变化而变化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)已知:2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ/mol;
H2(g)+ O2(g)=H2O(1); △H=-285.8 kJ/mol,
O2(g)=H2O(1); △H=-285.8 kJ/mol,
由此可知,在等温下蒸发45 g液态水需吸收___________ kJ的热量。
(2)在一定条件下,1 mol某气体若被O2完全氧化放热98.0 kJ。现有2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为:___________ (注:某反应物的转化率=该反应物转化(消耗)的物质的量÷该反应物起始的物质的量×100%)
(3)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。 已知:N≡N键的键能是948.9kJ·mol-1,H-H键的键能是436.0 kJ·mol-1,由N2和H2合成1molNH3时可放出46.2kJ的热量。 N-H键的键能是___________ kJ·mol-1
(1)已知:2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ/mol;
H2(g)+
 O2(g)=H2O(1); △H=-285.8 kJ/mol,
O2(g)=H2O(1); △H=-285.8 kJ/mol,由此可知,在等温下蒸发45 g液态水需吸收
(2)在一定条件下,1 mol某气体若被O2完全氧化放热98.0 kJ。现有2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为:
(3)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。 已知:N≡N键的键能是948.9kJ·mol-1,H-H键的键能是436.0 kJ·mol-1,由N2和H2合成1molNH3时可放出46.2kJ的热量。 N-H键的键能是
您最近一年使用:0次




