某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
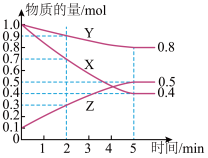
(1)反应的化学方程式是___________ 。
(2)2min内Y的转化率为___________ 。

(1)反应的化学方程式是
(2)2min内Y的转化率为
更新时间:2021-05-18 19:01:43
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如图所示,在容器A中装有20℃的水50mL,容器B中装有1mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2 ⇌ N2O4 △H=-57kJ/mol,当向A中加入50gNH4NO3晶体使之溶解;向B中加入2g苛性钠时:
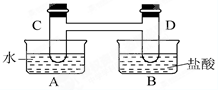
(1)C中的气体颜色______ ; (填“变浅” 或“变深”).
(2)若25℃时,起始时仅有NO2气体,达到平衡时,c(NO2)=0.0125mol/L,c(N2O4)=0.0321mol/L,则NO2的起始浓度为_____________ ,NO2的转化率为________ .

(1)C中的气体颜色
(2)若25℃时,起始时仅有NO2气体,达到平衡时,c(NO2)=0.0125mol/L,c(N2O4)=0.0321mol/L,则NO2的起始浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】将4 molA气体和2mol B气体在2L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g) 2C(g),若经2s后测得C的浓度为0.6mol·L-1,则
2C(g),若经2s后测得C的浓度为0.6mol·L-1,则
(1)用物质A表示的反应速率为____ 。
(2)用物质B表示的反应速率为____ 。
(3)2s时物质B的转化率为_____ 。
(4)2s时物质A的浓度为_____ 。
 2C(g),若经2s后测得C的浓度为0.6mol·L-1,则
2C(g),若经2s后测得C的浓度为0.6mol·L-1,则(1)用物质A表示的反应速率为
(2)用物质B表示的反应速率为
(3)2s时物质B的转化率为
(4)2s时物质A的浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.H2S与CH4重整,不但可以消除污染,还可以制氢。主要反应为 ;ΔH>0。
;ΔH>0。
(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应: ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。_______ 、_______ (填化学式)。
(3)M点对应温度下,H2S的转化率是_______ 。
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。_______ (填“A”“B”或“C”)组图像。三组图像中,C组图像中平均反应速率最低的可能原因是_______ 。
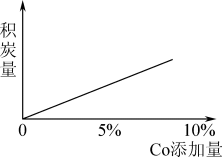
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为____ 。
 ;ΔH>0。
;ΔH>0。(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
| A.混合气体密度不变 |
| B.容器内压强不变 |
| C.2v正(H2S)=v逆(CS2) |
| D.CH4与H2的物质的量分数之比保持不变 |
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应:
 ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。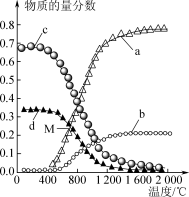
(3)M点对应温度下,H2S的转化率是
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。
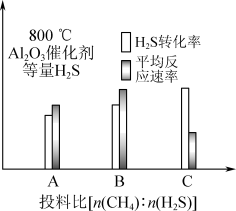
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2 L的密闭容器中发生反应:N2O4(g)  2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如下图所示。
2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如下图所示。
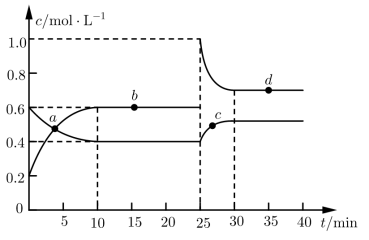
(1)该温度下,该反应的平衡常数为___________ ,若温度升高,K值将___________ (填“增大”“减小”或“不变”)。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的是___________ 点。从起点开始首次达到平衡时,以NO2表示的反应速率为___________ 。
(3)25 min时,加入了___________ (填加入物质的化学式及加入的物质的量),使平衡发生了移动。
 2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如下图所示。
2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如下图所示。
(1)该温度下,该反应的平衡常数为
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的是
(3)25 min时,加入了
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表所示:
①该反应的化学平衡常数表达式为K=___________ 。
②该反应为___________ 反应(填“吸热”或“放热”)。
③某温度下,平衡浓度符合下式:c(CO2)∙c(H2)=c(CO)∙c(H2O),试判断此时的温度为___________ ℃。
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol/L,c(H2)=1.5mol/L,c(CO)=1mol/L,c(H2O)=3mol/L,则下一时刻,反应向___________ (填“正向”或“逆向”)进行。
(2)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料, 4Al(s)+3TiO2(s)+3C(s) =2Al2O3(s)+3TiC(s) ΔH=−1176 kJ∙mol−1,则反应过程中,每转移1 mol电子放出的热量为___________ 。
(3)t℃时,关于N2、NH3的两个反应的信息如下表所示:
请写出t℃时NH3被NO氧化生成无毒气体的热化学方程式___________ (反应热用a、b、e、d代数式表示)。t℃该反应的平衡常数为___________ (用K1和K2表示)。
(1)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表所示:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应的化学平衡常数表达式为K=
②该反应为
③某温度下,平衡浓度符合下式:c(CO2)∙c(H2)=c(CO)∙c(H2O),试判断此时的温度为
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol/L,c(H2)=1.5mol/L,c(CO)=1mol/L,c(H2O)=3mol/L,则下一时刻,反应向
(2)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料, 4Al(s)+3TiO2(s)+3C(s) =2Al2O3(s)+3TiC(s) ΔH=−1176 kJ∙mol−1,则反应过程中,每转移1 mol电子放出的热量为
(3)t℃时,关于N2、NH3的两个反应的信息如下表所示:
| 化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
| N2(g)+O2(g)=2NO(g) ∆H>0 | a kJ∙mol−1 | b kJ∙mol−1 | K1 |
| 4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ∆H<0 | e kJ∙mol−1 | d kJ∙mol−1 | K2 |
请写出t℃时NH3被NO氧化生成无毒气体的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】某温度时,在容积为2L的密闭容器中,A、B气体的物质的量随时间变化的曲线如图I所示。若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。请据图回答下列问题:
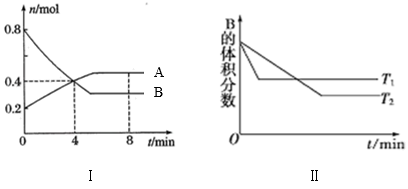
(1)该反应的化学方程式为____ 。正反应为____ (填“吸热”或“放热”)反应。
(2)在4min末时,A、B的物质的量浓度c(A)___ c(B),从0~4min内A、B的物质的量浓度变化量Δc(A)___ Δc(B)(以上填“>”、“<”或“=”)。
(3)反应开始至4min时,A的平均反应速率为____ 。
(4)4min时,v(正)__ (填“>”、“<”或“=”)v(逆)。
(5)8min后,改变下列某一条件,能使平衡向逆反应方向移动的有___ (填字母)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度

(1)该反应的化学方程式为
(2)在4min末时,A、B的物质的量浓度c(A)
(3)反应开始至4min时,A的平均反应速率为
(4)4min时,v(正)
(5)8min后,改变下列某一条件,能使平衡向逆反应方向移动的有
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
您最近一年使用:0次



