化学能在一定条件下可转化为电能。
(1)将锌片放入盛有稀硫酸的烧杯中,反应的化学方程式为_______ 。
(2)将锌片、铜片按照如图所示装置连接,锌片是_______ (填“正极”或“负极”)。能证明化学能转化为电能的实验现象是:_______ 、_______ 。锌片上的电极反应式为_______ 铜片上的电极反应式为_______ 。稀硫酸在如图所示装置中的作用是:传导离子、_______ 。
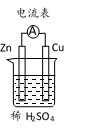
(3)下列反应通过原电池装置,可实现化学能直接转化为电能的是_______ (填序号)。
①2H2+O2 2H2O
2H2O
②Fe+Cu2+=Cu+Fe2+
③CaO+H2O=Ca(OH)2
(1)将锌片放入盛有稀硫酸的烧杯中,反应的化学方程式为
(2)将锌片、铜片按照如图所示装置连接,锌片是

(3)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①2H2+O2
 2H2O
2H2O②Fe+Cu2+=Cu+Fe2+
③CaO+H2O=Ca(OH)2
更新时间:2021-05-28 12:40:13
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】某同学设计实验探究构成原电池的条件,装置如图所示。
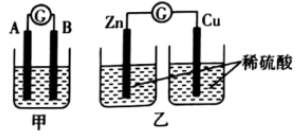
实验一:探究电极的构成(甲图)
①A、B两极均选用石墨,发现灵敏电流计指针不偏转;
②A、B两极均选用铜片,发现灵敏电流计指针不偏转;
③A极用锌片,B极用铜片,发现电流计指针向左偏转;
④A极用锌片,B极用石墨,发现电流计指针向左偏转。
结论一:_____________________ 。
实验二:探究溶液的构成(甲图,A极用锌片,B极用铜片)
①液体采用无水乙醇,发现灵敏电流计指针不偏转。
②改用硫酸溶液,发现灵敏电流计指针偏转,B极上有气体产生。
结论二:_______________________ 。
实验三:对比实验,探究乙图装置能否构成原电池将锌、铜两电极分别放入稀硫酸中,发现锌片上有气泡产生,铜片上无明显现象,灵敏电流计指针不发生偏转。
结论三:________________________ 。

实验一:探究电极的构成(甲图)
①A、B两极均选用石墨,发现灵敏电流计指针不偏转;
②A、B两极均选用铜片,发现灵敏电流计指针不偏转;
③A极用锌片,B极用铜片,发现电流计指针向左偏转;
④A极用锌片,B极用石墨,发现电流计指针向左偏转。
结论一:
实验二:探究溶液的构成(甲图,A极用锌片,B极用铜片)
①液体采用无水乙醇,发现灵敏电流计指针不偏转。
②改用硫酸溶液,发现灵敏电流计指针偏转,B极上有气体产生。
结论二:
实验三:对比实验,探究乙图装置能否构成原电池将锌、铜两电极分别放入稀硫酸中,发现锌片上有气泡产生,铜片上无明显现象,灵敏电流计指针不发生偏转。
结论三:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请仔细观察下列五种装置的构造示意图,回答下列问题。
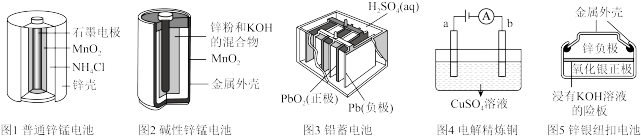
(1)碱性锌锰电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应为_______ 。
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素角度分析其原因:_______ 。
(3)图3中铅蓄电池放电过程中,H2SO4溶液浓度_______ (填“变大”“变小”或“不变”),充电时阴极的电极反应为_______ 。
(4)图4中电解精炼铜时,a极是_______ (填“纯铜”或“粗铜”)。锌银钮扣电池在工作过程中_______ (填物质名称)被还原。

(1)碱性锌锰电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应为
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素角度分析其原因:
(3)图3中铅蓄电池放电过程中,H2SO4溶液浓度
(4)图4中电解精炼铜时,a极是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】如图所示的原电池:当电解质溶液为稀H2SO4时,回答下列问题:
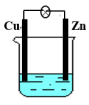
(1)Zn电极是___________ (填“正”或“负”)极,其电极反应为___________ ,该反应是___________ (填“氧化”或“还原”,下同)反应;
(2)Cu电极是___________ 极,其电极反应为___________ ,该反应是___________ 反应。
(3)装置中锌的作用是___________ ,稀硫酸的作用是___________
A.电极材料 B.电极反应物
C.电子导体 D.离子导体

(1)Zn电极是
(2)Cu电极是
(3)装置中锌的作用是
A.电极材料 B.电极反应物
C.电子导体 D.离子导体
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是______ (填字母代号),负极Zn发生了_____ 反应(填“氧化”或“还原”)。
(2)将纯锌片和纯铜片按如图所示方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是_______ (填字母代号)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲______ 乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的装置负极的电极反应式___________ 。
④当乙中产生1.12 L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为_______
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是
(2)将纯锌片和纯铜片按如图所示方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的装置负极的电极反应式
④当乙中产生1.12 L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】I.原电池是化学电源的雏形。
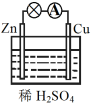
(1)如图连接好装置后,负极材料是_______ (填“Zn”或“Cu”)。
(2)相应原电池的总反应方程式为_______ 。
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是_______ (填序号)。
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2 2CO2 +3H2O
2CO2 +3H2O
II.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向_______ (填“Cu”或“X”)电极。
(5)若X为银,Y为硝酸银溶液,则X的电极方程式_______
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是_______ 。

(1)如图连接好装置后,负极材料是
(2)相应原电池的总反应方程式为
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2
 2CO2 +3H2O
2CO2 +3H2OII.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向
(5)若X为银,Y为硝酸银溶液,则X的电极方程式
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】化学能在一定条件下可转化为电能。
(1)如图所示装置中锌片是______ (填“正极”或“负极”),其电极反应式是______ 。溶液中H+移向______ (填“锌”或“石墨”)电极。

(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是______ (填序号)。
①2H2+O2=2H2O②HCl+NaOH=NaCl+H2O
(1)如图所示装置中锌片是

(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①2H2+O2=2H2O②HCl+NaOH=NaCl+H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某同学进行如下实验,研究化学反应中的能量变化。
I.化学能与热能
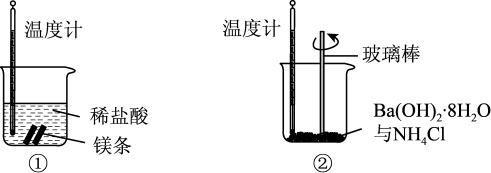
(1)反应后①中温度_______ ,②中温度_______ (填“升高”或“降低”)。由此判断①反应是_______ 反应(填“放热”或“吸热”),②中反应物总能量比生成物总能量_______ (填“高”或“低”)。
(2)②中反应的化学方程式是_______ 。
II.化学能与电能
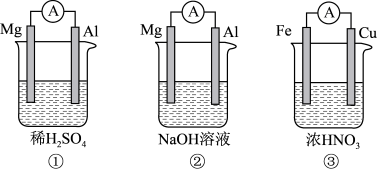
分析下图所示的四个原电池装置,回答问题
(3)①中负极材料是_______ ,正极反应式是_______ 。
(4)②中负极反应式是_______ 。
(5)③中Cu棒为_______ 极,正极反应式是_______ 。
I.化学能与热能

(1)反应后①中温度
(2)②中反应的化学方程式是
II.化学能与电能

分析下图所示的四个原电池装置,回答问题
(3)①中负极材料是
(4)②中负极反应式是
(5)③中Cu棒为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】被誉为改变未来世界的十大新科技之一的燃料电池。下图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。
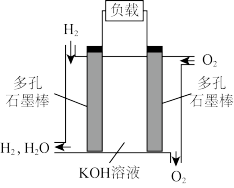
试回答下列问题:
(1)电解质溶液中的OH-移向______ 极(填“负”或“正”)。
(2)写出氢氧燃料电池工作时正极反应式:________ 。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为_______ 。
(4)利用该装置可以处理氮的氧化物和NH3尾气,总反应为6NO2+8NH3=7N2+12H2O,负极反应式为________ 。
(5)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+8OH--6e-= +6H2O。则下列说法正确的是
+6H2O。则下列说法正确的是______ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
(6)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:产生氢气的体积(标准状况)为________ 。

试回答下列问题:
(1)电解质溶液中的OH-移向
(2)写出氢氧燃料电池工作时正极反应式:
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为
(4)利用该装置可以处理氮的氧化物和NH3尾气,总反应为6NO2+8NH3=7N2+12H2O,负极反应式为
(5)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+8OH--6e-=
 +6H2O。则下列说法正确的是
+6H2O。则下列说法正确的是①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
(6)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:产生氢气的体积(标准状况)为
您最近一年使用:0次




