如图,根据图示回答:
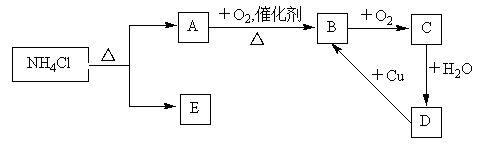
(1)A的分子式为___ ;B的分子式为___ ;C的分子式为___ 。
(2)将E溶于水,配制成0.1mol·L-1的溶液,滴入酚酞,显__ 色。
(3)写出NH4Cl溶液与NaOH溶液共热反应的离子方程式:__ 。
(4)D→B的化学方程式为___ 。

(1)A的分子式为
(2)将E溶于水,配制成0.1mol·L-1的溶液,滴入酚酞,显
(3)写出NH4Cl溶液与NaOH溶液共热反应的离子方程式:
(4)D→B的化学方程式为
更新时间:2021-05-19 18:48:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
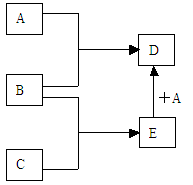
【推荐1】已知A、B、C、D、E均为常见物质,在一定条件下相互转化关系如下图所示(反应条件和部分产物已省略)。
请回答:
(1)若A为金属单质,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体,则B的化学式为______,A和E在一定条件下反应生成D的化学方程式为
___________ __。
(2)若A为非金属单质,且常温下为黄绿色气体,B为金属单质,C为不含氧元素的酸,且C的组成中含有与A相同的元素。则C的化学式为___________,A和E在一定条件下反应生成D的离子方程式 ____。

请回答:
(1)若A为金属单质,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体,则B的化学式为______,A和E在一定条件下反应生成D的化学方程式为
___________ __。
(2)若A为非金属单质,且常温下为黄绿色气体,B为金属单质,C为不含氧元素的酸,且C的组成中含有与A相同的元素。则C的化学式为___________,A和E在一定条件下反应生成D的离子方程式 ____。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
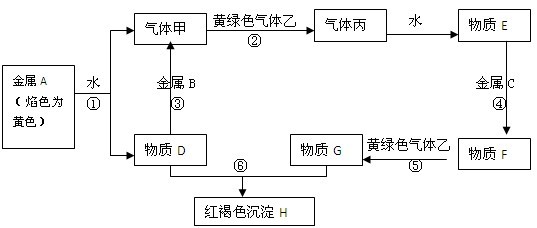
【推荐2】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:丙______________ G_____________
(2)写出下列反应的离子方程式:
反应①______________________________________________________________
反应⑤______________________________________________________________
(3)写出乙 + D的化学方程式________________________________________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:丙
(2)写出下列反应的离子方程式:
反应①
反应⑤
(3)写出乙 + D的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C为常见的单质,在一定条件下相互转化的关系如图:
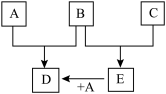
(1)若常温下,A、B均为气体,C为红色固体,E为黑色固体,则E的化学式为___________ ,写出A+E→D的化学反应方程式___________ 。
(2)若常温下B、C均为气体,A为金属单质,D为黑色晶体,则E的电子式为___________ ,写出A+E→D的化学反应方程式___________ 。
(3)若常温下B为气体,C为黑色固体,则构成金属A的原子结构示意图为___________ ,写出A+E→D的化学反应方程式___________ 。

(1)若常温下,A、B均为气体,C为红色固体,E为黑色固体,则E的化学式为
(2)若常温下B、C均为气体,A为金属单质,D为黑色晶体,则E的电子式为
(3)若常温下B为气体,C为黑色固体,则构成金属A的原子结构示意图为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某兴趣小组改进铜与浓硝酸反应的实验,并做进一步探究,实验装置如图。已知NaOH溶液不与NO反应,能与NO2和NO的混合气体或NO2反应。
ⅰ.按照上图组装实验仪器并添加试剂后,向下推动铜丝使其浸入到浓硝酸中,当气体充满装置时,停止反应;
ⅱ.用注射器取含紫色石蕊溶液的蒸馏水,逐滴滴入;
ⅲ.注入氧气至过量;
ⅳ.分别向试管1和试管2中注入适量的饱和氢氧化钠溶液。
回答下列问题:
(1)步骤(ⅰ)观察到的现象为____________ ,反应的离子方程式为____________ ,使反应停止的操作为______ 。
(2)步骤(ⅱ)加入含紫色石蕊溶液的蒸馏水后的现象为______ 。
(3)步骤(ⅲ)先注入少量氧气并观察现象,再注入过量氧气。依据观察到的现象,得出的结论为______ ,注入氧气过量的目的是______ 。
(4)步骤(ⅳ)注入饱和氢氧化钠溶液的目的是______ ,其中涉及的氧化还原反应的离子方程式为____________ 。

ⅰ.按照上图组装实验仪器并添加试剂后,向下推动铜丝使其浸入到浓硝酸中,当气体充满装置时,停止反应;
ⅱ.用注射器取含紫色石蕊溶液的蒸馏水,逐滴滴入;
ⅲ.注入氧气至过量;
ⅳ.分别向试管1和试管2中注入适量的饱和氢氧化钠溶液。
回答下列问题:
(1)步骤(ⅰ)观察到的现象为
(2)步骤(ⅱ)加入含紫色石蕊溶液的蒸馏水后的现象为
(3)步骤(ⅲ)先注入少量氧气并观察现象,再注入过量氧气。依据观察到的现象,得出的结论为
(4)步骤(ⅳ)注入饱和氢氧化钠溶液的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】利用下图装置,写出除去下列气体中的杂质的方法,并写出化学方程式(括号内的气体为杂质)。

(1)CO2(SO2):_______________ 化学方程式:___________________________ 。
(2)SO2(SO3)(假设SO3为气体):___________ 化学方程式:__________________
(3)NO(NO2):____________ 。化学方程式:____________________ 。

(1)CO2(SO2):
(2)SO2(SO3)(假设SO3为气体):
(3)NO(NO2):
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
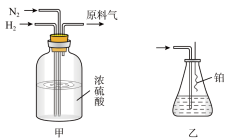
【推荐3】(一)实验室模拟合成氨和氨催化氧化的流程如下:
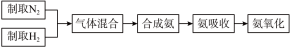
(1)N元素在周期表中位置_______________________ 。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合、干燥,还有______________ 作用。
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,锥形瓶中还可观察到的现象是_______________________________________ 。
(4)写出乙装置中氨氧化的化学方程式:__________________________________________ 。
(二)实验室探究铜与硝酸反应的相关问题,按下图所示装置进行实验。
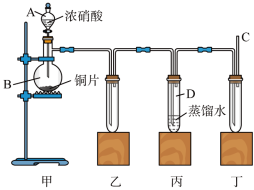
请回答下列问题:
(5)装置甲中盛放浓硝酸的仪器A的名称是_______________________ 。
(6)实验过程中,装置丙中出现的现象是:________________________________________ 。
(7)装置丙中的试管内发生反应的离子方程式为:__________________________________ 。
取下装置丙中的试管D,在其中滴加FeSO4溶液,再滴加KSCN溶液,溶液变为______________ 色。
(8)待反应停止后,Cu片有剩余,取下B,加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,离子方程式为________________________________________________________________ 。


(1)N元素在周期表中位置
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合、干燥,还有
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,锥形瓶中还可观察到的现象是
(4)写出乙装置中氨氧化的化学方程式:
(二)实验室探究铜与硝酸反应的相关问题,按下图所示装置进行实验。

请回答下列问题:
(5)装置甲中盛放浓硝酸的仪器A的名称是
(6)实验过程中,装置丙中出现的现象是:
(7)装置丙中的试管内发生反应的离子方程式为:
取下装置丙中的试管D,在其中滴加FeSO4溶液,再滴加KSCN溶液,溶液变为
(8)待反应停止后,Cu片有剩余,取下B,加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】工业上常用亚硝酸钠 作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备
作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备 并探究NO、
并探究NO、 的某一化学性质
的某一化学性质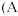 中加热装置已略去
中加热装置已略去 。请回答下列问题:
。请回答下列问题:

已知:①2NO+Na2O2=2NaNO2
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+
(1)装置A三颈烧瓶中发生反应的化学方程式为____________ 。
(2)用上图中的装置制备 ,其连接顺序为:
,其连接顺序为:
___ 
____ 
___ 
___ 
___ 
___  按气流方向,用小写字母表示
按气流方向,用小写字母表示 ,此时活塞
,此时活塞 、
、 如何操作
如何操作____________ 。
(3) 装置发生反应的离子方程式是
装置发生反应的离子方程式是________________ 。
(4)通过查阅资料, 或NO可能与溶液中
或NO可能与溶液中 发生反应。某同学选择上述装置并按
发生反应。某同学选择上述装置并按 顺序连接,E中装入
顺序连接,E中装入 溶液,进行如下实验探究。
溶液,进行如下实验探究。
步骤②操作的目的是___________ ;步骤③C瓶中发生的化学方程式为_________________ ;通过实验可以得出:___________  填“
填“ 、NO中的一种或两种”
、NO中的一种或两种” 和溶液中
和溶液中 发生反应使溶液呈深棕色。
发生反应使溶液呈深棕色。
 作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备
作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备 并探究NO、
并探究NO、 的某一化学性质
的某一化学性质 中加热装置已略去
中加热装置已略去 。请回答下列问题:
。请回答下列问题:
已知:①2NO+Na2O2=2NaNO2
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+
(1)装置A三颈烧瓶中发生反应的化学方程式为
(2)用上图中的装置制备
 ,其连接顺序为:
,其连接顺序为:





 按气流方向,用小写字母表示
按气流方向,用小写字母表示 ,此时活塞
,此时活塞 、
、 如何操作
如何操作(3)
 装置发生反应的离子方程式是
装置发生反应的离子方程式是(4)通过查阅资料,
 或NO可能与溶液中
或NO可能与溶液中 发生反应。某同学选择上述装置并按
发生反应。某同学选择上述装置并按 顺序连接,E中装入
顺序连接,E中装入 溶液,进行如下实验探究。
溶液,进行如下实验探究。 | 步骤 | 操作及现象 |
| ① | 关闭K2,打开K1,打开弹簧夹通一段时间的氮气,夹紧弹簧夹,开始A中反应,一段时间后,观察到E中溶液逐渐变为深棕色。 |
| ② | 停止A中反应,打开弹簧夹和K2、关闭K1,持续通入N2一段时间 |
| ③ | 更换新的E装置,再通一段时间N2后关闭弹簧夹,使A中反应继续,观察到的现象与步骤①中相同 |
步骤②操作的目的是
 填“
填“ 、NO中的一种或两种”
、NO中的一种或两种” 和溶液中
和溶液中 发生反应使溶液呈深棕色。
发生反应使溶液呈深棕色。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某溶液X中可能含有如下离子的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 (忽略水解和水的电离),已知:①溶液中每种离子的数目相等;②取少量X溶液加入足量盐酸,有气体Y产生,且反应前后阴离子种类没有变化;③继续向反应后的溶液中滴加少量氢氧化钡溶液,有白色沉淀生成,已知氧化性:HNO3>Fe3+>I2。回答下列问题:
(忽略水解和水的电离),已知:①溶液中每种离子的数目相等;②取少量X溶液加入足量盐酸,有气体Y产生,且反应前后阴离子种类没有变化;③继续向反应后的溶液中滴加少量氢氧化钡溶液,有白色沉淀生成,已知氧化性:HNO3>Fe3+>I2。回答下列问题:
(1)在溶液X中肯定存在的离子有___________ 。(可填“无”,下同)肯定不存在的离子有___________ ,可能存在的离子有___________ 。
(2)气体Y是___________ 。
a.CO2 b.NO c.NO2
(3)写出步骤②中发生的离子方程式:___________ 。
(4)写出步骤③中发生的离子方程式:___________ 。
(5)若要检验溶液中是否含有Cl-,具体操作是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 (忽略水解和水的电离),已知:①溶液中每种离子的数目相等;②取少量X溶液加入足量盐酸,有气体Y产生,且反应前后阴离子种类没有变化;③继续向反应后的溶液中滴加少量氢氧化钡溶液,有白色沉淀生成,已知氧化性:HNO3>Fe3+>I2。回答下列问题:
(忽略水解和水的电离),已知:①溶液中每种离子的数目相等;②取少量X溶液加入足量盐酸,有气体Y产生,且反应前后阴离子种类没有变化;③继续向反应后的溶液中滴加少量氢氧化钡溶液,有白色沉淀生成,已知氧化性:HNO3>Fe3+>I2。回答下列问题:(1)在溶液X中肯定存在的离子有
(2)气体Y是
a.CO2 b.NO c.NO2
(3)写出步骤②中发生的离子方程式:
(4)写出步骤③中发生的离子方程式:
(5)若要检验溶液中是否含有Cl-,具体操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学清洗银镜实验后试管内壁上的银并探究其中的反应原理,进行下列实验。
(1)用稀硝酸可以清洗试管内壁上的银,反应的化学方程式为____________________________ 。
(2)为消除(1)中所产生的污染问题,改为如下实验。
①该同学由现象推测H2O2将Ag氧化为Ag+,但通过实验排除了这种可能性。他的操作及现象是:取实验I所得液体于试管中,_________________________________ 。
②经查阅资料,发现:实验I中银镜溶解后经一系列反应,最后产物为Ag,但是因为颗粒很小(直径在1~100 nm间)分散在液体中,肉眼无法识别。该同学设计实验,证实了a中存在直径在1~100 nm间的颗粒。他的操作及现象是:_____________________________________ 。
③写出实验I的化学方程式:_________________________________________________ 。
(3)进一步探究银的化合物在H2O2分解反应中的作用,进行如下实验。
①实验II的目的是___________________________________________________ 。
根据实验Ⅲ的现象提出假设:
假设1:Ag2O在H2O2分解反应中作氧化剂;假设2:Ag2O在H2O2分解反应中作催化剂。
②若假设1成立,请写出该反应的化学方程式:________________________________ 。
③结合所给试剂,请设计一个简单的实验证明假设1,并将表格填写完整。
可选试剂:1 mol·L-1盐酸、0.1 mol·L-1氨水、1 mol·L-1 NaOH溶液
(1)用稀硝酸可以清洗试管内壁上的银,反应的化学方程式为
(2)为消除(1)中所产生的污染问题,改为如下实验。
| 实验编号 | 操 作 | 现 象 |
I | 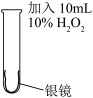 | 剧烈反应,有大量无色气体产生,该气体可以使带火星的木条复燃;反应停止后,试管内壁上的银全部溶解,得到澄清液体a。 |
②经查阅资料,发现:实验I中银镜溶解后经一系列反应,最后产物为Ag,但是因为颗粒很小(直径在1~100 nm间)分散在液体中,肉眼无法识别。该同学设计实验,证实了a中存在直径在1~100 nm间的颗粒。他的操作及现象是:
③写出实验I的化学方程式:
(3)进一步探究银的化合物在H2O2分解反应中的作用,进行如下实验。
| 实验编号 | 操 作 | 现 象 |
II | 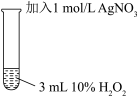 | 振荡,溶液无明显现象。 |
III |  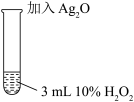 | 剧烈反应,产生大量无色气体,同时在试管底部仍有少量黑色固体。 |
根据实验Ⅲ的现象提出假设:
假设1:Ag2O在H2O2分解反应中作氧化剂;假设2:Ag2O在H2O2分解反应中作催化剂。
②若假设1成立,请写出该反应的化学方程式:
③结合所给试剂,请设计一个简单的实验证明假设1,并将表格填写完整。
可选试剂:1 mol·L-1盐酸、0.1 mol·L-1氨水、1 mol·L-1 NaOH溶液
| 实验步骤和操作 | 实验现象及结论 |
| 取3 mL 10% H2O2在试管中,加入少量Ag2O,充分反应后, |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:
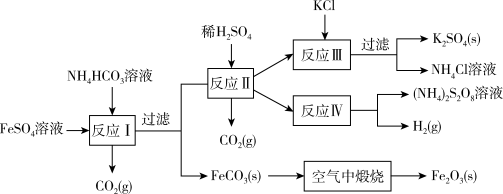
(1)反应Ⅰ前需在 溶液中加入___________(填字母),以除去溶液中的
溶液中加入___________(填字母),以除去溶液中的 ;
;
(2)反应Ⅰ需控制反应温度低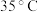 ,其目的是
,其目的是___________ 。
(3)反应Ⅳ常被用于电解生产 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为___________ 。
(4)反应Ⅰ的离子方程式为___________ 。
(5)空气中煅烧的化学方程式为___________ 。

(1)反应Ⅰ前需在
 溶液中加入___________(填字母),以除去溶液中的
溶液中加入___________(填字母),以除去溶液中的 ;
;| A.锌粉 | B.铁屑 | C. 溶液 溶液 | D. |
(2)反应Ⅰ需控制反应温度低
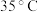 ,其目的是
,其目的是(3)反应Ⅳ常被用于电解生产
 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为(4)反应Ⅰ的离子方程式为
(5)空气中煅烧的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X和H是固体,B和G是液体,其余均为气体,1molX受热分解得到A、B、C各1mol。试回答下列问题:

(1)写出下列物质的化学式:X___________ ,B___________ 。
(2)实验室收集气体E和F的方法依次是___________ 法、___________ 法。
(3)写出下列反应的化学方程式:
C+D→E:___________ 。
F+B→G:___________ 。
G+H→A+F:___________ 。
(4)若Na2O2与A充分反应,生成标准状况下22.4L气体D,则该反应转移的电子数目为___________ 。
(5)检验X固体所含阳离子的实验方法:___________

(1)写出下列物质的化学式:X
(2)实验室收集气体E和F的方法依次是
(3)写出下列反应的化学方程式:
C+D→E:
F+B→G:
G+H→A+F:
(4)若Na2O2与A充分反应,生成标准状况下22.4L气体D,则该反应转移的电子数目为
(5)检验X固体所含阳离子的实验方法:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】已知 、
、 、
、 、
、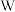 为原子序数依次增大的前四周期元素,其中
为原子序数依次增大的前四周期元素,其中 元素的单质是密度最小的气体,
元素的单质是密度最小的气体, 、
、 元素的单质都是空气的主要成分,
元素的单质都是空气的主要成分,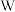 的
的 层为1个电子,其内层电子全充满。由上述四种元素组成的化合物在沸石笼作为载体时的反应历程如图所示:
层为1个电子,其内层电子全充满。由上述四种元素组成的化合物在沸石笼作为载体时的反应历程如图所示:

回答下列问题:
(1)上述反应历程中I→II进行很快的原因是___________ 。
(2)某 、
、 、
、 组成的化合物
组成的化合物 在加热的条件下分解只生成
在加热的条件下分解只生成 和
和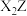 ,该化合物的化学式是
,该化合物的化学式是___________ 。
(3)工业上用惰性电极电解某 、
、 、
、 组成的化合物
组成的化合物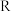 制备相应的强酸溶液和碱溶液,其工作原理如图所示:
制备相应的强酸溶液和碱溶液,其工作原理如图所示:

①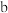 极为
极为___________ (填“阴”或“阳”,下同)极, 膜为
膜为___________ 离子交换膜。
②制得酸的化学式是___________ 。
③电解时阴极的电极反应式为___________ ;生成碱溶液的离子方程式是___________ 。
 、
、 、
、 、
、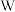 为原子序数依次增大的前四周期元素,其中
为原子序数依次增大的前四周期元素,其中 元素的单质是密度最小的气体,
元素的单质是密度最小的气体, 、
、 元素的单质都是空气的主要成分,
元素的单质都是空气的主要成分,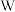 的
的 层为1个电子,其内层电子全充满。由上述四种元素组成的化合物在沸石笼作为载体时的反应历程如图所示:
层为1个电子,其内层电子全充满。由上述四种元素组成的化合物在沸石笼作为载体时的反应历程如图所示:
回答下列问题:
(1)上述反应历程中I→II进行很快的原因是
(2)某
 、
、 、
、 组成的化合物
组成的化合物 在加热的条件下分解只生成
在加热的条件下分解只生成 和
和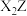 ,该化合物的化学式是
,该化合物的化学式是(3)工业上用惰性电极电解某
 、
、 、
、 组成的化合物
组成的化合物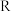 制备相应的强酸溶液和碱溶液,其工作原理如图所示:
制备相应的强酸溶液和碱溶液,其工作原理如图所示:
①
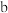 极为
极为 膜为
膜为②制得酸的化学式是
③电解时阴极的电极反应式为
您最近一年使用:0次



