如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。

(1)代表金刚石的是___ (填编号字母,下同),其中每个碳原子与___ 个碳原子最接近且距离相等。金刚石属于___ 晶体。
(2)代表石墨的是___ ,其中每个正六边形占有的碳原子数平均为___ 个。
(3)代表NaCl的是___ ,每个Na+周围与它最接近且距离相等的Na+有___ 个。
(4)代表CsCl的是___ ,它属于___ 晶体,每个Cs+与___ 个Cl-紧邻。
(5)代表干冰的是___ ,它属于___ 晶体,每个CO2分子与___ 个CO2分子紧邻。
(6)若说“离子晶体中只有离子键,分子晶体中没有化学键”是否正确,简述理由:___ 。
(7)NaCl晶体、HCl晶体、干冰、金刚石的熔点由高到低的顺序是___ ;其中在熔融或液态时能导电的电解质是___ ,液态不导电但为电解质的是___ ,在水溶液中能导电的非电解质是___ 。


(1)代表金刚石的是
(2)代表石墨的是
(3)代表NaCl的是
(4)代表CsCl的是
(5)代表干冰的是
(6)若说“离子晶体中只有离子键,分子晶体中没有化学键”是否正确,简述理由:
(7)NaCl晶体、HCl晶体、干冰、金刚石的熔点由高到低的顺序是
20-21高二下·河南开封·期中 查看更多[2]
更新时间:2021-05-19 18:08:38
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】四种晶体的比较
| 晶体 | 分子晶体 | 离子晶体 | 金属晶体 | 共价晶体 | |
| 构成微粒 | 金属离子、自由电子 | ||||
| 微粒间作用力 | 范德华力(少数有氢键) | 离子键 | 金属键 | 共价键 | |
| 性质 | 熔、沸点 | 较低 | 较高 | 一般较高 | 很高 |
| 硬度 | 小 | 略硬而脆 | 一般较大 | 很大 | |
| 溶解性 | 相似相溶 | 多数溶于水 | 不溶,有些与水反应 | 不溶 | |
| 机械加工性能 | 不良 | 不良 | 良好 | 不良 | |
| 导电性 | 固态、液态均不导电,部分溶于水时导电 | 固态时不导电,熔融时导电,能溶于水的溶于水时导电 | 固态、熔融态时导电 | 大部分固态、熔融时都不导电 | |
| 作用力大小规律 | 组成和结构相似的分子,相对分子质量大的范德华力大 | 离子所带电荷数多、半径小的离子键强 | 金属原子的价电子数多、半径小的金属离子与自由电子间的作用力强 | 共价键键长短(电子云重叠多)、原子半径小的共价键稳定 | |
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】常见的典型分子晶体
(1)所有_____________ :如H2O、H2S、NH3、CH4、HX(卤化氢)等。
(2)部分_____________ :如X2(卤素单质)、O2、H2、S8、P4、C60、稀有气体等。
(3)部分_____________ :如CO2、SO2、NO2、P4O6、P4O10等。
(4)几乎所有的_____________ :如H2SO4、HNO3、H3PO4、H2SiO3等。
(5)绝大多数_____________ :如苯、四氯化碳、乙醇、冰醋酸、蔗糖等。
(1)所有
(2)部分
(3)部分
(4)几乎所有的
(5)绝大多数
您最近半年使用:0次
【推荐1】GaAs的熔点为1 238 ℃,密度为ρ g·cm-3,其晶胞结构如图所示。该晶体的类型为___________ ,Ga与As以___________ 键键合。Ga和As的摩尔质量分别为MGa g·mol-1和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为___________ 。
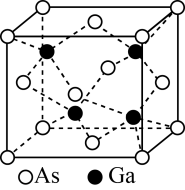

您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)离子化合物MgO2可被用于治疗消化道疾病,各原子均满足8电子稳定结构。写出MgO2的电子式___ 。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是___ 。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】二氧化硅晶体
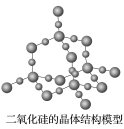
(1)二氧化硅晶体中,每个硅原子均以4个_____________ 对称地与相邻的_____________ 个氧原子相结合,每个氧原子与_____________ 个硅原子相结合,向空间扩展,形成三维骨架结构。晶体结构中最小的环上有_____________ 个硅原子和_____________ 个氧原子,硅、氧原子个数比为_____________ 。
(2)低温石英的结构中有顶角相连的_____________ 形成螺旋上升的长链,而没有封闭的_____________ 。这一结构决定了它具有_____________ 。

(1)二氧化硅晶体中,每个硅原子均以4个
(2)低温石英的结构中有顶角相连的
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】CaF2、CaCl2晶体的熔点依次为1402℃、782℃,二者熔点相差较大的主要原因是_____________ 。
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】四种晶体的比较
| 晶体 | 分子晶体 | 离子晶体 | 金属晶体 | 共价晶体 | |
| 构成微粒 | 金属离子、自由电子 | ||||
| 微粒间作用力 | 范德华力(少数有氢键) | 离子键 | 金属键 | 共价键 | |
| 性质 | 熔、沸点 | 较低 | 较高 | 一般较高 | 很高 |
| 硬度 | 小 | 略硬而脆 | 一般较大 | 很大 | |
| 溶解性 | 相似相溶 | 多数溶于水 | 不溶,有些与水反应 | 不溶 | |
| 机械加工性能 | 不良 | 不良 | 良好 | 不良 | |
| 导电性 | 固态、液态均不导电,部分溶于水时导电 | 固态时不导电,熔融时导电,能溶于水的溶于水时导电 | 固态、熔融态时导电 | 大部分固态、熔融时都不导电 | |
| 作用力大小规律 | 组成和结构相似的分子,相对分子质量大的范德华力大 | 离子所带电荷数多、半径小的离子键强 | 金属原子的价电子数多、半径小的金属离子与自由电子间的作用力强 | 共价键键长短(电子云重叠多)、原子半径小的共价键稳定 | |
您最近半年使用:0次
【推荐3】如图所示,直线交点处的圆圈为NaCl晶体中Na+或Cl-所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。
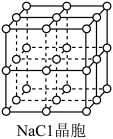
(1)在晶体中,每个Na+的周围与它最接近且距离相等的Na+共有___ 个。
(2)晶体中每一个重复的结构单元叫晶胞。在NaCl晶胞中正六面体的顶角上、面上、棱上的Na+或Cl-为该晶胞与其相邻的晶胞所共有,一个晶胞中Cl-的个数等于___ ,即___ (填计算式);Na+的个数等于___ ,即____ (填计算式)。

(1)在晶体中,每个Na+的周围与它最接近且距离相等的Na+共有
(2)晶体中每一个重复的结构单元叫晶胞。在NaCl晶胞中正六面体的顶角上、面上、棱上的Na+或Cl-为该晶胞与其相邻的晶胞所共有,一个晶胞中Cl-的个数等于
您最近半年使用:0次



