酞菁钴近年来被广泛应用于光电材料、非线性光学材料、催化剂等方面。酞菁钴的熔点约为163℃,其结构如图所示(部分化学键未画明)。下列说法正确的是
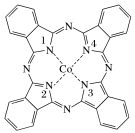

| A.酞菁钴中三种非金属元素的电负性大小顺序为N>H>C |
| B.酞菁钴中碳原子的杂化方式有sp2杂化和sp3杂化两种 |
| C.与Co离子通过配位键结合的是2号和4号N原子 |
| D.酞菁钴一定是离子晶体 |
更新时间:2021-05-23 15:45:29
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】由下列实验操作及现象能得出相应结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向氢氧化钠的乙醇溶液中加入1—溴丁烷,在一定条件下发生反应。将产生的气体通入 溶液中 溶液中 |  溶液褪色 溶液褪色 | 证明产生的气体中含有1—丁烯 |
| B | 在物质X柱面上滴一滴熔化的石蜡,用一根红热的铁针刺中凝固的石蜡 | 石蜡熔化呈椭圆形 | 说明物质X为非晶体 |
| C | 将 溶液加热 溶液加热 | 溶液变为黄色 | 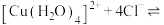 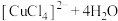 ,正反应方向为放热反应 ,正反应方向为放热反应 |
| D | 向盛有KI溶液的试管中加入少量氯水 | 溶液变为黄色 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某学习小组以铝铁铜合金为主要原料制备[Cu(NH3)4]SO4•H2O(一水硫酸四氨合铜),具体流程如图:下列说法不正确的是


| A.步骤I中加入(NH4)2SO4的作用之一是抑制NH3•H2O的电离,提高[Cu(NH3)4]2+的产率 |
B.步骤I发生的总离子反应为:Cu+2NH3•H2O+2NH +H2O2=[Cu(NH3)4]2++4H2O +H2O2=[Cu(NH3)4]2++4H2O |
| C.步骤Ⅱ中加入乙醇的速度过快,有利于得到较大颗粒的晶体 |
| D.步骤Ⅱ若改为蒸发浓缩、冷却结晶,得到的一水硫酸四氨合铜晶体会含有较多Cu(OH)2等杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液;在深蓝色溶液中加入等体积的95%乙醇,深蓝色溶液变浑浊,静置后有深蓝色晶体析出。下列对此现象说法正确的是
| A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键 |
| B.[Cu(NH3)4]2+的空间构型为平面正方形,中心离子Cu2+采用sp3杂化 |
| C.[Cu(NH3)4]SO4会与乙醇发生反应生成深蓝色晶体 |
| D.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有NH3分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氮及其化合物在生产生活中具有广泛应用。氮气经过一系列的变化可以合成氨、氮的氧化物、硝酸等重要的化工原料;NO能被 溶液吸收生成配合物
溶液吸收生成配合物 ,减少环境污染。下列说法正确的是
,减少环境污染。下列说法正确的是
 溶液吸收生成配合物
溶液吸收生成配合物 ,减少环境污染。下列说法正确的是
,减少环境污染。下列说法正确的是| A.该配合物中所含非金属元素均位于元素周期表的p区 |
B. 提供孤电子对用于形成配位键 提供孤电子对用于形成配位键 |
| C.该配合物中阴离子空间结构为正四面体形 |
D.配离子为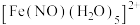 ,中心离子的配位数为5 ,中心离子的配位数为5 |
您最近一年使用:0次


 作催化剂,虚线框内物质是中间体
作催化剂,虚线框内物质是中间体


