如图是元素周期表的一部分,主族元素A、B、C、D、E在元素周期表中的位置如图,A元素的单质在空气中含量最高(请用相应的元素符号或化学式作答)∶
(1)A简单离子结构示意图_______
(2)下列说法不正确的是_______
A.C的最高价氧化物能溶于B的氢化物水溶液
B.元素A、E的气态氢化物相遇会产生白烟
C.B元素形成的其中一种18电子分子,能与A元素形成的一种10电子分子发生氧化还原反应
D.原子得电子能力∶D>E>A
(3)C、D、B氢化物的稳定性大小为_______ ,A和D氢化物沸点的大小为_______ 。
(4)设计实验比较D与E的非金属性强(用离子方程式表示)_______ 。
(5)A2的结构式_____ ,CB4的电子式为____ ,CB4溶于NaOH溶液的化学方程式____ 。
(6)E单质通入足量Na2CO3溶液发生反应的化学方程式_______ 。
| A | B | ||
| C | D | E |
(1)A简单离子结构示意图
(2)下列说法不正确的是
A.C的最高价氧化物能溶于B的氢化物水溶液
B.元素A、E的气态氢化物相遇会产生白烟
C.B元素形成的其中一种18电子分子,能与A元素形成的一种10电子分子发生氧化还原反应
D.原子得电子能力∶D>E>A
(3)C、D、B氢化物的稳定性大小为
(4)设计实验比较D与E的非金属性强(用离子方程式表示)
(5)A2的结构式
(6)E单质通入足量Na2CO3溶液发生反应的化学方程式
更新时间:2021-06-17 10:03:12
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氮元素是空气中含量最多的元素,在自然界中的分布十分广泛,在生物体内亦有极大作用。一定条件下,含氮元素的物质可发生如图所示的循环转化。回答下列问题:
(1)氮分子的电子式为______________________ 。
(2)图中属于“氮的固定”的是___________ (填字母)。
(3)已知NH4Cl溶液呈酸性,用离子方程式解释原因___________________________________________ 。
(4)用离子方程式举一例表示循环中发生非氧化还原反应的过程__________________ 。
(5)若反应h是在NO2与H2O的作用下实现,则该反应中氧化剂与还原剂物质的量之比为____________ 。
(6)若反应i是在酸性条件下由NO3—与Fe2+的作用实现,则该反应的离子方程式为_______________ 。

(1)氮分子的电子式为
(2)图中属于“氮的固定”的是
(3)已知NH4Cl溶液呈酸性,用离子方程式解释原因
(4)用离子方程式举一例表示循环中发生非氧化还原反应的过程
(5)若反应h是在NO2与H2O的作用下实现,则该反应中氧化剂与还原剂物质的量之比为
(6)若反应i是在酸性条件下由NO3—与Fe2+的作用实现,则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求作答
(1)写出下列微粒的电子式
Na+:_______ S2-:_______ NH3:_______ Na2O2:_______ HClO:_______
(2)用电子式表示下列化合物的形成过程
NaBr:_______ ;HF:_______ 。
(3)同主族从上到下:原子半径逐渐_______ (填“增大”或“减小”);金属性逐渐_______ (填“增强”或“减弱”,下同);最高价氧化物对应水化物碱性_______ 。同周期从左到右:原子半径逐渐_______ (填“增大”或“减小”);非属性逐渐_______ (填“增强”或“减弱”,下同);最高价氧化物对应水化物酸性_______ ;简单氢化物稳定性逐渐_______ 。
(1)写出下列微粒的电子式
Na+:
(2)用电子式表示下列化合物的形成过程
NaBr:
(3)同主族从上到下:原子半径逐渐
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学物质丰富多彩,在生产、生活、科研等方面都起着重要的作用。
(1) 的电子式为
的电子式为___________ 。
(2)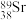 与
与 二者互为
二者互为___________ ;食盐不慎洒落在天然气的火焰上,观察的现象是___________ 。
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是___________ 。
(4)小苏打可用于烘焙糕点,在烘焙受热过程中涉及的化学方程式是___________ 。
(5)家庭厨卫管道常因留有菜渣、毛发而造成堵塞,可用管道疏通剂疏通。常用的管道疏通剂主要成分有铝粉和氢氧化钠,请用离子方程式表达其疏通原理:___________ 。
(6)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅。请写出化学方程式:___________ 。
(1)
 的电子式为
的电子式为(2)
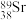 与
与 二者互为
二者互为(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
(4)小苏打可用于烘焙糕点,在烘焙受热过程中涉及的化学方程式是
(5)家庭厨卫管道常因留有菜渣、毛发而造成堵塞,可用管道疏通剂疏通。常用的管道疏通剂主要成分有铝粉和氢氧化钠,请用离子方程式表达其疏通原理:
(6)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅。请写出化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氯气是一种非常重要的化工原料,可用于制造盐酸、漂白剂、农药等,但氯气有毒,使用或接触到有关物质时应注意安全。请回答下列问题:
(1)新制氯水中,含有氯元素的微粒有___________ (填微粒符号,下同,不考虑水中杂质与氯气的反应),其中使新制氯水显淡黄绿色的微粒是___________ 。
(2) 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为___________ L。
(3)标准状况下,氯气的密度为___________ 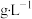 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是___________ (填序号)。
a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为___________ ;通常不用澄清石灰水吸收氯气的原因是___________ 。
(1)新制氯水中,含有氯元素的微粒有
(2)
 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为(3)标准状况下,氯气的密度为
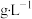 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】“84”消毒液是一种常见的含氯消毒剂。
(1)“84”消毒液的有效成分为_______ (用化学式表示)。
(2)常温下,将氯气通入NaOH溶液中可制得“84”消毒液。写出反应的离子方程式:_______ 。
(3)针对不同物品消毒,“84”消毒液需要稀释到不同浓度使用。取含次氯酸钠0.2mol·L-1的“84”消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为_______  。
。
(1)“84”消毒液的有效成分为
(2)常温下,将氯气通入NaOH溶液中可制得“84”消毒液。写出反应的离子方程式:
(3)针对不同物品消毒,“84”消毒液需要稀释到不同浓度使用。取含次氯酸钠0.2mol·L-1的“84”消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】常温下将Cl2缓慢通入水中至饱和,然后改向其中滴加浓NaOH溶液至恰好完全反应。上述整个实验过程中溶液的pH变化曲线如图所示(不考虑次氯酸的分解以及溶液体积的变化)。
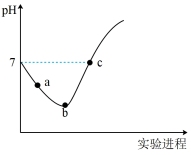
①请对图中pH的整个变化趋势作出解释(用离子方程式表示)________ 。
②写出b点对应溶液中的电荷守恒式___________ 。并且比较c(HClO) :a点___________ b点;c(Cl–):b点___________ c点(填>、<或=)
③Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为___________ 。
④ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1mol ClO2消耗NaClO2的量为______ mol; 产生“气泡”的化学方程式为____ 。
⑤“84消毒液“的有效成分为NaClO,不可与酸性清洁剂混用的原因是___________ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为 ___________ kg(保留整数)。

①请对图中pH的整个变化趋势作出解释(用离子方程式表示)
②写出b点对应溶液中的电荷守恒式
③Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
④ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1mol ClO2消耗NaClO2的量为
⑤“84消毒液“的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,用化学用语回答下列问题:
(1)⑧的原子结构示意图为________________________________ 。
(2)②和③气态氢化物稳定性的大小顺序:___________ (填化学式)。
(3)③⑧⑩的最高价含氧酸的酸性最强的是__________ (填化学式)。
(4)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是________ (填化学式),它属于________ (填“共价化合物”或“离子化合物”)。
(5)①④⑩三种元素的原子能形成原子数目比为1∶1∶1的共价化合物,它的电子式为________ 。
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是________ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸碱性
D.比较这两种元素单质与酸或碱反应的难易性
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑧的原子结构示意图为
(2)②和③气态氢化物稳定性的大小顺序:
(3)③⑧⑩的最高价含氧酸的酸性最强的是
(4)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是
(5)①④⑩三种元素的原子能形成原子数目比为1∶1∶1的共价化合物,它的电子式为
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物对应水化物的酸碱性
D.比较这两种元素单质与酸或碱反应的难易性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知X、Y为短周期元素,请按要求回答下列问题:
(1)若 X、Y 能形成 XY 型的离子化合物,且 X、Y 不在同一主族,则 X、Y 所在的族分别 为__________ 。
(2)若 X、Y 能形成 XY2 型的离子化合物,则 X 所在的族为__________________ ,Y 所在的族为___________ 。
(1)若 X、Y 能形成 XY 型的离子化合物,且 X、Y 不在同一主族,则 X、Y 所在的族分别 为
(2)若 X、Y 能形成 XY2 型的离子化合物,则 X 所在的族为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。

(1)④是___________ (用元素符号表示)。
(2)①、③、④元素中的两种元素可形成含10个电子的分子,请写出其中一种10个电子的分子的化学式___________ 。
(3)画出⑤的原子结构示意图:___________ 。
(4)⑧的单质与氢氧化钠溶液反应的离子方程式为___________ 。
Ⅱ.据《中国质量报》报道,我国首次将星载铷(Rb)钟应用于海洋二号卫星,已知 (铷)的原子序数为37。回答下列有关铷的问题:
(铷)的原子序数为37。回答下列有关铷的问题:
(1) Rb在元素周期表中的位置是___________ 。
(2)取少量铷单质加入水中,发生反应的离子方程式___________ 。

(1)④是
(2)①、③、④元素中的两种元素可形成含10个电子的分子,请写出其中一种10个电子的分子的化学式
(3)画出⑤的原子结构示意图:
(4)⑧的单质与氢氧化钠溶液反应的离子方程式为
Ⅱ.据《中国质量报》报道,我国首次将星载铷(Rb)钟应用于海洋二号卫星,已知
 (铷)的原子序数为37。回答下列有关铷的问题:
(铷)的原子序数为37。回答下列有关铷的问题:(1) Rb在元素周期表中的位置是
(2)取少量铷单质加入水中,发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】粉煤灰是燃煤电厂的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为38%,还有含量较多的SiO2。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4,有关化学反应方程式如下:Al6Si2O13+3Na2CO3→2NaAlSiO4+4NaAlO2+3CO2↑
结合上述反应完成下列填空:
(1)上述反应所涉及的元素中,原子核外电子运动状态最多的元素在周期表中的位置是___ ,其氧化物属于___ 晶体。
(2)上述元素中有三种元素在元素周期表中处于相邻位置,其原子半径从大到小的顺序为___ >___ >___ (用元素符号表示)。
(3)二氧化碳分子的空间构型为___ 型,碳酸钠溶液显碱性的原因是(用离子方程式表示)___ 。
(4)上述元素中有两种元素是同一主族,可以作为判断两者非金属性强弱的依据的是___ (填编号)。
a.该两种原子形成的共价键中共用电子对的偏向
b.最高价氧化物熔沸点高低
c.最高价氧化物对应水化物的酸性强弱
d.单质与酸反应的难易程度
结合上述反应完成下列填空:
(1)上述反应所涉及的元素中,原子核外电子运动状态最多的元素在周期表中的位置是
(2)上述元素中有三种元素在元素周期表中处于相邻位置,其原子半径从大到小的顺序为
(3)二氧化碳分子的空间构型为
(4)上述元素中有两种元素是同一主族,可以作为判断两者非金属性强弱的依据的是
a.该两种原子形成的共价键中共用电子对的偏向
b.最高价氧化物熔沸点高低
c.最高价氧化物对应水化物的酸性强弱
d.单质与酸反应的难易程度
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
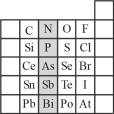
(1)阴影部分元素N在元素周期表中的位置为_____ 。根据元素周期律,预测酸性强弱:H3AsO4______ H3PO4(填“>”或“<”)。
(2)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度___ (填“更大”“更小”或“相同”)。
(3)下列说法错误的是______ (填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③干冰升华、液态水转变为气态水都要克服分子内的共价键
④HF、HCl、HBr、HI的热稳定性依次减弱

(1)阴影部分元素N在元素周期表中的位置为
(2)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度
(3)下列说法错误的是
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③干冰升华、液态水转变为气态水都要克服分子内的共价键
④HF、HCl、HBr、HI的热稳定性依次减弱
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】黑火药是中国四大发明之一,它爆炸时的反应为:2KNO3+ 3C + S A+ N2↑+3CO2↑(已配平)
A+ N2↑+3CO2↑(已配平)
(1)生成物中含极性键的非极性分子的电子式为_________ ,物质A属于_________ 晶体。
(2)黑火药中位于短周期的元素有_____ 种。其中有一种元素,其氧化物是造成酸雨的主要原因,该元素在周期表中的位置是________________ ,该元素氢化物的水溶液的电离方程式是_________________________________ 。
(3)黑火药所含元素中原子半径从大到小的顺序是__________________ (用元素符号表示)。
(4)下列能说明黑火药中碳与硫元素非金属性相对强弱的有( )
a.加热分解温度:CH4>H2S
b.相同条件下水溶液的pH:Na2CO3> Na2SO4
c.相同条件下酸性:H2SO3> H2CO3
d.硫与碳化合生成的CS2中碳元素为+4价,硫元素为-2价
 A+ N2↑+3CO2↑(已配平)
A+ N2↑+3CO2↑(已配平)(1)生成物中含极性键的非极性分子的电子式为
(2)黑火药中位于短周期的元素有
(3)黑火药所含元素中原子半径从大到小的顺序是
(4)下列能说明黑火药中碳与硫元素非金属性相对强弱的有
a.加热分解温度:CH4>H2S
b.相同条件下水溶液的pH:Na2CO3> Na2SO4
c.相同条件下酸性:H2SO3> H2CO3
d.硫与碳化合生成的CS2中碳元素为+4价,硫元素为-2价
您最近一年使用:0次



