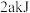科学家在研究碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中需要经过一个高能量的过渡态。NO2和CO反应生成CO2和NO的过程中的能量变化如图,下列说法正确的是

| A.NO2和CO反应生成CO2和NO的反应为吸热反应 |
| B.NO2和CO的总能量小于CO2和NO的总能量 |
| C.由NO2和CO到过渡态是一个吸热过程 |
| D.该反应中断键吸收的热量总和大于成键放出的热量总和 |
更新时间:2021-06-20 08:30:00
|
相似题推荐
单选题
|
适中
(0.64)
【推荐1】已知热化学方程式(Q1、Q2均为正值):
C(s)+ O2(g) =CO(g) ΔH=-Q1 kJ·mol-1,C(s)+O2(g) =CO2(g) ΔH=-Q2 kJ·mol-1,
O2(g) =CO(g) ΔH=-Q1 kJ·mol-1,C(s)+O2(g) =CO2(g) ΔH=-Q2 kJ·mol-1,
有关上述反应的叙述错误的是
C(s)+
 O2(g) =CO(g) ΔH=-Q1 kJ·mol-1,C(s)+O2(g) =CO2(g) ΔH=-Q2 kJ·mol-1,
O2(g) =CO(g) ΔH=-Q1 kJ·mol-1,C(s)+O2(g) =CO2(g) ΔH=-Q2 kJ·mol-1,有关上述反应的叙述错误的是
| A.Q1<Q2 |
| B.生成物总能量均高于反应物总能量 |
| C.由1 mol C反应生成1 mol CO气体时放出Q1 kJ的热量 |
| D.1 mol CO2气体具有的能量大于1 mol干冰具有的能量 |
您最近一年使用:0次
【推荐2】下列反应属于非氧化还原反应,且能量变化与图示能量相符合的是

A. 与稀 与稀 反应 反应 | B.氢气与氮气的化合反应 |
C.灼热的炭与 反应 反应 | D.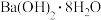 晶体与 晶体与 晶体反应 晶体反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知工业合成氨反应:N2(g)+3H2(g)  2NH3(g) △H= —Q1 kJ/mol (Q1>0),下列有关说法错误的是
2NH3(g) △H= —Q1 kJ/mol (Q1>0),下列有关说法错误的是
 2NH3(g) △H= —Q1 kJ/mol (Q1>0),下列有关说法错误的是
2NH3(g) △H= —Q1 kJ/mol (Q1>0),下列有关说法错误的是| A.1 mol N2和3 mol H2的总键能小于2 mol NH3的总键能 |
| B.1 mol N2(g)和3 mol H2(g)的总能量大于2 mol NH3(g)的总能量 |
| C.使用铁触媒作为催化剂将使反应速率加快,Q1减小 |
D.若 N2(g)+ N2(g)+  H2(g) H2(g)  NH3(l) △H = - Q2 kJ/mol(Q2>0),则Q2> NH3(l) △H = - Q2 kJ/mol(Q2>0),则Q2>  Q1 Q1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某科研小组尝试利用固体表面催化工艺用 制取乙炔(
制取乙炔( ),用下图表示反应可能的微观历程。
),用下图表示反应可能的微观历程。
 制取乙炔(
制取乙炔( ),用下图表示反应可能的微观历程。
),用下图表示反应可能的微观历程。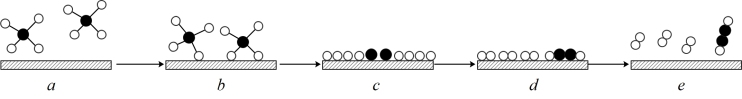
A. 过程中有非极性键的断裂 过程中有非极性键的断裂 |
| B.b、c、d中,c的能量最低 |
| C.反应过程中碳元素化合价发生变化 |
| D.上述反应原子利用率为100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理如图所示。下列关于该过程的说法不正确的是


| A.氧化剂和还原剂的物质的量之比为3:1 |
| B.该过程属于氮的固定 |
| C.工业中,氮气经过一系列反应可以制得硝酸 |
| D.该过程涉及极性键和非极性键的断裂和形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】高浓度的地面臭氧对生态系统和人类健康带来严重的危害。华东师大郭彦炳课题组在地面臭氧的去除研究方面取得了新的进展。该研究表明,高湿条件下,臭氧在氧化钼/石墨炔(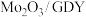 )表面具有优异的分解性能,该研究中臭氧分解的反应机理如图所示。
)表面具有优异的分解性能,该研究中臭氧分解的反应机理如图所示。
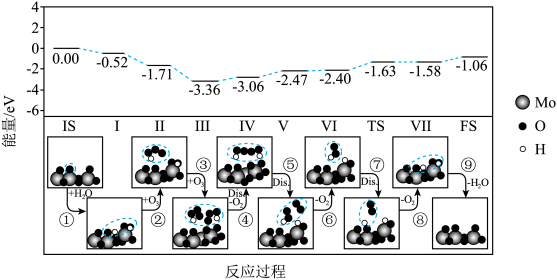
下列说法错误的是
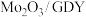 )表面具有优异的分解性能,该研究中臭氧分解的反应机理如图所示。
)表面具有优异的分解性能,该研究中臭氧分解的反应机理如图所示。
下列说法错误的是
A.  | B.该过程的决速步为步骤③ |
| C.步骤②③中均存在O-H键的断裂和形成 | D.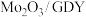 可以加快臭氧的分解速率 可以加快臭氧的分解速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
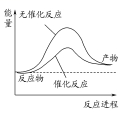

| A.上图可表示水分解过程中的能量变化 |
| B.若2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D.已知Ⅰ:反应H2(g)+Cl2(g)===2HCl(g) ΔH=-a kJ/mol Ⅱ:  且a、b、c均大于零,则断开1 mol H—Cl键所需的能量为(a+b+c)kJ/mol |
您最近一年使用:0次

 2HI(g),1molH2完全反应放出akJ热量.已知:
2HI(g),1molH2完全反应放出akJ热量.已知: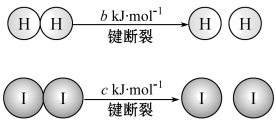 (a、b、c均大于零)
(a、b、c均大于零)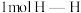 键和
键和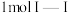 键所需能量大于断开
键所需能量大于断开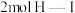 键所需能量
键所需能量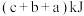
 和
和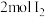 ,充分反应放出的热量小于
,充分反应放出的热量小于