两组同学对铁及其化合物的性质进行探究。
(1)一组同学用图1所示装置对铁与浓硫酸的反应进行实验。已知:2Fe + 6H2SO4(浓) Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
①检查装置气密性后,将过量的铁屑和一定量的浓硫酸放入烧瓶,塞紧橡皮塞,开始计时。t1时开始加热,在铁屑表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变。甲同学将收集到的气体体积与时间的关系粗略地表示为图2。
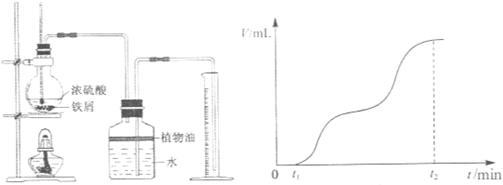
图1 图2
在0~t1时间段,铁屑表面没有气泡生成,说明铁在浓硫酸中发生了______ ;t1~t2时间段,反应生成的气体是______ 。
②t2时,取少量反应液,先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现红色褪去。同学们对红色褪去的原因提出各自的假设。乙同学的假设是:溶液中的+3价铁被氧化为更高的价态。你的另一种假设是______ ;为了验证你的假设,请设计一种简便的实验方案______ 。
(2)另一组同学对铁和稀硝酸的反应进行探究。他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+,则a/b的取值范围是______ ;若反应结束后的溶液中n(Fe3+):n(Fe2+)=2:1,则a/b的值为______ 。
(1)一组同学用图1所示装置对铁与浓硫酸的反应进行实验。已知:2Fe + 6H2SO4(浓)
 Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。①检查装置气密性后,将过量的铁屑和一定量的浓硫酸放入烧瓶,塞紧橡皮塞,开始计时。t1时开始加热,在铁屑表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变。甲同学将收集到的气体体积与时间的关系粗略地表示为图2。

图1 图2
在0~t1时间段,铁屑表面没有气泡生成,说明铁在浓硫酸中发生了
②t2时,取少量反应液,先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现红色褪去。同学们对红色褪去的原因提出各自的假设。乙同学的假设是:溶液中的+3价铁被氧化为更高的价态。你的另一种假设是
(2)另一组同学对铁和稀硝酸的反应进行探究。他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+,则a/b的取值范围是
12-13高二上·江苏南京·阶段练习 查看更多[2]
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】重铬酸铵[(NH4)2Cr2O7](M=252 g·mol-1)常用作分析试剂、催化剂及媒染剂等。某化学兴趣小组对重铬酸铵的一些性质及组成进行探究。已知: + H2O
+ H2O 2
2 +2H+。回答下列问题:
+2H+。回答下列问题:
(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol·L-1 NaOH溶液,振荡、微热。产生的现象是______________________ 。
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.52 g重铬酸铵样品进行实验。

①实验过程中通入N2的主要目的是___________ 。
②实验过程中,若发现加热温度不够,如何改进?___________ 。
③C装置的作用是___________ 。加热A至恒重,观察到B中固体由白变蓝,D中酚酞溶液不变色,同时测得A中剩余固体1.52 g、B增重0.72 g,另外分解产物中还含有N2,则重铬酸铵受热分解的化学方程式为___________ 。
(3)为探究溶液酸性增强对铬(VI)盐溶液氧化性或Na2SO3溶液还原性的影响,该小组利用下图装置继续实验(已知物质氧化性与还原性强弱差异越大,电压越大)。

a.K闭合时,记录电压。
b.向U型管左侧溶液中滴加硫酸至pH=2后,电压增大了y。
c.继续向U型管右侧溶液中滴加硫酸后,无气体逸出,电压几乎不变。
①上述实验得出结论:___________ ;酸性增强,对Na2SO3溶液还原性几乎无影响。
②有同学认为:随着溶液酸性的增强,溶液中O2的氧化性增强也会使电压增大。补做实验:U型管左管中改为盛放___________ 溶液;然后向左管中滴加硫酸至pH=2后,测得电压增大了z,若z_____ y(填“>”、“<”或“=”),则证明实验结论不受影响。
 + H2O
+ H2O 2
2 +2H+。回答下列问题:
+2H+。回答下列问题:(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol·L-1 NaOH溶液,振荡、微热。产生的现象是
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.52 g重铬酸铵样品进行实验。

①实验过程中通入N2的主要目的是
②实验过程中,若发现加热温度不够,如何改进?
③C装置的作用是
(3)为探究溶液酸性增强对铬(VI)盐溶液氧化性或Na2SO3溶液还原性的影响,该小组利用下图装置继续实验(已知物质氧化性与还原性强弱差异越大,电压越大)。

a.K闭合时,记录电压。
b.向U型管左侧溶液中滴加硫酸至pH=2后,电压增大了y。
c.继续向U型管右侧溶液中滴加硫酸后,无气体逸出,电压几乎不变。
①上述实验得出结论:
②有同学认为:随着溶液酸性的增强,溶液中O2的氧化性增强也会使电压增大。补做实验:U型管左管中改为盛放
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某研究性学习小组探究硫的化合物的制备和性质。
Ⅰ.制备二氧化硫
用70%的浓硫酸与 固体反应制备
固体反应制备 气体。
气体。
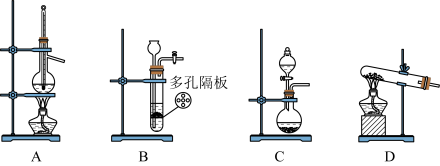
(1)制备 气体最合适的发生装置是
气体最合适的发生装置是_______ (填写字母)。
Ⅱ.制备硫代硫酸钠
已知:硫代硫酸钠易与酸反应。
反应原理: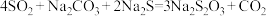
室温时,往 、
、 混合溶液中均匀通入
混合溶液中均匀通入 气体,一段时间后,溶液中有大量黄色浑浊物出现,然后浑浊物开始由黄变浅,当混合溶液pH值接近于7时,停止通入
气体,一段时间后,溶液中有大量黄色浑浊物出现,然后浑浊物开始由黄变浅,当混合溶液pH值接近于7时,停止通入 气体。
气体。
(2)制备 反应分三步进行
反应分三步进行
反应i: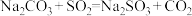 ;
;
反应ii: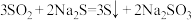 ;
;
反应iii的化学方程式为_______ 。
(3)当pH值接近于7时,停止通入 的原因是
的原因是_______ 。
Ⅲ.探究浓度对反应速率的影响
相同温度下,按下表中的体积将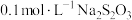 溶液、
溶液、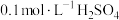 溶液与蒸馏水温合,并采集反应后浑浊度传感器数据。
溶液与蒸馏水温合,并采集反应后浑浊度传感器数据。
通过实验绘制出的浑浊度随时间变化关系如图所示:
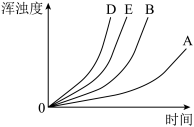
(4)①实验C、D、E探究_______ 溶液浓度对反应速率的影响。
②结合图像分析, 溶液、
溶液、 溶液二者相比,
溶液二者相比,_______ 溶液浓度的改变对化学反应速率的影响更大。
③请在答题卡相应的图中画出实验 对应的曲线
对应的曲线_______ 。
Ⅳ.探究性质
资料: 在酸性溶液中氧化
在酸性溶液中氧化 ,反应为:
,反应为: 。
。
向某浓度的过量 酸性溶液(含淀粉)中通入一定量后,停止通气,刚开始时溶液无明显变化,t秒后溶液突然变蓝。
酸性溶液(含淀粉)中通入一定量后,停止通气,刚开始时溶液无明显变化,t秒后溶液突然变蓝。
(5)某实验小组提出假设:t秒前生成了 ,但
,但 继续与溶液中的
继续与溶液中的 反应,且该反应速率较快,故溶液没有立刻变蓝,请写出
反应,且该反应速率较快,故溶液没有立刻变蓝,请写出 与
与 反应的离子方程式
反应的离子方程式_______ 。
(6)为验证该实验小组的假设合理,设计下面实验:
操作:向变蓝色的溶液中_______ ;现象:蓝色迅速消失,一段时间后再次变蓝。
Ⅰ.制备二氧化硫
用70%的浓硫酸与
 固体反应制备
固体反应制备 气体。
气体。
(1)制备
 气体最合适的发生装置是
气体最合适的发生装置是Ⅱ.制备硫代硫酸钠
已知:硫代硫酸钠易与酸反应。
反应原理:
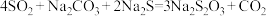
室温时,往
 、
、 混合溶液中均匀通入
混合溶液中均匀通入 气体,一段时间后,溶液中有大量黄色浑浊物出现,然后浑浊物开始由黄变浅,当混合溶液pH值接近于7时,停止通入
气体,一段时间后,溶液中有大量黄色浑浊物出现,然后浑浊物开始由黄变浅,当混合溶液pH值接近于7时,停止通入 气体。
气体。(2)制备
 反应分三步进行
反应分三步进行反应i:
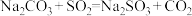 ;
;反应ii:
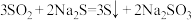 ;
;反应iii的化学方程式为
(3)当pH值接近于7时,停止通入
 的原因是
的原因是Ⅲ.探究浓度对反应速率的影响
相同温度下,按下表中的体积将
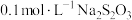 溶液、
溶液、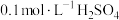 溶液与蒸馏水温合,并采集反应后浑浊度传感器数据。
溶液与蒸馏水温合,并采集反应后浑浊度传感器数据。| 实验标号 | 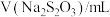 | 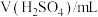 | V(蒸馏水)/mL |
| A | 1.5 | 3.5 | 10 |
| B | 2.5 | 3.5 | 9 |
| C | 3.5 | 3.5 | 8 |
| D | 3.5 | 2.5 | 9 |
| E | 3.5 | 1.5 | 10 |

(4)①实验C、D、E探究
②结合图像分析,
 溶液、
溶液、 溶液二者相比,
溶液二者相比,③请在答题卡相应的图中画出实验
 对应的曲线
对应的曲线Ⅳ.探究性质
资料:
 在酸性溶液中氧化
在酸性溶液中氧化 ,反应为:
,反应为: 。
。向某浓度的过量
 酸性溶液(含淀粉)中通入一定量后,停止通气,刚开始时溶液无明显变化,t秒后溶液突然变蓝。
酸性溶液(含淀粉)中通入一定量后,停止通气,刚开始时溶液无明显变化,t秒后溶液突然变蓝。(5)某实验小组提出假设:t秒前生成了
 ,但
,但 继续与溶液中的
继续与溶液中的 反应,且该反应速率较快,故溶液没有立刻变蓝,请写出
反应,且该反应速率较快,故溶液没有立刻变蓝,请写出 与
与 反应的离子方程式
反应的离子方程式(6)为验证该实验小组的假设合理,设计下面实验:
操作:向变蓝色的溶液中
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】某小组探究CuCl2溶液和Na2SO3溶液反应的主要产物,开展如下活动。
[实验准备]
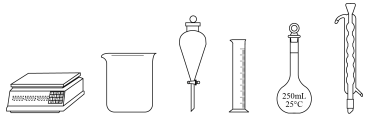
(1)用亚硫酸钠固体配制100mL0.2mol·L-1Na2SO3溶液,下列仪器中无需使用的有___________ (填名称)。
(2)检验亚硫酸钠溶液在空气中是否变质所需的试剂为___________ 。
[理论预测]
(3)预测3中反应的离子方程式为___________ 。
[实验探究]
实验1
取1mL0.2mol·L-1Na2SO3溶液和2mL0.2mol·L-1CuCl2溶液混合,立即生成橙黄色沉淀,3min后沉淀颜色变浅并伴有少量白色沉淀产生振荡1min沉淀全部变为白色。
为证明实验1产生的白色沉淀为CuCl,需鉴定沉淀中含Cl-、Cu+,其中鉴定含Cu+的实验设计如下:
实验2
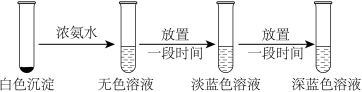
(4)已知[Cu(NH3)2]+、[Cu(NH3)4]2+在水中分别呈无色和深蓝色,实验2总反应的离子方程式为_____ 。
[进一步探究]
查阅资料获知橙黄色沉淀可能为xCuSO3·yCu2SO3·zH2O,在实验1获得橙黄色沉淀后,立即离心分离并洗涤。为探究其组成进行如下实验:
实验3

(5)离心分离的目的是加快过滤速度,防止___________ 。
(6)已知2Cu2++4I-=2CuI↓+I2,实验3___________ (选填“能”或“不能”)证明橙黄色沉淀中含有Cu2+和 。
。
为验证橙黄色沉淀转化为CuCl的原因可能是Cl-提高了Cu2+的氧化性,进行如下实验(已知装置中物质氧化性与还原性强弱差异越大,电压越大)。
实验4
(7)①表中X为___________ 。
②能证实实验结论的实验现象为___________ 。
[解释和结论]
综上所述,Cu2+与 发生复分解反应速率较快,发生氧化还原反应趋势更大。
发生复分解反应速率较快,发生氧化还原反应趋势更大。
[实验准备]
(1)用亚硫酸钠固体配制100mL0.2mol·L-1Na2SO3溶液,下列仪器中无需使用的有

(2)检验亚硫酸钠溶液在空气中是否变质所需的试剂为
[理论预测]
| 预测 | 主要产物 | 主要实验现象 |
| 1 | CuSO3 | 生成绿色沉淀 |
| 2 | Cu(OH)2、SO2 | 溶液中出现蓝色沉淀,伴有刺激性气味气体产生 |
| 3 | Cu2SO3 | 生成红色沉淀 |
| 4 | CuCl | 生成白色沉淀 |
[实验探究]
实验1
取1mL0.2mol·L-1Na2SO3溶液和2mL0.2mol·L-1CuCl2溶液混合,立即生成橙黄色沉淀,3min后沉淀颜色变浅并伴有少量白色沉淀产生振荡1min沉淀全部变为白色。
为证明实验1产生的白色沉淀为CuCl,需鉴定沉淀中含Cl-、Cu+,其中鉴定含Cu+的实验设计如下:
实验2

(4)已知[Cu(NH3)2]+、[Cu(NH3)4]2+在水中分别呈无色和深蓝色,实验2总反应的离子方程式为
[进一步探究]
查阅资料获知橙黄色沉淀可能为xCuSO3·yCu2SO3·zH2O,在实验1获得橙黄色沉淀后,立即离心分离并洗涤。为探究其组成进行如下实验:
实验3

(5)离心分离的目的是加快过滤速度,防止
(6)已知2Cu2++4I-=2CuI↓+I2,实验3
 。
。为验证橙黄色沉淀转化为CuCl的原因可能是Cl-提高了Cu2+的氧化性,进行如下实验(已知装置中物质氧化性与还原性强弱差异越大,电压越大)。
实验4
| 装置 | 试剂a | 试剂b | 电压表读数 |
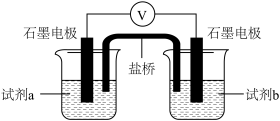 | 0.2mol·L-1Na2SO3溶液 | 0.2mol·L-1CuCl2 溶液 | V1 |
| 0.2mol·L-1Na2SO3溶液 | X | V2 |
②能证实实验结论的实验现象为
[解释和结论]
综上所述,Cu2+与
 发生复分解反应速率较快,发生氧化还原反应趋势更大。
发生复分解反应速率较快,发生氧化还原反应趋势更大。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】碘元素有“智力元素”之称。研究性学习小组做了如下实验探究海带中碘元素存在,并测定其中碘元素的含量。
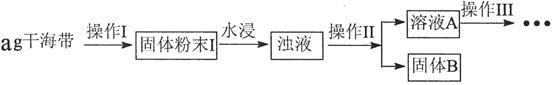
(1) 操作I为灼烧,则灼烧时用____________ (“烧杯”、“坩埚”、“蒸发皿”)盛装海带,操作Ⅱ为_________________ 。
(2) 水浸时通常要将悬浊液煮沸2-3min,目的是_________________ 。
(3) 操作III是某同学对溶液A中碘元素的存在形式进行的探究实验。
[推测]:① 以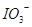 形式存在; ② 以
形式存在; ② 以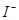 形式存在
形式存在
[查阅资料]:IO3- 和H2O2都具有较强的氧化性;
将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
限选试剂: 溶液、KSCN溶液、
溶液、KSCN溶液、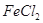 溶液、稀硫酸
溶液、稀硫酸
(4) 通过定量的检测实验操作和方法,测定某些数据,计算上述海带样品中碘元素的含量。

(1) 操作I为灼烧,则灼烧时用
(2) 水浸时通常要将悬浊液煮沸2-3min,目的是
(3) 操作III是某同学对溶液A中碘元素的存在形式进行的探究实验。
[推测]:① 以
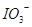 形式存在; ② 以
形式存在; ② 以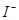 形式存在
形式存在[查阅资料]:IO3- 和H2O2都具有较强的氧化性;
将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
限选试剂:
 溶液、KSCN溶液、
溶液、KSCN溶液、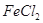 溶液、稀硫酸
溶液、稀硫酸| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管I、II | 无现象 | 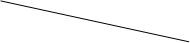 |
| ② | 往试管I中加入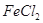 溶液,后加入2滴KSCN溶液并振荡; 溶液,后加入2滴KSCN溶液并振荡; | ||
| ③ | 溶液变蓝 |
(4) 通过定量的检测实验操作和方法,测定某些数据,计算上述海带样品中碘元素的含量。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某学习小组根据高中知识设计如下测定室内甲醛含量的装置(夹持装置已略)。

I.配制银氨溶液
⑴盛装AgNO3溶液的仪器D的名称_____________ 。
⑵关闭K2和K3,打开K1和分液漏斗活塞,将饱和食盐水滴入到圆底烧瓶中,当观察到D中最初生成的白色沉淀恰好完全溶解时,关闭K1和分液漏斗活塞。请写出A装置中发生反应的化学方程式_________ ;饱和食盐水的用途是________ 。
Ⅱ.测定室内空气中甲醛含量
⑶用热水浴加热D,打开K3,将滑动隔板由最左端抽到最右端,吸入1L室内空气,关闭K3,后续操作是_______________ 。
⑷装置中毛细管的作用是________________ 。
⑸已知甲醛被银氨溶液氧化的化学方程式为:HCHO+4Ag(NH3)2OH=(NH4)2CO3+4Ag↓+6NH3↑+2H2O,测得共生成Ag 2.16mg。则空气中甲醛的含量为_______ mg.L-1(空气中其它物质不与银氨溶液反应)。
⑹该设计装置存在一个明显的不足之处是____________ 。

I.配制银氨溶液
⑴盛装AgNO3溶液的仪器D的名称
⑵关闭K2和K3,打开K1和分液漏斗活塞,将饱和食盐水滴入到圆底烧瓶中,当观察到D中最初生成的白色沉淀恰好完全溶解时,关闭K1和分液漏斗活塞。请写出A装置中发生反应的化学方程式
Ⅱ.测定室内空气中甲醛含量
⑶用热水浴加热D,打开K3,将滑动隔板由最左端抽到最右端,吸入1L室内空气,关闭K3,后续操作是
⑷装置中毛细管的作用是
⑸已知甲醛被银氨溶液氧化的化学方程式为:HCHO+4Ag(NH3)2OH=(NH4)2CO3+4Ag↓+6NH3↑+2H2O,测得共生成Ag 2.16mg。则空气中甲醛的含量为
⑹该设计装置存在一个明显的不足之处是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】二氯亚砜(SOCl2)是一种无色易挥发液体,遇水剧烈水解生成两种气体,常用作脱水剂,其熔点-105℃,沸点79℃,140℃以上时易分解。
(1)用硫黄(用S表示)、液氯和三氧化硫为原料在一定条件合成二氯亚砜,原子利用率达100%,则三者的物质的量比为________ 。写出SOCl2吸收水蒸气的化学方程式:___________ 。
(2)甲同学设计下图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略):
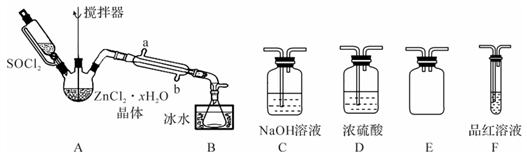
①装置的连接顺序为A→B→______→______→______→______。______________
②搅拌的作用是______ ,冷凝管的作用是_______________________________ 。
③实验结束后,为检测ZnCl2·xH2O晶体是否完全脱水,称取蒸干后的固体ag溶于水,加入足量稀硝酸和硝酸银溶液,过滤,洗涤,干燥,称得固体为bg。若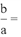
_____ (保留一位小数),即可证明ZnCl2·xH2O晶体已完全脱水。
④乙同学认为直接将ZnCl2·xH2O晶体置于坩埚中加热即可得到无水ZnCl2,但老师说此方法不可。请用化学方程式解释原因:______________________________________ 。
(3)丙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丁同学认为该实验会发生氧化还原反应。请你设计并简述实验方案判断丁同学的观点:_____________ 。
(1)用硫黄(用S表示)、液氯和三氧化硫为原料在一定条件合成二氯亚砜,原子利用率达100%,则三者的物质的量比为
(2)甲同学设计下图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略):

①装置的连接顺序为A→B→______→______→______→______。
②搅拌的作用是
③实验结束后,为检测ZnCl2·xH2O晶体是否完全脱水,称取蒸干后的固体ag溶于水,加入足量稀硝酸和硝酸银溶液,过滤,洗涤,干燥,称得固体为bg。若
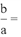
④乙同学认为直接将ZnCl2·xH2O晶体置于坩埚中加热即可得到无水ZnCl2,但老师说此方法不可。请用化学方程式解释原因:
(3)丙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丁同学认为该实验会发生氧化还原反应。请你设计并简述实验方案判断丁同学的观点:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】NH4Cl在生产生活中有重要的用途。某化学小组尝试制备NH4Cl并探究NH4Cl的某些性质,进行了以下实验:
(1)该小组用NH3和HCl合成NH4Cl。
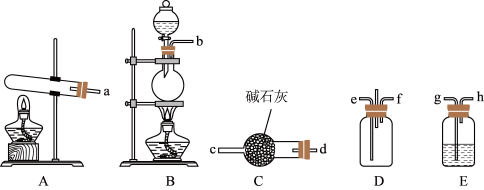
①写出用A装置制备NH3的化学方程式_______ 。
②为使NH3和HCl在D中充分混合并反应,上述装置的连接顺序为a→d→c→_______ 、_______ ←h←g←b。B中圆底烧瓶中放NaCl固体,则分液漏斗中的试剂为_______ 。
③装置D处除易堵塞导管外,还有不足之处为_______ 。
(2)该小组为探究Mg与NH4Cl溶液反应机理,常温下进行以下实验。实验中所取镁粉质量均为0.5g,分别加入到选取的实验试剂中。
资料:a.CH3COONH4溶液呈中性;b.Cl—对该反应几乎无影响。
①经检验实验2中刺激性气味气体为NH3,检验方法是_______ 。用排水法收集一小试管产生的气体,经检验小试管中气体为H2。
②已知灰白色沉淀中含有Mg2+、OH—。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。灰白色固体可能是_______ (填化学式)。
③甲同学认为实验2比实验1反应剧烈的原因是NH4Cl溶液中c(H+)大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。
试剂X是_______ 。
④为进一步探究实验2反应剧烈的原因,进行实验4:
依据上述实验,可以得出Mg能与NH 反应生成H2.,乙同学认为该方案不严谨,需要补充的实验方案是
反应生成H2.,乙同学认为该方案不严谨,需要补充的实验方案是_______ 。
⑤实验总结:通过上述实验,该小组同学得出Mg能与NH 反应生成H2的结论。
反应生成H2的结论。
(1)该小组用NH3和HCl合成NH4Cl。

①写出用A装置制备NH3的化学方程式
②为使NH3和HCl在D中充分混合并反应,上述装置的连接顺序为a→d→c→
③装置D处除易堵塞导管外,还有不足之处为
(2)该小组为探究Mg与NH4Cl溶液反应机理,常温下进行以下实验。实验中所取镁粉质量均为0.5g,分别加入到选取的实验试剂中。
资料:a.CH3COONH4溶液呈中性;b.Cl—对该反应几乎无影响。
| 实验 | 实验试剂 | 实验现象 |
| 1 | 5mL蒸馏水 | 反应缓慢,有少量气泡产生 (经检验为H2) |
| 2 | 5mL 1.0mol/L NH4Cl溶液 (pH=4.6) | 剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
②已知灰白色沉淀中含有Mg2+、OH—。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。灰白色固体可能是
③甲同学认为实验2比实验1反应剧烈的原因是NH4Cl溶液中c(H+)大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。
| 实验 | 实验装置 | 现象 |
| 3 | 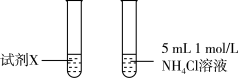 | 两试管反应剧烈程度相当 |
④为进一步探究实验2反应剧烈的原因,进行实验4:
| 实验 | 实验试剂 | 实验现象 |
| 4 | 5mL NH4Cl乙醇溶液 | 有无色无味气体产生 (经检验为H2) |
 反应生成H2.,乙同学认为该方案不严谨,需要补充的实验方案是
反应生成H2.,乙同学认为该方案不严谨,需要补充的实验方案是⑤实验总结:通过上述实验,该小组同学得出Mg能与NH
 反应生成H2的结论。
反应生成H2的结论。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】甲醛(HCHO)与葡萄糖相似具有强还原性,40%甲醛溶液沸点为96℃,易挥发。为探究过量甲醛和新制Cu(OH)2反应的产物,进行如下研究。
(1)在如图装置中进行实验,向a中加入0.5 mol/LCuSO4溶液50 mL和5 mol/LNaOH溶液100 mL,振荡,再加入40%的甲醛溶液50 mL,缓慢加热a,在65 ℃时回流20分钟后冷却至室温。反应过程中观察到有棕色固体生成,最后变成红褐色,并有气体产生。
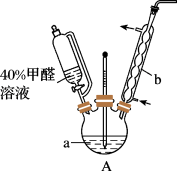
①仪器b的名称是_________ ,作用为_________ 。
②能说明甲醛具有还原性的实验现象是______________ 。
(2)查阅资料发现气体产物是副反应产生的。为确认气体产物含H2不含CO,将装置A和如图所示的装置连接后进行实验。
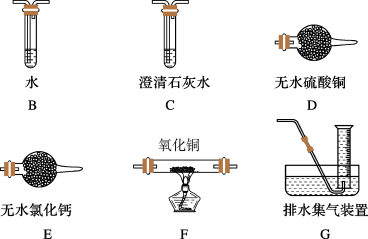
依次连接的合理顺序为A→B→___ →_____ →_____ →_____ →G,装置B的作用是______ 。
(3)已知: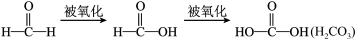 。设计实验证明a中甲醛的碳元素未被氧化成+4 价,
。设计实验证明a中甲醛的碳元素未被氧化成+4 价,___________ 。
(4)为研究红色固体产物的组成,进行如下实验(以下每步均充分反应):
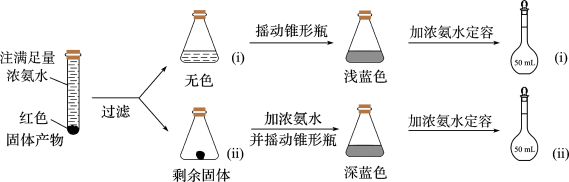
已知:Cu2O [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色)  [Cu(NH3)4]2+(蓝色)
[Cu(NH3)4]2+(蓝色)
①摇动锥形瓶i的目的是__________ 。
②锥形瓶ii中固体完全溶解得深蓝色溶液的离子方程式为_______________ 。
③将容量瓶ii中的溶液稀释100倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为___________ 。
(1)在如图装置中进行实验,向a中加入0.5 mol/LCuSO4溶液50 mL和5 mol/LNaOH溶液100 mL,振荡,再加入40%的甲醛溶液50 mL,缓慢加热a,在65 ℃时回流20分钟后冷却至室温。反应过程中观察到有棕色固体生成,最后变成红褐色,并有气体产生。

①仪器b的名称是
②能说明甲醛具有还原性的实验现象是
(2)查阅资料发现气体产物是副反应产生的。为确认气体产物含H2不含CO,将装置A和如图所示的装置连接后进行实验。

依次连接的合理顺序为A→B→
(3)已知:
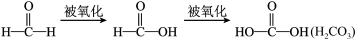 。设计实验证明a中甲醛的碳元素未被氧化成+4 价,
。设计实验证明a中甲醛的碳元素未被氧化成+4 价,(4)为研究红色固体产物的组成,进行如下实验(以下每步均充分反应):

已知:Cu2O
 [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色)  [Cu(NH3)4]2+(蓝色)
[Cu(NH3)4]2+(蓝色)①摇动锥形瓶i的目的是
②锥形瓶ii中固体完全溶解得深蓝色溶液的离子方程式为
③将容量瓶ii中的溶液稀释100倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】某兴趣小组设计实验验证铜与浓硝酸、稀硝酸的反应,装置如图所示(夹持装置未画出):
按图示连接好装置,_______后,装入药品,关闭 、
、 ,打开
,打开 ,一段时间后,再关闭
,一段时间后,再关闭 ,打开
,打开 ,加入足量的浓
,加入足量的浓 。
。
实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是_______ ;装置B中装浓硝酸的仪器名称是_______ 。
(2)实验一中“关闭 、
、 ,打开
,打开 ”的目的是
”的目的是_______
(3)装置B中发生反应的离子方程式为_______
(4)实验二的后续操作顺序为_______ (填标号),打开止水夹后装置C的具支试管中的现象为_______ 。
a.打开止水夹 b.打开 c.打开
c.打开 ,加入蒸馏水 d.关闭
,加入蒸馏水 d.关闭 e.插入铜丝。
e.插入铜丝。
(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2: 溶解在硝酸铜溶液中,导致溶液颜色不同。
溶解在硝酸铜溶液中,导致溶液颜色不同。
继续实验,打开 ,一段时间后,装置B中溶液变为蓝色,说明
,一段时间后,装置B中溶液变为蓝色,说明_______ 可能成立,请设计实验验证另一猜想的可能性:_______ 。
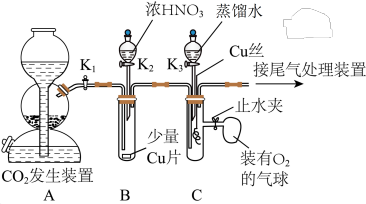
按图示连接好装置,_______后,装入药品,关闭
 、
、 ,打开
,打开 ,一段时间后,再关闭
,一段时间后,再关闭 ,打开
,打开 ,加入足量的浓
,加入足量的浓 。
。实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是
(2)实验一中“关闭
 、
、 ,打开
,打开 ”的目的是
”的目的是(3)装置B中发生反应的离子方程式为
(4)实验二的后续操作顺序为
a.打开止水夹 b.打开
 c.打开
c.打开 ,加入蒸馏水 d.关闭
,加入蒸馏水 d.关闭 e.插入铜丝。
e.插入铜丝。(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2:
 溶解在硝酸铜溶液中,导致溶液颜色不同。
溶解在硝酸铜溶液中,导致溶液颜色不同。继续实验,打开
 ,一段时间后,装置B中溶液变为蓝色,说明
,一段时间后,装置B中溶液变为蓝色,说明
您最近一年使用:0次



