下列有关微粒性质的排列顺序,正确的是
| A.原子半径:Sn>Si>P>S | B.热稳定性:CH4>NH3>H2O>HF |
| C.沸点:CH4>NH3>H2O>HF | D.键角:BF3>CH4>H2O>NH3 |
更新时间:2021-07-06 08:21:37
|
相似题推荐
【推荐1】氮、磷及其化合物应用广泛。磷元素有白磷、红磷等单质,白磷(P4)分子结构及晶胞如下图所示,实验室常用CuSO4溶液吸收有毒气体PH3,生成H3PO4、H2SO4和Cu。P元素可形成多种含氧酸,其中次磷酸(H3PO2)为一元弱酸;磷酸可与铁反应,在金属表面生成致密且难溶于水的磷酸盐膜。

| A.P4分子中的P-P-P键角为109°28′ |
| B.白磷和红磷互为同位素 |
| C.白磷晶体中1个P4分子周围有8个紧邻的P4分子 |
| D.白磷属于非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】元素非金属性强弱可以从简单氢化物的稳定性来判断。例如 、
、 、
、 的稳定性逐渐减弱,Cl、S、P的非金属性逐渐减弱。下列说法错误的是
的稳定性逐渐减弱,Cl、S、P的非金属性逐渐减弱。下列说法错误的是
 、
、 、
、 的稳定性逐渐减弱,Cl、S、P的非金属性逐渐减弱。下列说法错误的是
的稳定性逐渐减弱,Cl、S、P的非金属性逐渐减弱。下列说法错误的是A. 、 、 、 、 都是由极性键形成的极性分子 都是由极性键形成的极性分子 |
B. 、 、 、 、 中共价键键长逐渐增大,键能逐渐减小 中共价键键长逐渐增大,键能逐渐减小 |
C. 、 、 的中心原子的杂化方式相同 的中心原子的杂化方式相同 |
D.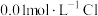 、S、P的最高价含氧酸溶液的 、S、P的最高价含氧酸溶液的 逐渐增大 逐渐增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z和W代表原子序数依次增大的四种短周期主族元素,它们满足以下条件:①在元素周期表中,Z与Y、W均相邻;②X、Y、W分别位于不同周期;③Y、Z、W三种元素的原子最外层电子数之和为17。下列说法错误的是
| A.在Y、Z的简单氢化物中,沸点高的是Z |
| B.X、Y、Z形成离子化合物的水溶液可以显酸性 |
| C.W的常见氧化物均为酸性氧化物 |
| D.X分别与Y、Z形成的核外电子总数为10的微粒最多只有4种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】W、X、Y、Z是原子序数依次增大的主族元素,在前三周期均有分布,基态X原子有四种不同空间运动状态的电子;Y为地壳中含量最多的元素,其简单离子与Z的简单离子具有相同电子数;工业上常通过电解Z的氧化物制取其单质,下列说法不正确的是
A.元素电负性: |
B.简单氢化物的沸点: |
| C.W2Y2和XY2都是极性分子 |
| D.Z同周期且第一电离能小于Z的元素有1种 |
您最近一年使用:0次

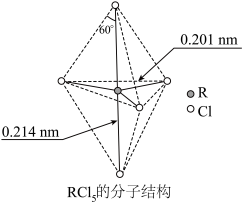
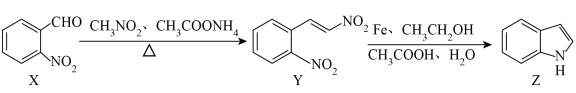
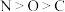
 原子的简化电子排布式为
原子的简化电子排布式为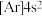
 分子中
分子中 原子和
原子和 原子都是
原子都是 杂化
杂化

