(1)①已知:
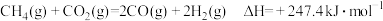
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
(2)一定条件下,在水溶液中所含离子 、
、 、
、 、
、 、
、 各
各 ,其相对能量的大小如下图所示(各离子在图中用氯元素的相应化合价表示),则反应
,其相对能量的大小如下图所示(各离子在图中用氯元素的相应化合价表示),则反应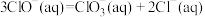 的
的
_______  。
。
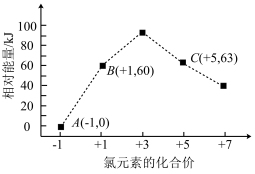
(3)工业上可通过天然气跟水蒸气反应制取 :
: ,有关反应的能量变化如下图所示,则该反应的
,有关反应的能量变化如下图所示,则该反应的
_______  (用含
(用含 、
、 、c的式子表示)。
、c的式子表示)。
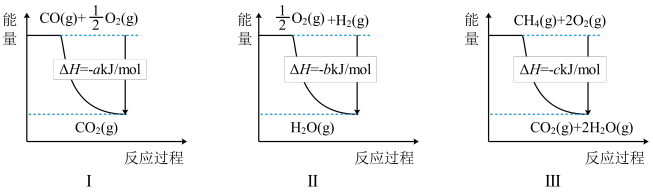

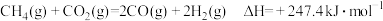
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)一定条件下,在水溶液中所含离子
 、
、 、
、 、
、 、
、 各
各 ,其相对能量的大小如下图所示(各离子在图中用氯元素的相应化合价表示),则反应
,其相对能量的大小如下图所示(各离子在图中用氯元素的相应化合价表示),则反应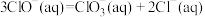 的
的
 。
。
(3)工业上可通过天然气跟水蒸气反应制取
 :
: ,有关反应的能量变化如下图所示,则该反应的
,有关反应的能量变化如下图所示,则该反应的
 (用含
(用含 、
、 、c的式子表示)。
、c的式子表示)。
更新时间:2021-07-06 07:54:48
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为:
C(石墨,s)
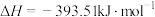
C(金刚石,s)

(1)请写出石墨转化为金刚石的热化学方程式________ 。
(2)已知物质的能量越低越稳定,请根据热化学方程式比较金刚石与石墨的稳定性________ 。
C(石墨,s)

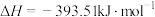
C(金刚石,s)


(1)请写出石墨转化为金刚石的热化学方程式
(2)已知物质的能量越低越稳定,请根据热化学方程式比较金刚石与石墨的稳定性
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.化学反应在发生物质变化的同时伴随着能量变化,请回答下列问题:
(1)汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图所示,则图中三种分子最稳定的是
的能量变化如图所示,则图中三种分子最稳定的是___________ ,图中对应反应的热化学方程式为___________ 。 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。
在空气中加热反应可制得铁系氧化物材料。
已知25℃,101 时:
时:
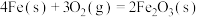
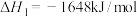


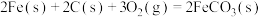
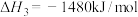
则

___________ 。
Ⅱ.某实验小组设计用0.55 的
的 溶液100
溶液100 与0.50
与0.50 的盐酸100
的盐酸100 置于如图所示的装置中进行测定中和反应反应热的实验。
置于如图所示的装置中进行测定中和反应反应热的实验。___________ ,装置中还存在的错误有___________ ;大烧杯杯口若不盖泡沫塑料板,测得中和反应的反应热 将
将___________ (填“偏大”、“偏小”或“无影响”)。
(4)实验中,所用 稍过量的原因是
稍过量的原因是___________ 。
(5)该实验小组做了三次实验,每次取盐酸和 溶液各100
溶液各100 ,并记录原始数据:
,并记录原始数据:
已知盐酸、 溶液密度均近似为1.00
溶液密度均近似为1.00 ,中和后混合液
,中和后混合液 ,则该中和反应的反应热
,则该中和反应的反应热
___________ 。(保留到小数点后1位)
(1)汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图所示,则图中三种分子最稳定的是
的能量变化如图所示,则图中三种分子最稳定的是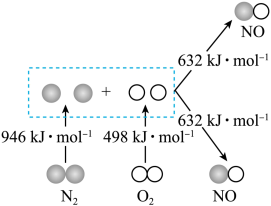
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。
在空气中加热反应可制得铁系氧化物材料。已知25℃,101
 时:
时: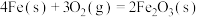
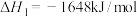


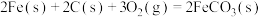
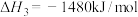
则


Ⅱ.某实验小组设计用0.55
 的
的 溶液100
溶液100 与0.50
与0.50 的盐酸100
的盐酸100 置于如图所示的装置中进行测定中和反应反应热的实验。
置于如图所示的装置中进行测定中和反应反应热的实验。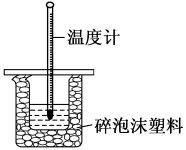
 将
将(4)实验中,所用
 稍过量的原因是
稍过量的原因是(5)该实验小组做了三次实验,每次取盐酸和
 溶液各100
溶液各100 ,并记录原始数据:
,并记录原始数据:| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温差 /℃ /℃ | ||
| 盐酸 |  溶液 溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.0 | 3.0 |
| 2 | 25.1 | 25.1 | 25.1 | 28.2 | 3.1 |
| 3 | 25.1 | 25.1 | 25.1 | 28.0 | 2.9 |
 溶液密度均近似为1.00
溶液密度均近似为1.00 ,中和后混合液
,中和后混合液 ,则该中和反应的反应热
,则该中和反应的反应热
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】依据事实,书写下列热化学方程式:
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:___ 。
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式__ 。
(3)已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–1
2NO(g)+O2(g) 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式___ 。
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:___ 。
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式
(3)已知:2SO2(g)+O2(g)
 2SO3(g)ΔH=-196.6kJ·mol–1
2SO3(g)ΔH=-196.6kJ·mol–12NO(g)+O2(g)
 2NO2(g)ΔH=-113.0kJ·mol–1
2NO2(g)ΔH=-113.0kJ·mol–1请写出NO2与SO2反应生成SO3和NO的热化学方程式
(4)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气,它由煤炭与水(蒸气)反应制得,故又称水煤气。当1mol水蒸气完全参与反应,吸收131kJ热量。试写出制取水煤气主要反应的热化学方程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】I (1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、___________ 、___________ 。
(2)量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是__________ (填序号)。
A.50 mL 0.50 mol·L-1 NaOH溶液
B.50 mL 0.55 mol·L-1 NaOH溶液
C.1.0 g NaOH固体
(3)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如下表所示。
乙在实验之前预计ΔH1≠ΔH2,他的根据是_________ 。
II(4)研究NOx、SO2、CO等大气污染气体的处理具有重要意义。处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是___________ 。
(5)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成1 mol AX5,放出热量123.8 kJ。该反应的热化学方程式为_____________ 。
(2)量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是
A.50 mL 0.50 mol·L-1 NaOH溶液
B.50 mL 0.55 mol·L-1 NaOH溶液
C.1.0 g NaOH固体
(3)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如下表所示。
| 反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热/kJ·mol-1 |
| A.1.0 mol·L-1 HCl溶液50 mL、1.1 mol·L-1 NaOH溶液50 mL | 13.0 | ΔH1 | |
| B.1.0 mol·L-1 HCl溶液50 mL、1.1 mol·L-1 NH3·H2O溶液50 mL | 13.0 | ΔH2 |
乙在实验之前预计ΔH1≠ΔH2,他的根据是
II(4)研究NOx、SO2、CO等大气污染气体的处理具有重要意义。处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是
(5)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成1 mol AX5,放出热量123.8 kJ。该反应的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】国际非政府组织“全球碳计划”发布报告显示,全球二氧化碳排放量增速趋缓。将CO2转化成有机物实现碳循环是解决温室问题的有效途径。
(1)已知:
C2H4(g)+H2O(l)=C2H5OH(l) ΔH1=-42.0kJ/mol
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) ΔH2=+1401.0kJ/mol
则92g的C2H5OH完全燃烧的ΔH=___________ kJ/mol。
(2)CO2镍催化氢化制甲烷,甲酸(HCOOH)是CO2转化为CH4的中间体:
CO2 HCOOH
HCOOH CH4
CH4
当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是___________ (填“I”或“Ⅱ”)。
(3)已知:
2CO(g)+O2(g)=2CO2(g) ΔH1=-560kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH2=-474kJ/mol
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ΔH3=-1360kJ/mol
写出以CO(g)和H2(g)为原料合成甲醇的热化学方程式___________
(4)下列将CO2转化成有机物的反应中,原子利用率最高的是___________ (填序号)。
A.6CO2+6H2O C6H12O6+6O2
C6H12O6+6O2
B.CO2+CH4 CH3COOH
CH3COOH
C.2CO2+6H2 CH2=CH2+4H2O
CH2=CH2+4H2O
D.CO2+3H2 CH3OH+H2O
CH3OH+H2O
(1)已知:
C2H4(g)+H2O(l)=C2H5OH(l) ΔH1=-42.0kJ/mol
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) ΔH2=+1401.0kJ/mol
则92g的C2H5OH完全燃烧的ΔH=
(2)CO2镍催化氢化制甲烷,甲酸(HCOOH)是CO2转化为CH4的中间体:
CO2
 HCOOH
HCOOH CH4
CH4当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是
(3)已知:
2CO(g)+O2(g)=2CO2(g) ΔH1=-560kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH2=-474kJ/mol
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ΔH3=-1360kJ/mol
写出以CO(g)和H2(g)为原料合成甲醇的热化学方程式
(4)下列将CO2转化成有机物的反应中,原子利用率最高的是
A.6CO2+6H2O
 C6H12O6+6O2
C6H12O6+6O2B.CO2+CH4
 CH3COOH
CH3COOHC.2CO2+6H2
 CH2=CH2+4H2O
CH2=CH2+4H2OD.CO2+3H2
 CH3OH+H2O
CH3OH+H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)写出下列物质在水溶液中电离的方程式:
HNO3_______________________________ ;HClO___________________________________ ;
NaHCO3__________________________________ 、___________________________________ 。
(2)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________________________________________ 。
(3)已知:①H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+ O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
回答下列问题:
①上述反应中属于放热反应的是________________________________________________ 。
②H2的燃烧热为_____________________ ,C的燃烧热为____________________________ 。
③燃烧l0gH2生成液态水,放出的热量为________________________________________ 。
④CO的燃烧热为___________ ,其热化学方程式为_________________________________ 。
HNO3
NaHCO3
(2)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(3)已知:①H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+ O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
回答下列问题:
①上述反应中属于放热反应的是
②H2的燃烧热为
③燃烧l0gH2生成液态水,放出的热量为
④CO的燃烧热为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】写出或完成下列热化学方程式。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ 的热量。写出CH4燃烧的热化学方程式__________ 。
(2)通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。下表是一些化学键的键能。
根据键能数据估算下列反应:CH4(g) + 4F2(g)=CF4(g) + 4HF(g)的反应热△H为_____ 。
(3)1840年瑞士的化学家盖斯(Hess)在总结大量实验事实(热化学实验数据)的基础上提出:“定压或定容条件下的任意化学反应,在不做其它功时,不论是一步完成的还是几步完成的,其热效应总是相同的(反应热的总值相等)。”
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3
请写出CO还原FeO的热化学方程式:______ 。
(4)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为__________ ;
②氢气燃烧热的热化学方程式为________ ;
(5)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
则ΔH2=_______ kJ·mol-1;
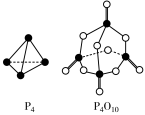
(6)白磷与氧气可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH为_____ 。
(7)同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
①P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2 983.2 kJ·mol-1
②P(红磷,s)+5/4O2(g)=1/4P4O10(s) ΔH2=-738.5 kJ·mol-1
相同状况下,能量较低的是________ ;白磷的稳定性比红磷________ (填“大”或“小”)。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ 的热量。写出CH4燃烧的热化学方程式
(2)通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。下表是一些化学键的键能。
| 化学键 | C-H | C-F | H-F | F-F |
| 键能kJ/mol | 414 | 489 | 565 | 155 |
根据键能数据估算下列反应:CH4(g) + 4F2(g)=CF4(g) + 4HF(g)的反应热△H为
(3)1840年瑞士的化学家盖斯(Hess)在总结大量实验事实(热化学实验数据)的基础上提出:“定压或定容条件下的任意化学反应,在不做其它功时,不论是一步完成的还是几步完成的,其热效应总是相同的(反应热的总值相等)。”
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3
请写出CO还原FeO的热化学方程式:
(4)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为
②氢气燃烧热的热化学方程式为
(5)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
则ΔH2=
(6)白磷与氧气可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH为

(7)同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
①P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2 983.2 kJ·mol-1
②P(红磷,s)+5/4O2(g)=1/4P4O10(s) ΔH2=-738.5 kJ·mol-1
相同状况下,能量较低的是
您最近一年使用:0次

 经过催化氢化合成低碳烯烃。其合成乙烯的反应为
经过催化氢化合成低碳烯烃。其合成乙烯的反应为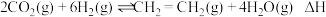 。几种物质的能量(在标准状况下规定单质的能量为0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
。几种物质的能量(在标准状况下规定单质的能量为0,测得其他物质在生成时所放出或吸收的热量)如下表所示:

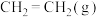

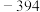


 ,已知:
,已知:







