近年来人们开发了一种由铝合金和硼纤维组成的铝合金基-硼纤维复合材料。该材料具有比铝合金更高的比强度和比模量,可用于航空、航天飞行器。有人设计了一种分析这种复合材料中硼含量的方法:用混酸溶解m克样品,配成体积为V0的试样溶液;通过强酸型阳离子交换树脂除尽溶液中的金属阳离子;以甲基红为指示剂,用NaOH溶液中和试样溶液;加入甘露醇,使硼酸(Ka=5.8×10-10)定量地转变为甘露醇-硼酸配合物(Ka=8.4×10-6),反应方程式为:
 +H3BO3=
+H3BO3=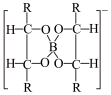 +H++3H2O
+H++3H2O
再加入适当指示剂,用NaOH溶液滴定到终点。主要分析流程图如下(图中只列出主要物质,其他少量物质的干扰可以不予考虑)。

(1)写出从A框到B框生成H3BO3的反应方程式以及H3BO3在水溶液中的电离方程式___ 、___ 。
(2)除去过量酸后的热溶液在冷却至室温过程中有时析出白色鳞片状晶体。写出该晶体的化学式并解释为什么晶体呈片状_____ 、_____ 。
(3)从C框到D框的滴定操作过程中,是否需要准确地中和H+____ ?简述原因_____ 。
(4)从原理上分析D框到E框这一步操作的目的______ 。
(5)如果E框中配合物和NaOH滴定剂的浓度均为0.10mol·L-1,请估算滴定到化学计量点时的pH___ ,并指出从E框到F框的滴定过程中,应该选用哪种指示剂___ ?滴定终点的颜色是什么____ ?
(6)V0、V1和V2的单位都为mL,MB为硼的摩尔质量(g·mol-1),c(NaOH)为NaOH溶液的浓度(mol·L-1),请给出被测溶液中硼含量(g·L-1)的计算式________ 。
 +H3BO3=
+H3BO3= +H++3H2O
+H++3H2O再加入适当指示剂,用NaOH溶液滴定到终点。主要分析流程图如下(图中只列出主要物质,其他少量物质的干扰可以不予考虑)。

(1)写出从A框到B框生成H3BO3的反应方程式以及H3BO3在水溶液中的电离方程式
(2)除去过量酸后的热溶液在冷却至室温过程中有时析出白色鳞片状晶体。写出该晶体的化学式并解释为什么晶体呈片状
(3)从C框到D框的滴定操作过程中,是否需要准确地中和H+
(4)从原理上分析D框到E框这一步操作的目的
(5)如果E框中配合物和NaOH滴定剂的浓度均为0.10mol·L-1,请估算滴定到化学计量点时的pH
| 指示剂 | 变色范围pH | 颜色 | pKHln | |
| 酸式 | 碱式 | |||
| 甲基橙 | 3.1~4.4 | 红 | 橙黄 | 3.4 |
| 甲基红 | 4.4~6.2 | 红 | 黄 | 5.0 |
| 酚红 | 6.7~8.4 | 黄 | 红 | 8.0 |
| 酚酞 | 8.2~10.0 | 无 | 紫红 | 9.4 |
2008高三上·全国·竞赛 查看更多[2]
更新时间:2021-07-08 14:37:24
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】工业上用含三价钒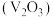 为主的某石煤为原料(含有
为主的某石煤为原料(含有 、
、 等杂质),钙化法焙烧制备
等杂质),钙化法焙烧制备 ,其流程如下:
,其流程如下:

【资料】: 价钒在溶液中的主要存在形式与溶液pH的关系:
价钒在溶液中的主要存在形式与溶液pH的关系:
(1)焙烧:向石煤中加生石灰焙烧,将 转化为
转化为 的化学方程式是
的化学方程式是___________ 。
(2)酸浸:
① 难溶于水可溶于盐酸。若焙砂酸浸时溶液的
难溶于水可溶于盐酸。若焙砂酸浸时溶液的 ,
, 溶于盐酸的离子方程式是
溶于盐酸的离子方程式是___________ 。
②酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约3.2%,根据如图推测,酸浸时不选择更高酸度的原因是___________ 。

(3)转沉:将浸出液中的钒转化为 固体,其流程如下:
固体,其流程如下:

①浸出液中加入石灰乳的作用是___________ 。
②已知 的溶解度小于
的溶解度小于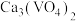 。向
。向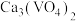 沉淀中加入
沉淀中加入 溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:
溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:___________ 。
(4)测定产品中 的纯度:
的纯度:
称取ag产品,先用硫酸溶解,得到 溶液。再加入
溶液。再加入 溶液
溶液 。最后用
。最后用 溶液滴定过量的
溶液滴定过量的 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 。已知
。已知 被还原为
被还原为 ,假设杂质不参与反应,则产品中
,假设杂质不参与反应,则产品中 的质量分数是
的质量分数是___________ 。( 的摩尔质量:
的摩尔质量: )
)
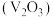 为主的某石煤为原料(含有
为主的某石煤为原料(含有 、
、 等杂质),钙化法焙烧制备
等杂质),钙化法焙烧制备 ,其流程如下:
,其流程如下:
【资料】:
 价钒在溶液中的主要存在形式与溶液pH的关系:
价钒在溶液中的主要存在形式与溶液pH的关系:| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  | 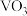 |  |  |
(1)焙烧:向石煤中加生石灰焙烧,将
 转化为
转化为 的化学方程式是
的化学方程式是(2)酸浸:
①
 难溶于水可溶于盐酸。若焙砂酸浸时溶液的
难溶于水可溶于盐酸。若焙砂酸浸时溶液的 ,
, 溶于盐酸的离子方程式是
溶于盐酸的离子方程式是②酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约3.2%,根据如图推测,酸浸时不选择更高酸度的原因是

(3)转沉:将浸出液中的钒转化为
 固体,其流程如下:
固体,其流程如下:
①浸出液中加入石灰乳的作用是
②已知
 的溶解度小于
的溶解度小于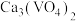 。向
。向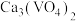 沉淀中加入
沉淀中加入 溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:
溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:(4)测定产品中
 的纯度:
的纯度:称取ag产品,先用硫酸溶解,得到
 溶液。再加入
溶液。再加入 溶液
溶液 。最后用
。最后用 溶液滴定过量的
溶液滴定过量的 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 。已知
。已知 被还原为
被还原为 ,假设杂质不参与反应,则产品中
,假设杂质不参与反应,则产品中 的质量分数是
的质量分数是 的摩尔质量:
的摩尔质量: )
)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】取一定量加碘食盐(可能含 、KI、
、KI、 等),加蒸馏水溶解,分成几份对加碘食盐的组成进行实验测定。(已知酸性条件下
等),加蒸馏水溶解,分成几份对加碘食盐的组成进行实验测定。(已知酸性条件下 能氧化
能氧化 ,碱性或中性条件下
,碱性或中性条件下 不能氧化
不能氧化 )
)
(1)配制一定质量分数的加碘盐溶液的下列操作正确的是_______ 。_______ ,实验Ⅱ中红色物质的化学名称为_______ 。
(3)实验Ⅲ中溶液不变色,说明加碘食盐_______ (填“含”或“不含”)KI。
(4)有同学认为该加碘盐中可能含 ,设计实验方案检验是否含
,设计实验方案检验是否含
_______ 。
(5)加碘盐中若含KI,在潮湿空气中易引起碘的损失,为提高其稳定性,可加适量稳定剂,以减少碘的损失,下列物质可以作为稳定剂的是_______。
(6)为测定加碘盐中 的含量,实验小组称取x g加碘盐,加蒸馏水溶解,滴加适量稀盐酸和几滴淀粉溶液,并加入足量KI固体,充分反应后,用a mol/L的
的含量,实验小组称取x g加碘盐,加蒸馏水溶解,滴加适量稀盐酸和几滴淀粉溶液,并加入足量KI固体,充分反应后,用a mol/L的 标准溶液进行滴定,消耗VmL标准溶液,则加碘盐中
标准溶液进行滴定,消耗VmL标准溶液,则加碘盐中 含量为
含量为_______ mg/kg。(列出计算表达式,已知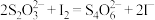 ,忽略测定过程中微量
,忽略测定过程中微量 的干扰)
的干扰)
(7)有同学认为可以直接用 溶液检测
溶液检测 的存在,并根据反应溶液蓝色出现的时间来衡量反应速率,实验记录如下:
的存在,并根据反应溶液蓝色出现的时间来衡量反应速率,实验记录如下:
设计该实验的目的是_______ 。
 、KI、
、KI、 等),加蒸馏水溶解,分成几份对加碘食盐的组成进行实验测定。(已知酸性条件下
等),加蒸馏水溶解,分成几份对加碘食盐的组成进行实验测定。(已知酸性条件下 能氧化
能氧化 ,碱性或中性条件下
,碱性或中性条件下 不能氧化
不能氧化 )
)| 实验 | 现象 |
Ⅰ.取一份溶液,滴加少量稀硫酸酸化,加入足量KI固体,加入适量 振荡,静置 振荡,静置 | 加入足量KI固体,溶液显淡黄色,加入 振荡静置后下层溶液显紫红色 振荡静置后下层溶液显紫红色 |
| Ⅱ.另取一份溶液滴加KSCN溶液 | 溶液显红色 |
| Ⅲ.另取一份溶液滴加淀粉溶液,并滴加少量稀硫酸 | 溶液不变色 |
a.  b.
b.  c.
c.  d.
d. 
(3)实验Ⅲ中溶液不变色,说明加碘食盐
(4)有同学认为该加碘盐中可能含
 ,设计实验方案检验是否含
,设计实验方案检验是否含
(5)加碘盐中若含KI,在潮湿空气中易引起碘的损失,为提高其稳定性,可加适量稳定剂,以减少碘的损失,下列物质可以作为稳定剂的是_______。
A. | B. | C. | D. |
 的含量,实验小组称取x g加碘盐,加蒸馏水溶解,滴加适量稀盐酸和几滴淀粉溶液,并加入足量KI固体,充分反应后,用a mol/L的
的含量,实验小组称取x g加碘盐,加蒸馏水溶解,滴加适量稀盐酸和几滴淀粉溶液,并加入足量KI固体,充分反应后,用a mol/L的 标准溶液进行滴定,消耗VmL标准溶液,则加碘盐中
标准溶液进行滴定,消耗VmL标准溶液,则加碘盐中 含量为
含量为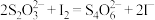 ,忽略测定过程中微量
,忽略测定过程中微量 的干扰)
的干扰)(7)有同学认为可以直接用
 溶液检测
溶液检测 的存在,并根据反应溶液蓝色出现的时间来衡量反应速率,实验记录如下:
的存在,并根据反应溶液蓝色出现的时间来衡量反应速率,实验记录如下:| 含淀粉和稀盐酸的加碘盐溶液/mL | 0.01mol/L的 溶液/mL 溶液/mL | 加水体积/mL | 实验温度/℃ | 出现蓝色时间/s | |
| 实验1 | 15 | 5 | 25 | 25 | |
| 实验2 | 15 |  | 30 | 25 | |
| 实验3 | 15 | 5 |  | 0 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2) 制取MnSO4·H2O并回收单质硫的工艺流程如下:
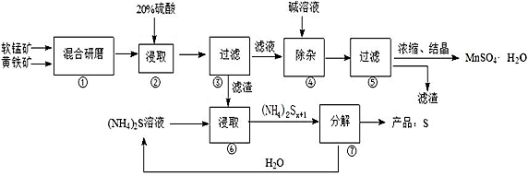
已知:本实验条件下,高锰酸钾溶液与硫酸锰溶液混合产生二氧化锰。
回答下列问题:
(1)步骤①混合研磨成细粉的主要目的是___________________________________ ;步骤②浸取时若生成S、MnSO4及Fe2(SO4)3的化学方程式为___________________________________ 。
(2)步骤③所得酸性滤液可能含有Fe2+,为了除去Fe2+可先加入_________________ ;步骤④需将溶液加热至沸然后在不断搅拌下加入碱调节pH为4-5,再继续煮沸一段时间,“继续煮沸”的目的是_____________________________________ 。步骤⑤所得滤渣为__________________ (填化学式)。
(3)步骤⑦需在90-100℃下进行,该反应的化学方程式________________________ 。
(4)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1KMnO4标准溶液滴定至浅红色且半分钟不褪色,消耗标准溶液VmL,产品中Mn2+的质量分数为w(Mn2+)=________________ 。

已知:本实验条件下,高锰酸钾溶液与硫酸锰溶液混合产生二氧化锰。
回答下列问题:
(1)步骤①混合研磨成细粉的主要目的是
(2)步骤③所得酸性滤液可能含有Fe2+,为了除去Fe2+可先加入
(3)步骤⑦需在90-100℃下进行,该反应的化学方程式
(4)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1KMnO4标准溶液滴定至浅红色且半分钟不褪色,消耗标准溶液VmL,产品中Mn2+的质量分数为w(Mn2+)=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】同为常见小分子,NO星光熠熠,H2S却臭名昭著。然而,近期研究发现,在生命体系中NO与H2S窃窃私语。研究二者的相互作用对于解开生命起源、理解生理过程的奥秘至关重要。NO与H2S之间的反应及产物非常复杂,这里我们一起关注一些重要的基本问题。
(1)早在19世纪,NO与H2S的反应就受到关注。依赖于反应条件甚至容器(表面可能作为催化剂),可以得到多种产物。最简单的一种就是产物中出现两种单质(反应1),而反应过程出现笑气也是绕不开的步骤(反应2),条件适当的时候,还会产生硫化铵(反应3)。写出反应1-3的方程式_____ 。
(2)研究发现,HNO、HSNO、HSSNO、HS2-等均是生理过程的关键物种,可由NO与H2S作用产生。
①HSNO(A)表达式给出的原子次序就是其连接方式。画出A及其共轭碱(B)的Lewis结构式(要求最稳定的形式)_____ 。
②尽管A是最稳定的形式,但是通过低温下光解反应,也可以得到其他键合方式不同的异构体。画出A所有其他合理异构体的骨架结构_____ 。
③据信SSNO-参与多个生理过程。其中涉及SSNO-形成及变化的可能反应及热力学常数
如下: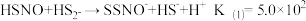

计算298K下HSSNO的酸解离常数Ka_____ 。
(3)为理解佥属离子在相关过程的作用,开展了如下研究:空气中,在络离子A([Ru(EDTA)(OH)]2-,EDTA为乙二胺四乙酸根)的溶液中,加入NaHS溶液并充分搅拌,溶液变为蓝绿色,对应于双核络离子B的生成(反应4)。分别取A和B的溶液,在惰性气体保护下,加入被NO饱和的磷酸盐缓冲液(pH=8.2),充分反应,A转化为C,B转化为D(反应5)。借助于质谱分析,计算出四个络离子的式量分别为A:406.3,B:842.7,C:419.3,D:451.4.磁性测量发现,C为抗磁性,D为顺磁性。
①写出络离子B、C、D的结构简式_____ 。
②写出反应4和5的离子方程式_____ 。
③画出C和D中佥属离子d轨道在八面体场(近似看作正八面体)中的分裂图并给出d电子排布_____ 。
(1)早在19世纪,NO与H2S的反应就受到关注。依赖于反应条件甚至容器(表面可能作为催化剂),可以得到多种产物。最简单的一种就是产物中出现两种单质(反应1),而反应过程出现笑气也是绕不开的步骤(反应2),条件适当的时候,还会产生硫化铵(反应3)。写出反应1-3的方程式
(2)研究发现,HNO、HSNO、HSSNO、HS2-等均是生理过程的关键物种,可由NO与H2S作用产生。
①HSNO(A)表达式给出的原子次序就是其连接方式。画出A及其共轭碱(B)的Lewis结构式(要求最稳定的形式)
②尽管A是最稳定的形式,但是通过低温下光解反应,也可以得到其他键合方式不同的异构体。画出A所有其他合理异构体的骨架结构
③据信SSNO-参与多个生理过程。其中涉及SSNO-形成及变化的可能反应及热力学常数
如下:
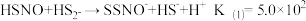

计算298K下HSSNO的酸解离常数Ka
(3)为理解佥属离子在相关过程的作用,开展了如下研究:空气中,在络离子A([Ru(EDTA)(OH)]2-,EDTA为乙二胺四乙酸根)的溶液中,加入NaHS溶液并充分搅拌,溶液变为蓝绿色,对应于双核络离子B的生成(反应4)。分别取A和B的溶液,在惰性气体保护下,加入被NO饱和的磷酸盐缓冲液(pH=8.2),充分反应,A转化为C,B转化为D(反应5)。借助于质谱分析,计算出四个络离子的式量分别为A:406.3,B:842.7,C:419.3,D:451.4.磁性测量发现,C为抗磁性,D为顺磁性。
①写出络离子B、C、D的结构简式
②写出反应4和5的离子方程式
③画出C和D中佥属离子d轨道在八面体场(近似看作正八面体)中的分裂图并给出d电子排布
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】钒在生物医学、机械、催化等领域具有广泛的应用。多钒酸盐阴离子具有生物活性。溶液中五价钒的存在形体与溶液酸度和浓度有关,在弱酸性溶液中易形成多钒酸根阴离子,如十钒酸根V10O 、HV10O
、HV10O 和H2V10O
和H2V10O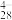 等。将NH4VO3溶于弱酸性介质中,加入乙醇可以得到橙色的十钒酸铵晶体(NH4)xH6-xV10O28·nH2O(用A表示)。元素分析结果表明,A中氢的质量分数为3.13%。用下述实验对该化合物进行分析,以确定其组成。
等。将NH4VO3溶于弱酸性介质中,加入乙醇可以得到橙色的十钒酸铵晶体(NH4)xH6-xV10O28·nH2O(用A表示)。元素分析结果表明,A中氢的质量分数为3.13%。用下述实验对该化合物进行分析,以确定其组成。
实验1:准确称取0.9291gA于三颈瓶中,加入100mL蒸馏水和150mL20%NaOH溶液,加热煮沸,生成的氨气用50.00mL0.1000mol·L-1HCl标准溶液吸收。加入酸碱指示剂,用0.1000mol·L-1NaOH标准溶液滴定剩余的HCl标准溶液,终点时消耗19.88mLNaOH标准溶液。
实验2:准确称取0.3097gA于锥形瓶中,加入40mL1.5mol·L-1H2SO4,微热使之溶解。加入50mL蒸馏水和1gNaHSO3,搅拌5分钟,便反应完全,五价钒被还原成四价。加热煮沸15分钟,然后用0.02005mol·L-1KMnO4标准溶液滴定,终点时消耗25.10mLKMnO4标准溶液。
(1)如图为滴定曲线图,请回答哪一个图为实验1的滴定曲线_______ ;请根据此滴定曲线选择一种最佳酸碱指示剂,并简述做出选择的理由_______ 。有关指示剂的变色范围如下:甲基橙(pH3.1~4.4),溴甲酚绿(pH3.8~5.4),酚酞(pH8.0~10.0)。
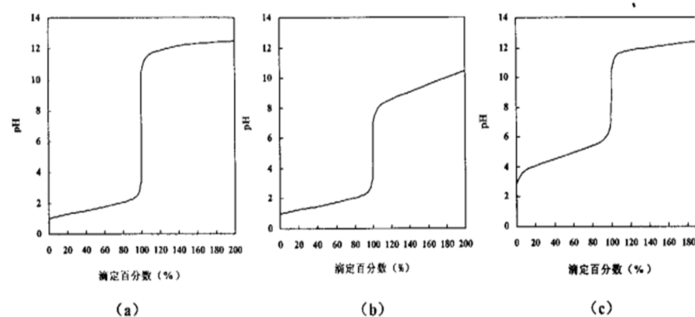
(2)在实验2中,加NaHSO3还原V10O ,反应完全后需要加热煮沸15分钟。煮沸的目的是
,反应完全后需要加热煮沸15分钟。煮沸的目的是_______ ?写出KMnO4滴定反应的离子方程式_______ 。
(3)根据实验结果,计算试样A中NH 和V10O
和V10O 的质量分数,确定A的化学式
的质量分数,确定A的化学式_______ (x和n取整数)。
 、HV10O
、HV10O 和H2V10O
和H2V10O 等。将NH4VO3溶于弱酸性介质中,加入乙醇可以得到橙色的十钒酸铵晶体(NH4)xH6-xV10O28·nH2O(用A表示)。元素分析结果表明,A中氢的质量分数为3.13%。用下述实验对该化合物进行分析,以确定其组成。
等。将NH4VO3溶于弱酸性介质中,加入乙醇可以得到橙色的十钒酸铵晶体(NH4)xH6-xV10O28·nH2O(用A表示)。元素分析结果表明,A中氢的质量分数为3.13%。用下述实验对该化合物进行分析,以确定其组成。实验1:准确称取0.9291gA于三颈瓶中,加入100mL蒸馏水和150mL20%NaOH溶液,加热煮沸,生成的氨气用50.00mL0.1000mol·L-1HCl标准溶液吸收。加入酸碱指示剂,用0.1000mol·L-1NaOH标准溶液滴定剩余的HCl标准溶液,终点时消耗19.88mLNaOH标准溶液。
实验2:准确称取0.3097gA于锥形瓶中,加入40mL1.5mol·L-1H2SO4,微热使之溶解。加入50mL蒸馏水和1gNaHSO3,搅拌5分钟,便反应完全,五价钒被还原成四价。加热煮沸15分钟,然后用0.02005mol·L-1KMnO4标准溶液滴定,终点时消耗25.10mLKMnO4标准溶液。
(1)如图为滴定曲线图,请回答哪一个图为实验1的滴定曲线

(2)在实验2中,加NaHSO3还原V10O
 ,反应完全后需要加热煮沸15分钟。煮沸的目的是
,反应完全后需要加热煮沸15分钟。煮沸的目的是(3)根据实验结果,计算试样A中NH
 和V10O
和V10O 的质量分数,确定A的化学式
的质量分数,确定A的化学式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】镍矿石中一般含有钴,利用镍生产过程中产生的含钴废渣提取钴氧化物具有重要的意义。含钴废渣中含有Co(OH)3、Ni(OH)3、Fe(OH)3以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下:

已知:黄铁钒钠[NaFe3(SO4)2(OH)6]具有沉淀颗粒大、沉淀速度快、容易过滤等特点,常用于除铁,黄钠铁矾沉淀的合适pH是1.5~2.0。
(1)写出酸浸步骤溶解Co(OH)3反应的离子方程式_______ 。
(2)黄钠铁矾除铁步骤中加入NaClO3的作用是_______ ,加入Na2CO3的作用是_______ 。
(3)除杂是用NH4F除去氯化钴溶液中少量的Ca2+、Mg2+,为了使除杂后溶液中Ca2+、Mg2+均小于0.1g/L,溶液中的c(F-)至少为_______ 。(已知:Ksp(CaF2)=1.44×10-10,Ksp(MgF2)=7.42×10-11)
(4)沉钴得到的是CoC2O4·2H2O,热重分析实验发现,将该固体在空气中加热会发生如下分解过程:
若制备过程中煅烧控制温度约为340℃,则发生反应的化学方程式是:_______ 。

已知:黄铁钒钠[NaFe3(SO4)2(OH)6]具有沉淀颗粒大、沉淀速度快、容易过滤等特点,常用于除铁,黄钠铁矾沉淀的合适pH是1.5~2.0。
(1)写出酸浸步骤溶解Co(OH)3反应的离子方程式
(2)黄钠铁矾除铁步骤中加入NaClO3的作用是
(3)除杂是用NH4F除去氯化钴溶液中少量的Ca2+、Mg2+,为了使除杂后溶液中Ca2+、Mg2+均小于0.1g/L,溶液中的c(F-)至少为
(4)沉钴得到的是CoC2O4·2H2O,热重分析实验发现,将该固体在空气中加热会发生如下分解过程:
| 温度范围(℃) | 150~250 | 250~300 | 910~950 |
| 失重率(%) | 19.7 | 36.4 | 2.9 |
若制备过程中煅烧控制温度约为340℃,则发生反应的化学方程式是:
您最近一年使用:0次



