设计出燃料电池使汽油氧化直接产生电流是对世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子。回答如下问题:
(1)以丁烷代表汽油,这个电池放电时发生的化学反应的化学方程式是:_______
(2)这个电池的正极发生的反应是:_______ 负极发生的反应是:_______ 固体电解质里的O2-的移动方向是:_______ 向外电路释放电子的电极是:_______
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:_______
(4)你认为在ZrO2晶体里掺杂Y2O3用Y3+代替晶体里部分的Zr4+对提高固体电解质的导电能力会起什么作用?其可能的原因是什么?_______
(5)汽油燃料电池最大的障碍是氧化反应不完全产生_______ 堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间,正是新一代化学家的历史使命。
(1)以丁烷代表汽油,这个电池放电时发生的化学反应的化学方程式是:
(2)这个电池的正极发生的反应是:
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:
(4)你认为在ZrO2晶体里掺杂Y2O3用Y3+代替晶体里部分的Zr4+对提高固体电解质的导电能力会起什么作用?其可能的原因是什么?
(5)汽油燃料电池最大的障碍是氧化反应不完全产生
更新时间:2021-07-16 07:57:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:
A极:2H2+2O2--4e-===2H2O;B极:O2+4e-===2O2-
则A极是电池的________ 极;电子从该极________ (填“流入”或“流出”)。
(2)有人以化学反应:2Zn+O2+4H+===2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是________ ,发生的电极反应为__________________ 。
A极:2H2+2O2--4e-===2H2O;B极:O2+4e-===2O2-
则A极是电池的
(2)有人以化学反应:2Zn+O2+4H+===2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)画出原电池装置图_______ ,该电池的负极发生_______ 反应(填“氧化”或“还原”),电解质溶液是_______ ;
(2)放电时银离子向__________ (填“正极”或“负极”),正极上出现的现象是________ 。
(3)当反应进行一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了电子数目是___________ 。
(1)画出原电池装置图
(2)放电时银离子向
(3)当反应进行一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了电子数目是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是某同学设计的一个简易的原电池装置,请回答下列问题。

(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为_____ ,当有1.6g负极材料溶解时,转移的电子为_____ mol。
(2)若a电极材料为铁、b溶液为稀硫酸,电流表的指针也会偏转,则电子的流向为_____ →_____ (填电极材料,下同),溶液中的SO 向
向_____ 极移动。
(3)氢氧燃料电池已应用于航天飞机。“这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2=2H2O,则正极为_____ 。

(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为
(2)若a电极材料为铁、b溶液为稀硫酸,电流表的指针也会偏转,则电子的流向为
 向
向(3)氢氧燃料电池已应用于航天飞机。“这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2=2H2O,则正极为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)今有氢氧燃料电池,则正极通入的气体是________ ,负极通入的气体是________ ,电解质溶液为稀硫酸时,电极反应式为:正极____________ ;负极___________ ,电池的总反应式为__________ ;
(2)如把H2改为甲烷、KOH作导电物质,则电极反应式为:负极___________ 。
(2)如把H2改为甲烷、KOH作导电物质,则电极反应式为:负极
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】空军通信卫星电源是以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2为原料的燃料电池,电极材料均采用Pt,其工作原理如图所示。回答下列问题:

(1)该燃料电池能量转化的主要形式是__ ,外电路中电子的流动方向为___ (填标号)。
①电极a→用电器→电极b;②电极b→用电器→电极a;③电极a→离子交换膜→电极b;④电极b→离子交换膜→电极a。
(2)电极a上的电极反应式为___ 。
(3)图中离子交换膜为___ (填“阴”或“阳”)离子交换膜,电池工作时,Na+往___ (填“电极a”或“电极b”)方向迁移。
(4)每生成0.01molOH-,转移的电子数为__ NA,需要H2O2溶液(质量分数2%)的质量为___ g。
(5)若用LiAlH4代替NaBH4进行上述反应,则该电池的总反应为___ 。

(1)该燃料电池能量转化的主要形式是
①电极a→用电器→电极b;②电极b→用电器→电极a;③电极a→离子交换膜→电极b;④电极b→离子交换膜→电极a。
(2)电极a上的电极反应式为
(3)图中离子交换膜为
(4)每生成0.01molOH-,转移的电子数为
(5)若用LiAlH4代替NaBH4进行上述反应,则该电池的总反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.高铁酸盐在能源、环保等方面有着广泛的用途。高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。下图是高铁电池的模拟实验装置:
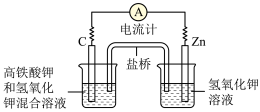
(1)该电池放电时正极的电极反应式为____ 。
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向_____ (填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向_____ (填“左”或“右”)移动。
(3)下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有____ 。

II.电解制取KIO3
电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应3I2+6KOH= 5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为____ ;电解过程中阴极附近溶液pH____ (填“变大”“变小”或“不变”)。

(1)该电池放电时正极的电极反应式为
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
(3)下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

II.电解制取KIO3
电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应3I2+6KOH= 5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电池的发明和应用是化学家们对人类社会的重要贡献之一。
每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如下图所示。
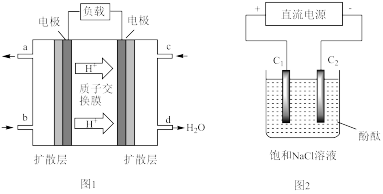
(1)甲烷燃料应从__________ 口通入(图1),发生的电极反应式 __________________ 。
(2)以石墨做电极电解饱和食盐水,如下图2所示。电解开始后在__________ 的周围(填“阴极”或“阳极”)先出现红色,该极的电极反应式为_______________ 。.
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是____ 。
a.利用阳极泥可回收Ag、Pt、Au等金属
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.电能全部转化为化学能
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。
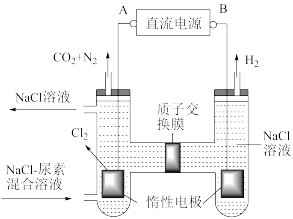
①电源的正极为________ (填“A”或“B”)。
②电解结束后,阴极室溶液的pH与电解前相比将________ (填“增大”、“减小”、“不变”);若两极共收集到气体6.72 L(标准状况),则除去的尿素为________ g(忽略气体的溶解)。
每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如下图所示。

(1)甲烷燃料应从
(2)以石墨做电极电解饱和食盐水,如下图2所示。电解开始后在
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.利用阳极泥可回收Ag、Pt、Au等金属
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.电能全部转化为化学能
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。

①电源的正极为
②电解结束后,阴极室溶液的pH与电解前相比将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】用CH4和O2组合形成的质子交换膜燃料电池的结构如图丙:
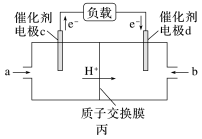
(1)电极c为电子_______ (填流入或流出)的一极,H+移向_______ (填正极或负极)。
(2)气体a为_______ (CH4或O2),若线路中转移2 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为_______ L。

(1)电极c为电子
(2)气体a为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】燃料电池具有能量利用率高、可连续使用和污染轻等优点,已成为一种发展前景十分广阔的化学电源。氢氧燃料电池是目前最成熟的燃料电池,它可以使用不同的电解质,如酸式、碱式、熔融碳酸盐、固体电解质等。回答以下问题。
(1)通入氧气的一极为___________ 极,若电解质溶液为硫酸溶液,负极反应式为____________ ,若电解质溶液为KOH溶液,正极反应式为____________ 。
(2)若将氢气改为CH4,电解质溶液为KOH溶液,此时负极反应式为__________ ,一段时间后,电解质溶液的OH-的浓度将____________ (填“增大”“减小”或“不变”)。
(3)肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%〜30%的KOH溶液。已知N2H4燃烧产物之一为空气中含量最高的一种气体。肼-空气燃料电池放电时负极的电极反应式为___________________ .
(1)通入氧气的一极为
(2)若将氢气改为CH4,电解质溶液为KOH溶液,此时负极反应式为
(3)肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%〜30%的KOH溶液。已知N2H4燃烧产物之一为空气中含量最高的一种气体。肼-空气燃料电池放电时负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某远洋船只的船壳浸水面积为4500m2,与锌块相连来保护,额定电流密度为150mA/m2,预定保护期限2年,可选择的锌块有两种,每块的质量分别为15.7kg和25.9kg,通过每块锌块的电流强度分别为0.92A和1.2A.计算说明,为达到上述保护船体的目的,最少各需几块锌块_______ ?用哪种锌块更合理___ ?为什么_____ ?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高铁酸钾(K2FeO4)是一种新型选择性氧化剂和超铁电池的正极材料,在水处理、有机合成、电池工业等方面展现出广阔的应用前景。早在1951年,Thompson等已成功地利用化学方法合成了纯度为97%~99%的K2FeO4。已知相关物质的标准电极电势如下:
 +8H++3e-→Fe3++4H2O
+8H++3e-→Fe3++4H2O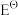 =2.20V
=2.20V
 +4H2O+3e-→Fe(OH)3+5OH-
+4H2O+3e-→Fe(OH)3+5OH-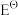 =0.72V
=0.72V
2HClO+2H++2e-→Cl2+2H2O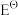 =1.611V。
=1.611V。
ClO-+H2O+2e-→Cl-+2OH-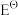 =0.81V
=0.81V
Cl2+2e-→2Cl-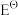 =1.358V
=1.358V
(1)试写出以Fe(NO3)3为铁源、KClO为氧化剂,在KOH溶液中制备K2FeO4的离子方程式_______ 。
(2)研究发现,Fe(OH)3能催化溶液中K2FeO4的分解。在相同条件下,分别以Fe(NO3)3和K3[FeF6]为原料制备K2FeO4,哪种铁源制备K2FeO4的产率较高______ ?简述理由_______ 。
(3)高铁酸在水溶液中有4种形体,其酸常数为pKa1=1.6、pKa2=3.5、pKa3=7.3.pH=1.0的该溶液4种形体中哪2种是主要的?写出它们的化学式_______ 。
(4)K2FeO4在KOH溶液中可将甲苯氧化成苯甲醛, 转化为红棕色沉淀和绿色溶液(绿色是由
转化为红棕色沉淀和绿色溶液(绿色是由 呈现的),该绿色溶液与适量S2-发生氧化还原反应生成深色沉淀,组成分析发现该沉淀为3种物质的混合物,写出它们的化学式
呈现的),该绿色溶液与适量S2-发生氧化还原反应生成深色沉淀,组成分析发现该沉淀为3种物质的混合物,写出它们的化学式________ 。
(5)以K2FeO4作为锂离子电池的正极材料,可嵌入/脱嵌Li+离子。1.00gK2FeO4的理论容量为406mAh,请通过计算写出K2FeO4可逆嵌入/脱嵌Li+的方程式__________ 。
 +8H++3e-→Fe3++4H2O
+8H++3e-→Fe3++4H2O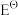 =2.20V
=2.20V +4H2O+3e-→Fe(OH)3+5OH-
+4H2O+3e-→Fe(OH)3+5OH-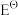 =0.72V
=0.72V2HClO+2H++2e-→Cl2+2H2O
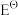 =1.611V。
=1.611V。ClO-+H2O+2e-→Cl-+2OH-
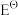 =0.81V
=0.81VCl2+2e-→2Cl-
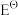 =1.358V
=1.358V(1)试写出以Fe(NO3)3为铁源、KClO为氧化剂,在KOH溶液中制备K2FeO4的离子方程式
(2)研究发现,Fe(OH)3能催化溶液中K2FeO4的分解。在相同条件下,分别以Fe(NO3)3和K3[FeF6]为原料制备K2FeO4,哪种铁源制备K2FeO4的产率较高
(3)高铁酸在水溶液中有4种形体,其酸常数为pKa1=1.6、pKa2=3.5、pKa3=7.3.pH=1.0的该溶液4种形体中哪2种是主要的?写出它们的化学式
(4)K2FeO4在KOH溶液中可将甲苯氧化成苯甲醛,
 转化为红棕色沉淀和绿色溶液(绿色是由
转化为红棕色沉淀和绿色溶液(绿色是由 呈现的),该绿色溶液与适量S2-发生氧化还原反应生成深色沉淀,组成分析发现该沉淀为3种物质的混合物,写出它们的化学式
呈现的),该绿色溶液与适量S2-发生氧化还原反应生成深色沉淀,组成分析发现该沉淀为3种物质的混合物,写出它们的化学式(5)以K2FeO4作为锂离子电池的正极材料,可嵌入/脱嵌Li+离子。1.00gK2FeO4的理论容量为406mAh,请通过计算写出K2FeO4可逆嵌入/脱嵌Li+的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图是一种正在投入生产的大型蓄电系统。左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2 和NaBr3, 放。电后,分别变为Na2S4 和NaBr。
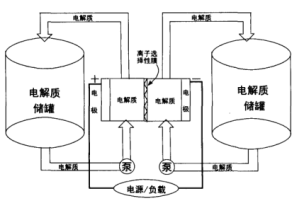
(1)左、右储罐中的电解质分别为:
左:___________ ; 右:___________ 。
(2)写出电池充电时,阳极和阴极的电极反应。
阳极:___________ ; 阴极:___________ 。
(3)写出电池充、放电的反应方程式_______ 。
(4)指出在充电过程中钠离子通过膜的流向_______ 。

(1)左、右储罐中的电解质分别为:
左:
(2)写出电池充电时,阳极和阴极的电极反应。
阳极:
(3)写出电池充、放电的反应方程式
(4)指出在充电过程中钠离子通过膜的流向
您最近一年使用:0次



