金属簇合物是含有金属-金属键、具有精确组成的一类物质,常表现出优美的化学结构和独特的光物理性能。
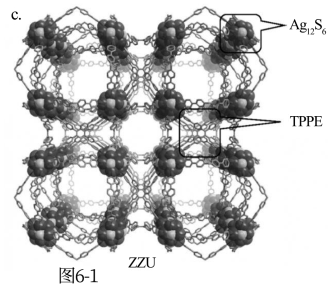
图6-1-a示出一种电中性银硫簇(简记为Ag12S6)的结构,包含12个银原子和6个硫原子(图中未区分原子大小)。6个银原子位于同一平面(称为赤道面),形成正六边形,彼此之间不成键。赤道面上、下方各有3个银原子,皆呈正三角形排布,彼此之间形成Ag-Ag键,并分别与赤道面。上的两个银原子形成Ag-Ag键。6个硫原子的位置如图所示。

(1)计算Ag12S6中Ag-Ag键的个数________ 。
(2)计算Ag12S6中三角形面的个数___________ 。
(3)Ag12S6的硫原子来自于叔丁巯基,银为正一价。在Ag12S6上还连接有若干个CF3COO-,计算CF3COO-的个数__________ 。
(4)聚集诱导发光(AIE)现象是一种由中国科学家首先发现的光致发光现象。具有AIE特性的有机分子在聚集状态下表现出远强于分散状态的光致发光性能。四苯乙烯(TPE)是一种典型的AIE分子。将TPE完全溶解于乙醇中,分别取等量的该溶液加入到等体积的水和甲苯中,判断哪一个体系的光致发光较强并简要解释原因__________ 。
(5)利用上述Ag12S6和图6-1-b所示的TPPE配体组装,得到一种晶体框架材料ZZU(图6-1-c)。ZZU中,每个Ag12S6连接6个TPPE,每个TPPE连接4个Ag12S6.ZZU属于立方晶系,正当晶胞参数a=4.209mm,密度为0.618g·cm-3.ZZU沿着晶轴方向的投影如图6-2所示,在图6-2中用粗虚线画出ZZU正当晶胞的投影________ 。计算每个正当晶胞中Ag12S6和TPPE的数目_______ 、________ 。
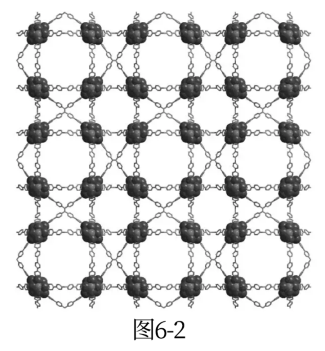
图6-1-a示出一种电中性银硫簇(简记为Ag12S6)的结构,包含12个银原子和6个硫原子(图中未区分原子大小)。6个银原子位于同一平面(称为赤道面),形成正六边形,彼此之间不成键。赤道面上、下方各有3个银原子,皆呈正三角形排布,彼此之间形成Ag-Ag键,并分别与赤道面。上的两个银原子形成Ag-Ag键。6个硫原子的位置如图所示。


(1)计算Ag12S6中Ag-Ag键的个数
(2)计算Ag12S6中三角形面的个数
(3)Ag12S6的硫原子来自于叔丁巯基,银为正一价。在Ag12S6上还连接有若干个CF3COO-,计算CF3COO-的个数
(4)聚集诱导发光(AIE)现象是一种由中国科学家首先发现的光致发光现象。具有AIE特性的有机分子在聚集状态下表现出远强于分散状态的光致发光性能。四苯乙烯(TPE)是一种典型的AIE分子。将TPE完全溶解于乙醇中,分别取等量的该溶液加入到等体积的水和甲苯中,判断哪一个体系的光致发光较强并简要解释原因
(5)利用上述Ag12S6和图6-1-b所示的TPPE配体组装,得到一种晶体框架材料ZZU(图6-1-c)。ZZU中,每个Ag12S6连接6个TPPE,每个TPPE连接4个Ag12S6.ZZU属于立方晶系,正当晶胞参数a=4.209mm,密度为0.618g·cm-3.ZZU沿着晶轴方向的投影如图6-2所示,在图6-2中用粗虚线画出ZZU正当晶胞的投影

2019高三·全国·竞赛 查看更多[1]
更新时间:2021-07-14 06:34:07
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】LiFePO4、LiPF6原材料丰富,对环境污染性较少、安全稳定,是锂离子电池理想的正极材料和电解液。回答下列问题:
(1)HF、HCl、HBr的酸性由强到弱的顺序为___________ (填化学式,下同);沸点由高到低的顺序为___________ ;还原性由强到弱的顺序为___________ 。
(2)Li2O为立方晶系晶体,离子位置按图示坐标系为:Li+:(0.25,0.25,0.25);(0.25,0.75,0.25);(0.75,0.25,0.25);(0.75,0.75,0.25);…O2-:(0,0,0);(0.5,0.5,0);(0.5,0,0.5);(0,0.5,0.5);则Li2O晶胞沿z轴投影的俯视图(其中表示“ ”Li+,“
”Li+,“ ”表示O2-)为___________。
”表示O2-)为___________。

(3)亚磷酸(H3PO3)中心原子磷的配位数为4,则亚磷酸为___________ 元酸。磷酸通过分子间脱水缩合形成多磷酸,如:

如果有n个磷酸分子间脱水形成环状的多磷酸,则该环状的多磷酸的化学式为___________ 。
(4)一种铁基超导化合物的晶胞结构如图,则该超导化合物的化学式为___________ 。

已知晶胞边长为x pm,高为y pm,α=β=γ=90°,化合物的摩尔质量为M g·mol–1,设NA为阿伏加德罗常数的值,则该晶体的密度为___________ g·cm–3(用代数式表示)。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。该晶胞中,1号Fe原子的分数坐标为(0, ,
, ),3号In原子的分数坐标为(0,
),3号In原子的分数坐标为(0, ,
, ),则2号S原子的分数坐标为
),则2号S原子的分数坐标为___________ 。
(1)HF、HCl、HBr的酸性由强到弱的顺序为
(2)Li2O为立方晶系晶体,离子位置按图示坐标系为:Li+:(0.25,0.25,0.25);(0.25,0.75,0.25);(0.75,0.25,0.25);(0.75,0.75,0.25);…O2-:(0,0,0);(0.5,0.5,0);(0.5,0,0.5);(0,0.5,0.5);则Li2O晶胞沿z轴投影的俯视图(其中表示“
 ”Li+,“
”Li+,“ ”表示O2-)为___________。
”表示O2-)为___________。
A. | B. | C. | D. |

如果有n个磷酸分子间脱水形成环状的多磷酸,则该环状的多磷酸的化学式为
(4)一种铁基超导化合物的晶胞结构如图,则该超导化合物的化学式为

已知晶胞边长为x pm,高为y pm,α=β=γ=90°,化合物的摩尔质量为M g·mol–1,设NA为阿伏加德罗常数的值,则该晶体的密度为
 ,
, ),3号In原子的分数坐标为(0,
),3号In原子的分数坐标为(0, ,
, ),则2号S原子的分数坐标为
),则2号S原子的分数坐标为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】铋 的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为
的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含
,含 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下: 易水解,
易水解, 难溶于冷水。
难溶于冷水。
ii.“氧化浸取”时,铋元素转化为 ,硫元素转化为硫单质。
,硫元素转化为硫单质。
iii
 。
。
回答下列问题。
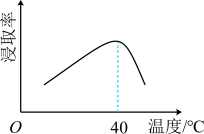
(1)滤渣1的主要成分为______ 。为提高“浸取”速率,采取的措施有:升高温度、__________________ (写出一条)。辉铋矿浸取率随温度的变化曲线如图,高于40℃时浸取率快速下降,其可能的原因是______________________________ 。 和
和 物质的量之比为
物质的量之比为______ 。
(3)“除铜”时发生反应:
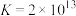 ,则
,则
______ 。
(4)“转化”时,生成 的离子方程式为
的离子方程式为________________________ 。
(5)取 产品
产品 ,加入足量稀硫酸和
,加入足量稀硫酸和 稀溶液使其完全反应,再用
稀溶液使其完全反应,再用
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗
,当溶液紫红色恰好褪去时,消耗 标准溶液。该
标准溶液。该
产品的纯度为______ (用含w,a、b的代数式表示)。
(6)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:__________________ 。
② 的配位数为
的配位数为______ 。
③该晶胞参数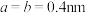 ,
, ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为__________________  (列出计算式)。
(列出计算式)。
 的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为
的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含
,含 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下: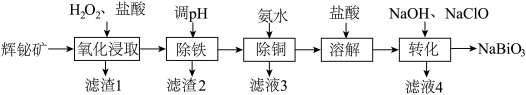
 易水解,
易水解, 难溶于冷水。
难溶于冷水。ii.“氧化浸取”时,铋元素转化为
 ,硫元素转化为硫单质。
,硫元素转化为硫单质。iii

 。
。回答下列问题。
(1)滤渣1的主要成分为
 和
和 物质的量之比为
物质的量之比为(3)“除铜”时发生反应:

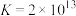 ,则
,则
(4)“转化”时,生成
 的离子方程式为
的离子方程式为(5)取
 产品
产品 ,加入足量稀硫酸和
,加入足量稀硫酸和 稀溶液使其完全反应,再用
稀溶液使其完全反应,再用
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗
,当溶液紫红色恰好褪去时,消耗 标准溶液。该
标准溶液。该产品的纯度为
(6)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
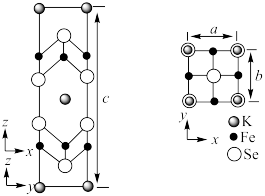
②
 的配位数为
的配位数为③该晶胞参数
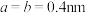 ,
, ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】有E、Q、T、X、Z五种前四周期元素,原子序数 。E、Q、T三种元素的基态原子具有相同的能层和能级,且第一电离能
。E、Q、T三种元素的基态原子具有相同的能层和能级,且第一电离能 ,其中基态Q原子的2p轨道处于半充满状态,且
,其中基态Q原子的2p轨道处于半充满状态,且 与
与 具有相同的原子数和价电子数。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
具有相同的原子数和价电子数。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)写出 的电子式:
的电子式:_______ ,基态Z原子的核外电子排布式为_______ 。
(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有_______ 、_______ 。
(3)化合物甲由T、X两元素组成,其晶胞如下图所示,则甲的化学式为_______ 。

(4)化合物乙的晶胞如下图所示,乙由E、Q两元素组成,硬度超过金刚石。

①乙的晶体类型为_______ ,其硬度超过金刚石的原因是_______ 。
②乙的晶体中E、Q两种元素原子的杂化方式均为_______ 。
 。E、Q、T三种元素的基态原子具有相同的能层和能级,且第一电离能
。E、Q、T三种元素的基态原子具有相同的能层和能级,且第一电离能 ,其中基态Q原子的2p轨道处于半充满状态,且
,其中基态Q原子的2p轨道处于半充满状态,且 与
与 具有相同的原子数和价电子数。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
具有相同的原子数和价电子数。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):(1)写出
 的电子式:
的电子式:(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有
(3)化合物甲由T、X两元素组成,其晶胞如下图所示,则甲的化学式为

(4)化合物乙的晶胞如下图所示,乙由E、Q两元素组成,硬度超过金刚石。

①乙的晶体类型为
②乙的晶体中E、Q两种元素原子的杂化方式均为
您最近一年使用:0次
【推荐1】水是自然界中普遍存在的一种物质,也是维持生命活动所必需的一种物质。
信息一:水的性质存在许多反常现象,如固态密度小于液态密度使冰浮在水面上,沸点相对较高使水在常温常压下呈液态等。
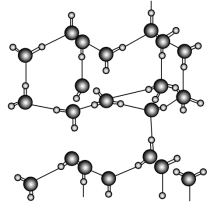
信息二:在20 ℃、1个大气压下,水可以结成冰,称为“热冰”(如下图):
试根据以上信息回答下列问题:
(1)s轨道与s轨道重叠形成的共价键可用符号表示为ds-s,p轨道以“头碰头”方式重叠形成的共价键可用符号表示为dp-p,则H2O分子中含有的共价键用符号表示为________ 。
(2)下列物质熔化时,所克服的微粒间的作用与“热冰”熔化时所克服的作用类型完全相同的是________ 。
A 金刚石 B 干冰 C 食盐 D 固态氨
(3)已知:2H2O=H3O++OH-,H3O+的立体构型是________ ,H3O+中含有一种特殊的共价键是________ 。
(4)根据等电子原理,写出短周期元素原子形成的与H3O+互为等电子体的分子或离子________ 。
(5)水的分解温度远高于其沸点的原因是________________ 。
(6)从结构的角度分析固态水(冰)的密度小于液态水的密度的原因是_______ 。
信息一:水的性质存在许多反常现象,如固态密度小于液态密度使冰浮在水面上,沸点相对较高使水在常温常压下呈液态等。
信息二:在20 ℃、1个大气压下,水可以结成冰,称为“热冰”(如下图):

试根据以上信息回答下列问题:
(1)s轨道与s轨道重叠形成的共价键可用符号表示为ds-s,p轨道以“头碰头”方式重叠形成的共价键可用符号表示为dp-p,则H2O分子中含有的共价键用符号表示为
(2)下列物质熔化时,所克服的微粒间的作用与“热冰”熔化时所克服的作用类型完全相同的是
A 金刚石 B 干冰 C 食盐 D 固态氨
(3)已知:2H2O=H3O++OH-,H3O+的立体构型是
(4)根据等电子原理,写出短周期元素原子形成的与H3O+互为等电子体的分子或离子
(5)水的分解温度远高于其沸点的原因是
(6)从结构的角度分析固态水(冰)的密度小于液态水的密度的原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】GaN是制造5G芯片的材料,氮化镓和氮化铝LED可发出紫外光。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]____ 。
(2)根据元素周期律,元素的电负性Ga____ (填“大于”或“小于”,下同)As。
(3)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为____ ,其中的阴离子的空间构型为____ 。
(4)组成相似的CaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是________ 。
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为___ ;紧邻的As原子之间的距离为b,紧邻的As、Ca原子之间的距离为d,则b:d=____ ,该晶胞的密度为__ g ▪cm-3。(阿伏加 德罗常数用NA表示)

(1)基态Ga原子的核外电子排布式为[Ar]
(2)根据元素周期律,元素的电负性Ga
(3)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为
(4)组成相似的CaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】2020年11月我国载人潜水器“奋斗者”号在马里亚纳海沟完成万米深潜,轻且坚固的球形载人舱由国产新型钛合金材料( )制造。
)制造。
(1)钛在元素周期表中位于____ 区。
(2)高温条件下,可用 和
和 反应制取
反应制取 。
。
① 的熔点为
的熔点为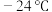 ,易溶于乙醇等有机溶剂,说明
,易溶于乙醇等有机溶剂,说明 属于
属于___ 晶体; 的熔点为
的熔点为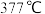 ,
, 的熔点明显高于
的熔点明显高于 的原因是
的原因是___ 。
②用锌还原 的盐酸溶液,经后续处理可制得配合物
的盐酸溶液,经后续处理可制得配合物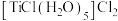 ,
, 该配合物中含
该配合物中含 键
键___  。
。
(3) 的天然晶体最常见的有两种:金红石型和锐钛型。
的天然晶体最常见的有两种:金红石型和锐钛型。
①金红石型 是最稳定的一种晶体,其晶胞结构如图所示,则黑球表示
是最稳定的一种晶体,其晶胞结构如图所示,则黑球表示___ 原子。

②研究发现,天然锐钛型 晶体中掺杂一定量的氮原子后生成
晶体中掺杂一定量的氮原子后生成 对可见光具有活性,掺杂前后晶胞的变化如图所示:
对可见光具有活性,掺杂前后晶胞的变化如图所示:
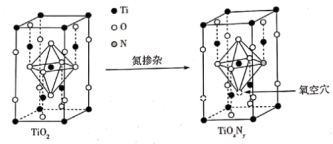
 晶胞中
晶胞中 位于六个
位于六个 围成的正八面体的中心,则该晶胞中含有
围成的正八面体的中心,则该晶胞中含有___ 个这样的正八面体;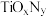 晶胞中x=
晶胞中x=___ 。
 )制造。
)制造。(1)钛在元素周期表中位于
(2)高温条件下,可用
 和
和 反应制取
反应制取 。
。①
 的熔点为
的熔点为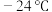 ,易溶于乙醇等有机溶剂,说明
,易溶于乙醇等有机溶剂,说明 属于
属于 的熔点为
的熔点为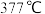 ,
, 的熔点明显高于
的熔点明显高于 的原因是
的原因是②用锌还原
 的盐酸溶液,经后续处理可制得配合物
的盐酸溶液,经后续处理可制得配合物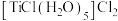 ,
, 该配合物中含
该配合物中含 键
键 。
。(3)
 的天然晶体最常见的有两种:金红石型和锐钛型。
的天然晶体最常见的有两种:金红石型和锐钛型。①金红石型
 是最稳定的一种晶体,其晶胞结构如图所示,则黑球表示
是最稳定的一种晶体,其晶胞结构如图所示,则黑球表示
②研究发现,天然锐钛型
 晶体中掺杂一定量的氮原子后生成
晶体中掺杂一定量的氮原子后生成 对可见光具有活性,掺杂前后晶胞的变化如图所示:
对可见光具有活性,掺杂前后晶胞的变化如图所示:
 晶胞中
晶胞中 位于六个
位于六个 围成的正八面体的中心,则该晶胞中含有
围成的正八面体的中心,则该晶胞中含有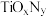 晶胞中x=
晶胞中x=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】(1)下列玻璃仪器的洗涤方法不涉及氧化还原反应的是_____
A.附有银镜的试管用稀硝酸清洗
B.附有油脂的烧杯用热纯碱溶液清洗
C.附有MnO2的烧瓶用热的浓盐酸清洗
D.附有硫的燃烧匙用热的烧碱溶液清洗
(2)室温下,某兴趣小组用下图装置在通风橱中进行如下实验:
下列说法正确的是_____
A.试管I中浅棕色气体为NO2,由硝酸还原生成
B.等量的Cu完全溶解时,I中消耗的HNO3更多
C.换成Fe之后重复实验,依然是试管II中反应更剧烈
D.试管II中反应后溶液颜色与试管I中的不同,是由于溶有NO2
(3)溶液的导电性与溶液中的离子的种类和浓度有关,下列各组实验过程的被滴加溶液导电性变化与如图对应的是_____
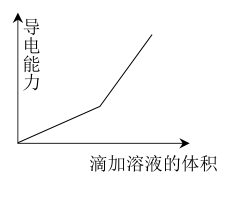
A.向Ba(OH)2溶液中滴加H2SO4溶液
B.向醋酸溶液中滴加NaOH溶液
C.向糖水中滴加NaCl溶液。
D.向盐酸中滴加氨水
(4)卤化钠(NaX)和四卤化钛(TiX4) 的熔点如图所示。下列判断不正确的是_____
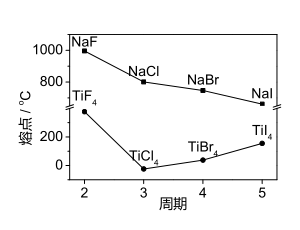
A. TiF4 的熔点反常升高是由于氢键的作用
B. NaX随X-半径增大,离子键减弱。
C. NaX均为离子化合物
D. TiCl4 为共价化合物
(5)如图所示,钠-氯化镍电池是以β-Al2O3(Al2O3· xNa2O)作为固体电解质构成的一种新型高能电池(2Na + NiCl2 Ni+2NaCl),下列关于该电池的叙述错误的是
Ni+2NaCl),下列关于该电池的叙述错误的是_____
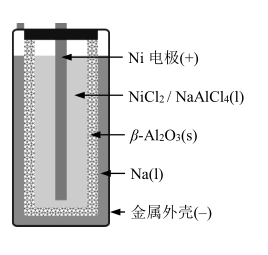
A.放电时NaCl在熔融电解质中生成
B.充电时阴极反应: Na++e-= Na 。
C.氯离子通过β-Al2O3 (s)在两电极间移动
D.如果电池过度放电,AlCl 可能被还原
可能被还原
(6)最近我国科学家预测并据此合成了新型碳材料: T-碳。可以看做金刚石结构中的一个碳原子被四个碳原子构成一个正四面体结构单元替代(如下图所示,所有小球都代表碳原子)。下列说法正确的是_____

A.T-碳与石墨、金刚石互为同素异形体
B.T-碳晶体与金刚石晶体类似,属于原子晶体。
C.T-碳晶体和金刚石晶体中含有的化学键不同
D.T-碳与金刚石中的碳原子都采取杂化方式不同
A.附有银镜的试管用稀硝酸清洗
B.附有油脂的烧杯用热纯碱溶液清洗
C.附有MnO2的烧瓶用热的浓盐酸清洗
D.附有硫的燃烧匙用热的烧碱溶液清洗
(2)室温下,某兴趣小组用下图装置在通风橱中进行如下实验:
| 实验 | 现象 |
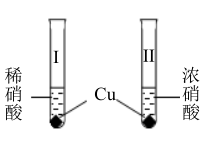 | 试管I中开始无明显现象,逐渐有微小气泡生成,越来越剧烈,液面上方出现浅棕色气体,溶液呈蓝色。 |
| 试管II中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色;之后向绿色溶液中持续通入N2,溶液变为蓝色。 |
下列说法正确的是
A.试管I中浅棕色气体为NO2,由硝酸还原生成
B.等量的Cu完全溶解时,I中消耗的HNO3更多
C.换成Fe之后重复实验,依然是试管II中反应更剧烈
D.试管II中反应后溶液颜色与试管I中的不同,是由于溶有NO2
(3)溶液的导电性与溶液中的离子的种类和浓度有关,下列各组实验过程的被滴加溶液导电性变化与如图对应的是

A.向Ba(OH)2溶液中滴加H2SO4溶液
B.向醋酸溶液中滴加NaOH溶液
C.向糖水中滴加NaCl溶液。
D.向盐酸中滴加氨水
(4)卤化钠(NaX)和四卤化钛(TiX4) 的熔点如图所示。下列判断不正确的是

A. TiF4 的熔点反常升高是由于氢键的作用
B. NaX随X-半径增大,离子键减弱。
C. NaX均为离子化合物
D. TiCl4 为共价化合物
(5)如图所示,钠-氯化镍电池是以β-Al2O3(Al2O3· xNa2O)作为固体电解质构成的一种新型高能电池(2Na + NiCl2
 Ni+2NaCl),下列关于该电池的叙述错误的是
Ni+2NaCl),下列关于该电池的叙述错误的是
A.放电时NaCl在熔融电解质中生成
B.充电时阴极反应: Na++e-= Na 。
C.氯离子通过β-Al2O3 (s)在两电极间移动
D.如果电池过度放电,AlCl
 可能被还原
可能被还原(6)最近我国科学家预测并据此合成了新型碳材料: T-碳。可以看做金刚石结构中的一个碳原子被四个碳原子构成一个正四面体结构单元替代(如下图所示,所有小球都代表碳原子)。下列说法正确的是

A.T-碳与石墨、金刚石互为同素异形体
B.T-碳晶体与金刚石晶体类似,属于原子晶体。
C.T-碳晶体和金刚石晶体中含有的化学键不同
D.T-碳与金刚石中的碳原子都采取杂化方式不同
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】ⅥB族元素有着独特的性质,其中的多酸化合物可谓是引人入胜。
(1)请写出Cr、Mo、W的价电子组态。(如Fe的为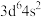 )
)_______
(2)请写出铬酸根离子在酸性水溶液的条件下聚合成重铬酸根离子的可逆反应方程式。_______
(3)当钼酸盐水溶液酸化至pH小于6时,可以得到一种带6个负电荷的七钼酸根阴离子。请写出该聚合平衡的离子反应方程式。_______
(4)当上述溶液进一步酸化到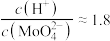 时,由电动势和超离心法研究结果推断,溶液中形成了非常大的聚阴离子X,已知X带有8个负电荷,只含两种配体,且其中一个配体为中性,
时,由电动势和超离心法研究结果推断,溶液中形成了非常大的聚阴离子X,已知X带有8个负电荷,只含两种配体,且其中一个配体为中性,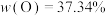 ,
,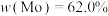 ,请写出X的化学式(书写时要表示出配体种类)和计算过程。
,请写出X的化学式(书写时要表示出配体种类)和计算过程。_______
(5)将正磷酸、钼酸铵、硝酸混合在一起,会生成一种黄色的十二钼磷酸铵,化学式为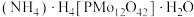 ,此反应在分析化学上被用来检验
,此反应在分析化学上被用来检验 及其盐。请写出该反应的化学方程式。
及其盐。请写出该反应的化学方程式。_______
(1)请写出Cr、Mo、W的价电子组态。(如Fe的为
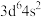 )
)(2)请写出铬酸根离子在酸性水溶液的条件下聚合成重铬酸根离子的可逆反应方程式。
(3)当钼酸盐水溶液酸化至pH小于6时,可以得到一种带6个负电荷的七钼酸根阴离子。请写出该聚合平衡的离子反应方程式。
(4)当上述溶液进一步酸化到
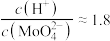 时,由电动势和超离心法研究结果推断,溶液中形成了非常大的聚阴离子X,已知X带有8个负电荷,只含两种配体,且其中一个配体为中性,
时,由电动势和超离心法研究结果推断,溶液中形成了非常大的聚阴离子X,已知X带有8个负电荷,只含两种配体,且其中一个配体为中性,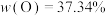 ,
,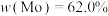 ,请写出X的化学式(书写时要表示出配体种类)和计算过程。
,请写出X的化学式(书写时要表示出配体种类)和计算过程。(5)将正磷酸、钼酸铵、硝酸混合在一起,会生成一种黄色的十二钼磷酸铵,化学式为
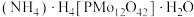 ,此反应在分析化学上被用来检验
,此反应在分析化学上被用来检验 及其盐。请写出该反应的化学方程式。
及其盐。请写出该反应的化学方程式。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】半导体芯片的发明是二十世纪的一项创举,奠定了信息时代的基础。单晶硅、氮化镓、碳化硅等是制作半导体芯片的关键材料,也是我国优先发展的新材料。请解答如下问题:
(1)硅的晶体结构是金刚石结构,如图所示。材料密度是制作芯片的重要参数之一,已知Si的共价半径是117pm,求每立方厘米体积的单晶硅中硅的原子数目_______

(2)芯片是在高纯单晶硅材料。上进行侵蚀、布线,集合多种.电子元器件实现某种特定功能的电路模块。晶体往往,呈现出各向异性,不同晶面结构不同,高品质芯片的制造与材料表面的结构密切相关。以晶胞定点为原点,边a、b、c为x、y、z建立坐标系,试画出单晶硅(100)、(110)、(111)晶面上硅原子的排布方式_______ (至少画出一个重复单元)
(3)经过半个多世纪的发展,硅基材料的半导体器件性能已经接近其物理极限,以碳化硅、氮化镓等为代表的第二代半导体材料或为当今热点。
①碳化硅常见的有α-SiC和β-SiC,它们分别具有六方和立方ZnS型结构,六方晶胞参数为a=308.0pm,c=505.0pm;立方晶胞参数为a=435.5pm,试通过计算比较两者硬度大小_______ 。
②作为半导体材料,β-SiC比α-SiC性能更加优良。β-SiC从立方晶胞对角线的视角观察,画出一维空间上C、Si原子的分布规律_______ (注意原子的符号和相对位置,至少画两个周期);给出β-SiC中临近的C-Si之间的距离_______
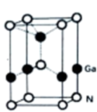
③GaN被誉为21世纪引领5G时代的基石材料,是目前全球半导体研究的前沿和热点。有一种氮化镓晶体为六方ZnS型结构,如图所示,请在图中构建一个以标有Ga的原子为中心的四面体结构_______ 。
(1)硅的晶体结构是金刚石结构,如图所示。材料密度是制作芯片的重要参数之一,已知Si的共价半径是117pm,求每立方厘米体积的单晶硅中硅的原子数目

(2)芯片是在高纯单晶硅材料。上进行侵蚀、布线,集合多种.电子元器件实现某种特定功能的电路模块。晶体往往,呈现出各向异性,不同晶面结构不同,高品质芯片的制造与材料表面的结构密切相关。以晶胞定点为原点,边a、b、c为x、y、z建立坐标系,试画出单晶硅(100)、(110)、(111)晶面上硅原子的排布方式
(3)经过半个多世纪的发展,硅基材料的半导体器件性能已经接近其物理极限,以碳化硅、氮化镓等为代表的第二代半导体材料或为当今热点。
①碳化硅常见的有α-SiC和β-SiC,它们分别具有六方和立方ZnS型结构,六方晶胞参数为a=308.0pm,c=505.0pm;立方晶胞参数为a=435.5pm,试通过计算比较两者硬度大小
②作为半导体材料,β-SiC比α-SiC性能更加优良。β-SiC从立方晶胞对角线的视角观察,画出一维空间上C、Si原子的分布规律
③GaN被誉为21世纪引领5G时代的基石材料,是目前全球半导体研究的前沿和热点。有一种氮化镓晶体为六方ZnS型结构,如图所示,请在图中构建一个以标有Ga的原子为中心的四面体结构

您最近一年使用:0次



