根据原子结构、元素周期律、电化学的知识,回答下列问题:
(1)现有 7种元素,它们在周期表中的位置如下:
7种元素,它们在周期表中的位置如下:
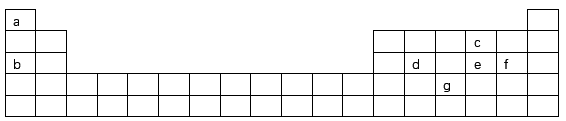
①以上7种元素中,原子半径最小的是___________ (填元素符号);d元素在周期表中的位置是___________ ;c元素的原子结构示意图为___________ 。
②a与f元素形成的化合物中的化学键属于___________ ,其电子式为___________ ;e元素最简单氢化物的化学式为___________ ;g元素最高价氧化物对应的水化物为___________ (填“强”或“弱”)酸。
③d元素最高价氧化物与b元素最高价氧化物对应水化物反应的离子方程式为___________ 。
(2)为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如下图所示:
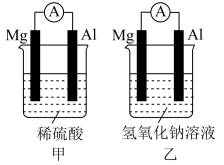
①装置甲的负极材料为___________ ,正极电极反应式为___________ 。
②装置乙中的阴离子向___________ (填“ ”或“
”或“ ”)电极移动,所发生的电池总反应为
”)电极移动,所发生的电池总反应为___________ 。
③甲装置在放电过程中,电解质溶液的酸性___________ (填“增强”“减弱”或“不变”)
(1)现有
 7种元素,它们在周期表中的位置如下:
7种元素,它们在周期表中的位置如下:
①以上7种元素中,原子半径最小的是
②a与f元素形成的化合物中的化学键属于
③d元素最高价氧化物与b元素最高价氧化物对应水化物反应的离子方程式为
(2)为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如下图所示:

①装置甲的负极材料为
②装置乙中的阴离子向
 ”或“
”或“ ”)电极移动,所发生的电池总反应为
”)电极移动,所发生的电池总反应为③甲装置在放电过程中,电解质溶液的酸性
更新时间:2021-07-20 15:30:09
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】一种利用废旧三元锂离子电池分步回收金属的实验流程如下:
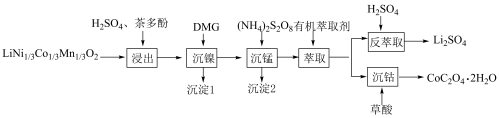
已知:
① 中元素
中元素 、
、 、
、 的价态分别为+1、+2、+3;
的价态分别为+1、+2、+3;
②室温下,几种金属离子形成氢氧化物沉淀的 如下表:
如下表:
③DMG的结构为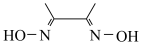 ;
;
④金属离子与有机萃取剂TBP结合能力为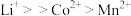 ,与P507的结合能力为
,与P507的结合能力为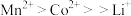 。
。
回答下列问题:
(1) 中锰元素的化合价是
中锰元素的化合价是___________ 。
(2) 可表示为LNCM,充放电时
可表示为LNCM,充放电时 分别脱出、嵌入。为提高锂的回收率,回收前应对电池进行放电处理。判断LNCM是电池的
分别脱出、嵌入。为提高锂的回收率,回收前应对电池进行放电处理。判断LNCM是电池的___________ (填“正极”或“负极”)材料。
(3)“浸出”后的溶液中过渡金属离子的化合价均为+2,茶多酚的作用是___________ 。
(4)沉淀1为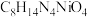 ,“沉镍”过程主要反应的离子方程式是
,“沉镍”过程主要反应的离子方程式是___________ (DMG用化学式表示),该过程中应控制溶液的 ,理论上最佳的
,理论上最佳的 不超过
不超过___________ (填序号),原因是___________ 。
A.7.2 B.8.1 C.8.7 D.10.1
(5)沉淀2为 ,“沉锰”过程主要反应的离子方程式是
,“沉锰”过程主要反应的离子方程式是___________ 。
(6)有机萃取剂应选择___________ (填“TBP”或“P507”),利用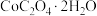 的热重图进行计算,可知400℃时的固体成分是
的热重图进行计算,可知400℃时的固体成分是___________ (填化学式)。
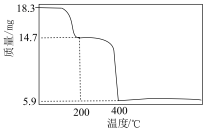

已知:
①
 中元素
中元素 、
、 、
、 的价态分别为+1、+2、+3;
的价态分别为+1、+2、+3;②室温下,几种金属离子形成氢氧化物沉淀的
 如下表:
如下表:| 金属离子 |  |  |  |
开始沉淀 | 8.1 | 7.2 | 7.2 |
完全沉淀 | 10.1 | 8.7 | 8.7 |
 ;
;④金属离子与有机萃取剂TBP结合能力为
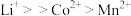 ,与P507的结合能力为
,与P507的结合能力为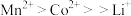 。
。回答下列问题:
(1)
 中锰元素的化合价是
中锰元素的化合价是(2)
 可表示为LNCM,充放电时
可表示为LNCM,充放电时 分别脱出、嵌入。为提高锂的回收率,回收前应对电池进行放电处理。判断LNCM是电池的
分别脱出、嵌入。为提高锂的回收率,回收前应对电池进行放电处理。判断LNCM是电池的(3)“浸出”后的溶液中过渡金属离子的化合价均为+2,茶多酚的作用是
(4)沉淀1为
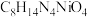 ,“沉镍”过程主要反应的离子方程式是
,“沉镍”过程主要反应的离子方程式是 ,理论上最佳的
,理论上最佳的 不超过
不超过A.7.2 B.8.1 C.8.7 D.10.1
(5)沉淀2为
 ,“沉锰”过程主要反应的离子方程式是
,“沉锰”过程主要反应的离子方程式是(6)有机萃取剂应选择
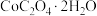 的热重图进行计算,可知400℃时的固体成分是
的热重图进行计算,可知400℃时的固体成分是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】把一块锌片和一块铜片平行地插入盛有稀硫酸的烧杯中,用导线把锌片和铜片连接起来,导线中间接入灵敏电流表,这个装置(见下图)就是简单的原电池。回答下列问题。
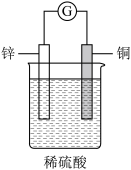
(1)电流表上出现的现象是___________ 。
(2)原电池工作时,能把氧化反应和还原反应分开在两个不同区域进行,实现电子的定向转移,电子流动的方向是___________ 。
(3)锌片为___________ 极,锌片上发生___________ 反应,溶液中的H+在铜片上___________ (选填:得到、失去)电子转化为H2。
(4)写出电池中总反应的化学方程式___________ 。
(5)如果装置中锌片、铜片没有用导线连接,化学能则转化为___________ 能。

(1)电流表上出现的现象是
(2)原电池工作时,能把氧化反应和还原反应分开在两个不同区域进行,实现电子的定向转移,电子流动的方向是
(3)锌片为
(4)写出电池中总反应的化学方程式
(5)如果装置中锌片、铜片没有用导线连接,化学能则转化为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。
I.
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是 (填字母)。
II.如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:
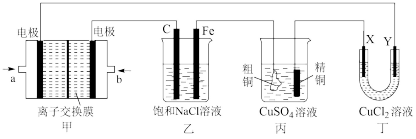
(2)甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是________________________ (填“CH4”或“O2”),负极的电极反应式是________
(3)在乙装置中,总反应的离子方程式是______ 。
(4)如果丙装置中精铜电极的质量增加了6.4 g,则甲装置中消耗的CH4的质量为_____ g。
I.
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是 (填字母)。
| A.C(s)+CO2(g)=2CO(g) ΔH>0 |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0 |
| C.2H2O(l)=2H2(g)+O2(g) ΔH>0 |
| D.C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH<0 |
II.如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:

(2)甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是
(3)在乙装置中,总反应的离子方程式是
(4)如果丙装置中精铜电极的质量增加了6.4 g,则甲装置中消耗的CH4的质量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)现有以下物质:a.NaOH溶液,b.液氨,c.Ba(OH)2固体,d.NaHSO4,e.Fe(OH)3胶体,f.铜,g.CO2,h.CH3COOH。
①以上物质中属于电解质的是___________ (填字母)。
②写出d在熔融时的电离方程式:___________ 。
③在d的水溶液中加入过量c的水溶液,发生反应的离子方程式为___________ 。
(2)高锰酸钾(硫酸酸化)溶液和草酸溶液的反应可用于测定血钙的含量。方法是取2mL血液用蒸馏水稀释后,向其中加入足量草酸铵晶体[化学式为(NH4)2C2O4],反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解后得到H2C2O4,再用KMnO4溶液滴定。
①高锰酸钾(硫酸酸化)溶液和草酸溶液的反应的化学方程式为:___________ ;
②用KMnO4溶液滴定H2C2O4时,判断滴定终点的方法是___________ 。
(3)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为___________ 。
(4)①钢铁在自然界中发生电化学腐蚀时的负极反应式为___________ ;
②碱性条件下,甲醇空气燃料电池的负极反应式为___________ 。
(1)现有以下物质:a.NaOH溶液,b.液氨,c.Ba(OH)2固体,d.NaHSO4,e.Fe(OH)3胶体,f.铜,g.CO2,h.CH3COOH。
①以上物质中属于电解质的是
②写出d在熔融时的电离方程式:
③在d的水溶液中加入过量c的水溶液,发生反应的离子方程式为
(2)高锰酸钾(硫酸酸化)溶液和草酸溶液的反应可用于测定血钙的含量。方法是取2mL血液用蒸馏水稀释后,向其中加入足量草酸铵晶体[化学式为(NH4)2C2O4],反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解后得到H2C2O4,再用KMnO4溶液滴定。
①高锰酸钾(硫酸酸化)溶液和草酸溶液的反应的化学方程式为:
②用KMnO4溶液滴定H2C2O4时,判断滴定终点的方法是
(3)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为
(4)①钢铁在自然界中发生电化学腐蚀时的负极反应式为
②碱性条件下,甲醇空气燃料电池的负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】某兴趣小组用如图所示装置研究电化学相关问题。电解质溶液都是足量的,当闭合该装置的电键时,观察到电流表的指针发生了偏转。
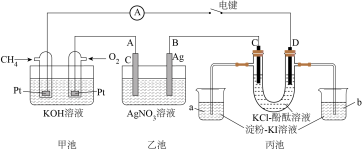
回答下面问题:
(1)甲池是_______ (填“原电池”或“电解池”),其中通入甲烷( )的Pt电极是
)的Pt电极是_______ (填“正极”“负极”“阳极”或“阴极”),通入氧气的Pt电极上发生的电极反应_______ 。
(2)乙池电极A石墨碳棒上发生的电极反应_______ ,电极B银棒上发生_______ (填“氧化”或“还原”)反应,开始时 溶液呈酸性,用离子方程式表示呈酸性的原因
溶液呈酸性,用离子方程式表示呈酸性的原因_______ 。电解一段时间后溶液的pH将_______ (填“增大”“减小”或“不变”)。
(3)丙池中C和D电极均为石墨电极,电极D上发生的电极反应_______ 。丙池两个烧杯中溶液变为蓝色的是_______ (填“a”或“b”),若U形管中盛有100mL溶液,电解一段时间断开电键K,两个电极上一共收集到224mL气体(标准状况下,忽略溶液体积的变化),此时U形管中溶液的
_______ 。
(4)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。
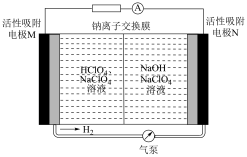
写出活性吸附电极N上的电极反应_______ , 在溶液中移动方向
在溶液中移动方向_______ (填序号)。
A.从左室穿过交换膜进入右室 B.从右室穿过交换膜进入左室

回答下面问题:
(1)甲池是
 )的Pt电极是
)的Pt电极是(2)乙池电极A石墨碳棒上发生的电极反应
 溶液呈酸性,用离子方程式表示呈酸性的原因
溶液呈酸性,用离子方程式表示呈酸性的原因(3)丙池中C和D电极均为石墨电极,电极D上发生的电极反应

(4)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

写出活性吸附电极N上的电极反应
 在溶液中移动方向
在溶液中移动方向A.从左室穿过交换膜进入右室 B.从右室穿过交换膜进入左室
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氮氧化物污染指数是衡量空气质量的重要标准,氮氧化物的治理刻不容缓。回答下列问题:
(1)已知:①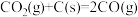 ΔH1
ΔH1
②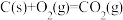 ΔH2
ΔH2
③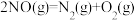 ΔH3
ΔH3
则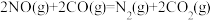 的ΔH=
的ΔH=___________ 。
(2)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为 ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
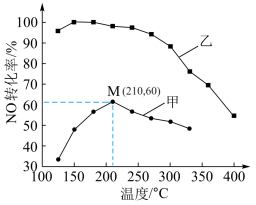
①工业上选择催化剂___________ (填“甲”或“乙”)。
②在催化剂甲作用下,图中M点NO的转化率___________ (填“是”或“不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是___________ 。
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的NO ,其工作原理如下图所示。
,其工作原理如下图所示。
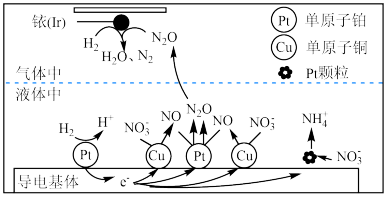
①导电基体Pt颗粒 上NO
上NO 发生的电极反应式为
发生的电极反应式为___________ 。
②在单原子铜、铂催化作用下,H2转化NO 为N2的过程可描述为
为N2的过程可描述为___________ 。
(1)已知:①
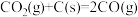 ΔH1
ΔH1②
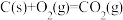 ΔH2
ΔH2③
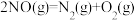 ΔH3
ΔH3则
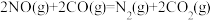 的ΔH=
的ΔH=(2)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为
 ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
①工业上选择催化剂
②在催化剂甲作用下,图中M点NO的转化率
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的NO
 ,其工作原理如下图所示。
,其工作原理如下图所示。
①导电基体Pt颗粒
 上NO
上NO 发生的电极反应式为
发生的电极反应式为②在单原子铜、铂催化作用下,H2转化NO
 为N2的过程可描述为
为N2的过程可描述为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E为原子序数依次增大的五种短周期元素,A与B形成的共价化合物M的水溶液呈碱性,C原子的最内层电子数是最外层电子数的2倍,D是同周期中单核离子半径最小的元素,E元素的最高正价与最低负价的代数和为6。请回答下列问题:
(1)元素E在周期表中的位置是_________ ;与元素C同族的下一周期元素的原子结构示意图为_________ 。
(2)M的沸点比PH3的沸点_____ (填“高”或“低”),原因是________ 。
(3)A、C形成的化合物CA与水反应生成无色气体,该反应的化学方程式______ ,每生成l mol气体,转移电子数为______ 。
(4)工业上,将CEO3与Na2SO3溶液混合后,再加入H2SO4制备水消毒剂EO2,该反应的离子方程式______ 。
(5)下列说法正确,且能够证明C的金属性比D强的是____ 。
A C离子的氧化性比D离子的氧化性弱
B C的最高价氧化物水化物的碱性比D的最高价氧化物的水化物碱性强
C C能从D的盐溶液中置换出D
D C在常温下能与水反应,而D不能
(1)元素E在周期表中的位置是
(2)M的沸点比PH3的沸点
(3)A、C形成的化合物CA与水反应生成无色气体,该反应的化学方程式
(4)工业上,将CEO3与Na2SO3溶液混合后,再加入H2SO4制备水消毒剂EO2,该反应的离子方程式
(5)下列说法正确,且能够证明C的金属性比D强的是
A C离子的氧化性比D离子的氧化性弱
B C的最高价氧化物水化物的碱性比D的最高价氧化物的水化物碱性强
C C能从D的盐溶液中置换出D
D C在常温下能与水反应,而D不能
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】I.有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)D﹣的结构示意图是___ 。
(2)C元素的气态氢化物的化学式为:___ ;其检验方法:___ 。
(3)B元素在周期表中的位置___ ;离子半径:B___ A(填“大于”或“小于”)。
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为___ ,与D的氢化物的水化物反应的离子方程式为___ 。
II.在2L密闭容器内,800℃时反应:2NO(g)+O2(g)⇌2NO2(g)体系中,n(NO)随时间的变化如下表:

(1)NO的平衡浓度c(NO)=___ 。
(2)图中表示NO2变化的曲线是___ ,用O2表示0~2s内该反应的平均速率υ=___ 。
(3)能说明该反应已达到平衡状态的是___ 。
a.υ(NO2)=2υ(O2) b.容器内气体压强保持不变
c.υ逆(NO)=2υ正(O2) d.容器内气体的密度保持不变
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)D﹣的结构示意图是
(2)C元素的气态氢化物的化学式为:
(3)B元素在周期表中的位置
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为
II.在2L密闭容器内,800℃时反应:2NO(g)+O2(g)⇌2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

(1)NO的平衡浓度c(NO)=
(2)图中表示NO2变化的曲线是
(3)能说明该反应已达到平衡状态的是
a.υ(NO2)=2υ(O2) b.容器内气体压强保持不变
c.υ逆(NO)=2υ正(O2) d.容器内气体的密度保持不变
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D、E五种短周期元素,其元素特征信息如下表,回答下列问题:
(1)写出下列元素的名称:C________ ;元素E在元素周期表中的位置是__________ 。
(2)写出A、B、C形成的化合物M的电子式________ ;五种原子中半径最大的是________ (填元素符号 )。五种元素最高价氧化物的水化物酸性最强的是(以上填化学式)___________ 。
(3)实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为________ 。
(4)D单质与M的水溶液反应的离子方程式:________ 。
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(2)写出A、B、C形成的化合物M的电子式
(3)实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为
(4)D单质与M的水溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】人体必需的一些元素在周期表中的分布情况如下:

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是_______ 。 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为_______ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将 通入NaOH溶液中,可以得到一种漂白液,上述反应的离子方程式为
通入NaOH溶液中,可以得到一种漂白液,上述反应的离子方程式为_______ 。
(3)钙元素和磷元素促进了我们骨骼发育与牙齿的正常生长。从物质分类的角度看,羟基磷灰石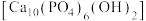 属于
属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。Ca与Mg在元素周期表同一族,化学性质相似同时也有递变性,试写出Ca与 反应的化学方程式:
反应的化学方程式:_______ 。
(4)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是_______ ,原子序数为_______ 。
(5)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______ 。
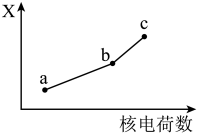
(6)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是
 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将
 通入NaOH溶液中,可以得到一种漂白液,上述反应的离子方程式为
通入NaOH溶液中,可以得到一种漂白液,上述反应的离子方程式为(3)钙元素和磷元素促进了我们骨骼发育与牙齿的正常生长。从物质分类的角度看,羟基磷灰石
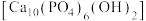 属于
属于 反应的化学方程式:
反应的化学方程式:(4)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(5)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性
 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(6)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
| C.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】如表列出8种元素在元素周期表(元素周期表只给出部分)中的位置。
请回答下列问题:
(1)考古工作者利用某元素的一种核素测定文物年代,这种核素的元素符号是_______ 。
(2)元素⑧的最高价氧化物对应的水化物的化学式是_______ ;元素②的简单气态氢化物的化学式是_______ 。
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(4)③、④、⑤三种元素的简单氢化物中稳定性最强的是_______ (填化学式);③、④、⑤中原子半径最小的是_______ (画原子结构示意图)。
(5)根据元素周期律,自然界中最强的碱是_______ (填化学式)。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ |
(1)考古工作者利用某元素的一种核素测定文物年代,这种核素的元素符号是
(2)元素⑧的最高价氧化物对应的水化物的化学式是
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物中稳定性最强的是
(5)根据元素周期律,自然界中最强的碱是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①—⑨在表中的位置,回答下列问题:
(1)第三周期中元素非金属性最强的元素的原子结构示意图为___________ 。
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)___________
(3)下列可以判断⑤和⑥金属性强弱的是___________ 。
a.⑤单质的熔点比⑥单质低 b.⑤的化合价比⑥低
c.⑤单质与水反应比单质⑥剧烈 d.⑤最高价氧化物的水化物的碱性比⑥强
(4)工业制备⑥单质的化学方程式___________ 。用⑥与赤铁矿冶炼金属铁的化学方程式___________ 。
(5)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:
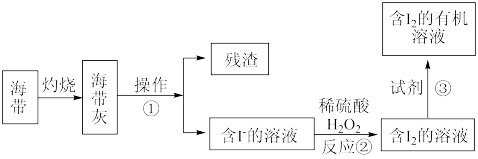
操作①的名称是___________ ;反应②的离子方程式是___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)
(3)下列可以判断⑤和⑥金属性强弱的是
a.⑤单质的熔点比⑥单质低 b.⑤的化合价比⑥低
c.⑤单质与水反应比单质⑥剧烈 d.⑤最高价氧化物的水化物的碱性比⑥强
(4)工业制备⑥单质的化学方程式
(5)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

操作①的名称是
您最近一年使用:0次



