根据各物质间的能量循环图(如图),下列说法正确的是


| A.ΔH4<0 | B.ΔH7>0 |
| C.K的第一电离能为ΔH6 | D.ΔH1= ΔH2+ΔH3+ΔH4+ΔH5+ΔH6+ΔH7 |
更新时间:2021-07-15 17:48:13
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】依据元素周期律,下列判断错误 的是
A.第一电离能: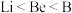 | B.原子半径: |
C.电负性: | D.酸性: |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列元素或化合物的性质变化顺序正确的是
| A.第一电离能:Cl>S>P>Si |
| B.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3 |
| C.晶格能:NaF>NaCl>NaBr>NaI |
| D.共价键的极性:HF>HCl>HBr>HI |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】如图所示是元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是


| A.W单质和氯气反应可生成两种空间结构相同的分子 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.最高价氧化物对应的水化物的酸性:W>X |
| D.第一电离能:R>W>Y |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度见下表:
下列说法中,正确的是
| 气体 | X | Y | Z |
| 初始浓度/(mol·L-1) | 0.10 | 0.20 | 0 |
| 平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.10 |
| A.X的平衡转化率为50% |
| B.与反应开始相比,反应达到平衡后容器内气体的总压强减小了50% |
| C.反应可表示为X(g)+3Y(g) ⇌2Z(g),该温度下其平衡常数为1.6 ×10 3(L·mol-1)2 |
| D.增大压强,平衡会向生成Z的方向移动,反应的平衡常数增大 |
您最近一年使用:0次
【推荐2】一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
①CH4(g) + 4NO2(g)= 4NO(g) + CO2(g) + 2H2O(g) △H1= - 574 kJ·mol-1
②CH4(g) + 4NO(g)=2N2(g) + CO2(g) + 2H2O(g) △H2= -1160 kJ·mol-1
下列选项中,正确的是
①CH4(g) + 4NO2(g)= 4NO(g) + CO2(g) + 2H2O(g) △H1= - 574 kJ·mol-1
②CH4(g) + 4NO(g)=2N2(g) + CO2(g) + 2H2O(g) △H2= -1160 kJ·mol-1
下列选项中,正确的是
| A.CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)的反应热为△H=-867kJ·mol-1 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)的反应热为△H3,则△H3<△H1 |
| C.若用0.2molCH4还原NO2至N2,则反应中放出的热量一定为173.4kJ |
| D.若用2.24LCH4(标况)全部还原NO2至N2,整个过程中转移的电子为1.6mol |
您最近一年使用:0次



