下表是元素周期表的一部分。请按要求回答下列有关问题:
(1)元素⑨单质形成的晶体的晶体类型是___________ 。
(2)在这些主族元素中,原子半径最大的是___________ 。(填元素符号)
(3)最高价氧化物对应水化物酸性最强物质的化学式是___________ 。
(4)最高价氧化物对应的水化物中,碱性最强的物质与呈两性的氢氧化物反应的离子反应方程式为___________ 。
(5)证明⑧与⑫的单质活泼性强弱的离子方程式为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)在这些主族元素中,原子半径最大的是
(3)最高价氧化物对应水化物酸性最强物质的化学式是
(4)最高价氧化物对应的水化物中,碱性最强的物质与呈两性的氢氧化物反应的离子反应方程式为
(5)证明⑧与⑫的单质活泼性强弱的离子方程式为
20-21高一下·江苏常州·期中 查看更多[3]
江苏省常州市武进区横山桥高级中学2020-2021学年高一下学期期中考试化学试题(已下线)第四章 物质结构 元素周期律(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)新疆克孜勒苏柯尔克孜自治州阿克陶县2022-2023学年高一上学期11月期中考试化学试题
更新时间:2021-07-17 21:58:07
|
相似题推荐
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】写出基态Ti原子的下列表示方法。
(1)电子排布式___________ 。
(2)简化电子排布式___________ 。
(3)价层电子排布式___________ 。
(4)价层电子轨道表示式___________ 。
(5)周期表中的位置(周期、族、区)___________ 。
(1)电子排布式
(2)简化电子排布式
(3)价层电子排布式
(4)价层电子轨道表示式
(5)周期表中的位置(周期、族、区)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】根据元素周期表中元素的性质和递变规律,填写下列空白。
(1)碱金属元素是_______ 族的金属元素,卤族元素是_______ 族元素。
(2)第三周期中,原子半径最大的元素是(稀有气体元素除外)_______ 。(填元素符号,下同)
(3)第三周期中金属性最强的元素与氧气反应,生成的化合物有_______ (写出两种化合物的化学式)。
(4)用电子式表示HCl、NaBr的形成过程。
①HCl:_______
②NaBr:_______
(1)碱金属元素是
(2)第三周期中,原子半径最大的元素是(稀有气体元素除外)
(3)第三周期中金属性最强的元素与氧气反应,生成的化合物有
(4)用电子式表示HCl、NaBr的形成过程。
①HCl:
②NaBr:
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】镁和铝在金属活动性顺序表中均排在氢之前,但是二者分别与盐酸反应的速率、现象不一样,①中反应剧烈,②中反应不剧烈。
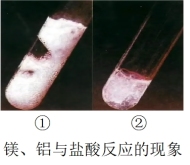
(1)根据图示以及镁、铝的电子层结构分析,哪个图表示的是镁与盐酸的反应?_______
(2)试利用原子结构的观点解释反应剧烈的一方剧烈的原因是什么?_______

(1)根据图示以及镁、铝的电子层结构分析,哪个图表示的是镁与盐酸的反应?
(2)试利用原子结构的观点解释反应剧烈的一方剧烈的原因是什么?
您最近一年使用:0次



