(1)30 g 12C18O 和 28 g 14N2 所含的分子数之比为_______ 。
(2)同温同压下,12C18O和14N2两种气体的密度之比为_______ 。
(3)同温同压同体积的12C18O和 14N2具有电子数之比为_______ 。
(4)28 g14N2所含的原子数为_______ NA.
(5)将乙烯、CO、N2三种气体分别盛放在三个相同容器中,若三个容器的温度和质量相等,则三个容器的气体压强之比为_______ 。
(2)同温同压下,12C18O和14N2两种气体的密度之比为
(3)同温同压同体积的12C18O和 14N2具有电子数之比为
(4)28 g14N2所含的原子数为
(5)将乙烯、CO、N2三种气体分别盛放在三个相同容器中,若三个容器的温度和质量相等,则三个容器的气体压强之比为
2021高三·全国·专题练习 查看更多[2]
更新时间:2021-07-26 11:17:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】根据所学知识,回答下列问题:
(1)等物质的量的SO2和H2S所含的原子总数之比为___________ ,电子数之比为___________ 。
(2)氢原子物质的量相等的NH3和H2的物质的量之比为___________ ,质量之比为___________ 。
(3)在标准状况下,等质量的CH4和H2S的体积之比为___________ ,氢原子的数目之比___________ 。
(4)相同条件下,NH3、CH4、H2S三种气体的密度之比为___________ 。
(1)等物质的量的SO2和H2S所含的原子总数之比为
(2)氢原子物质的量相等的NH3和H2的物质的量之比为
(3)在标准状况下,等质量的CH4和H2S的体积之比为
(4)相同条件下,NH3、CH4、H2S三种气体的密度之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为______ 。
(2)在25℃、101kPa的条件下,相同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______ 。
(3)两个相同容积的密闭容器X、Y,在25℃下,X中充入agA气体,Y中充入agCH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为______ 。
(1)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为
(2)在25℃、101kPa的条件下,相同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为
(3)两个相同容积的密闭容器X、Y,在25℃下,X中充入agA气体,Y中充入agCH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】同温同压下,同体积的氨气( )和硫化氢气体(
)和硫化氢气体( )的质量比为
)的质量比为_________ ;同质量的氨和硫化氢气体的体积比为___________ ;若二者氢原子数相等,则它们的体积比为___________ 。(均为前者比后者)
 )和硫化氢气体(
)和硫化氢气体( )的质量比为
)的质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答问题:
(1)在标准状况下①
 ②
②
 ③
③ 个
个 分子 ④
分子 ④
 ,所占的体积由大到小的顺序是(填序号,下同)
,所占的体积由大到小的顺序是(填序号,下同)___________ ;所含氢原子数由多到少的顺序是___________ ;密度由大到小的顺序是___________ ;质量由大到小的顺序是___________ 。
(2)某气态氧化物化学式为 ,在标准状况下,
,在标准状况下,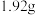 该氧化物的体积为
该氧化物的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为___________ , 的相对原子质量为
的相对原子质量为___________ 。
(3)相同物质的量的铁、镁、铝分别跟足量稀硫酸反应,在同温同压下产生气体的体积之比为___________ ;体积相同,物质的量浓度相同的稀硫酸分别跟足量的铁、镁、铝反应,在同温同压下产生气体的体积之比为___________ 。
(4)标准状况下,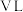 的某气体(摩尔质量为
的某气体(摩尔质量为
 )溶解在
)溶解在 水(水的密度近似为
水(水的密度近似为 )中,假设气体完全溶解且不与水发生反应,溶液的密度为
)中,假设气体完全溶解且不与水发生反应,溶液的密度为 ,则所得溶液的物质的量浓度
,则所得溶液的物质的量浓度
___________ ;质量分数
___________ 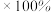 。(选择以上字母表达计算式,要求化简)。
。(选择以上字母表达计算式,要求化简)。
(1)在标准状况下①

 ②
②
 ③
③ 个
个 分子 ④
分子 ④
 ,所占的体积由大到小的顺序是(填序号,下同)
,所占的体积由大到小的顺序是(填序号,下同)(2)某气态氧化物化学式为
 ,在标准状况下,
,在标准状况下,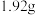 该氧化物的体积为
该氧化物的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为 的相对原子质量为
的相对原子质量为(3)相同物质的量的铁、镁、铝分别跟足量稀硫酸反应,在同温同压下产生气体的体积之比为
(4)标准状况下,
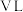 的某气体(摩尔质量为
的某气体(摩尔质量为
 )溶解在
)溶解在 水(水的密度近似为
水(水的密度近似为 )中,假设气体完全溶解且不与水发生反应,溶液的密度为
)中,假设气体完全溶解且不与水发生反应,溶液的密度为 ,则所得溶液的物质的量浓度
,则所得溶液的物质的量浓度

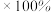 。(选择以上字母表达计算式,要求化简)。
。(选择以上字母表达计算式,要求化简)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碱式氯化铜是重要的无机杀菌剂。
(1)碱式氯化铜有多种制备方法
①方法1:45 ~ 50℃时,向CuCl悬浊液中持续通入空气得到Cu2 (OH)2 Cl2·3H2O,该反应的化学方程式为_____________ 。
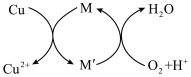
②方法2:先制得CuCl2,再与石灰乳反应生成碱式氯化铜。Cu与稀盐酸在持续通入空气的条件下反应生成CuCl2,Fe3+对该反应有催化作用,其催化原理如图所示。M'的化学式为______ 。
(2)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O。为测定某碱式氯化铜的组成,进行下列实验:
①称取样品2.2320g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25. 00mL溶液A,加入足量AgNO3溶液,得AgCl 0. 3444g;
③另取25. 00mL溶液A,调节pH 4 ~ 5,用浓度为0.08000mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++ H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液60.00mL。通过计算确定该样品的化学式(写出计算过程)。_____________
(1)碱式氯化铜有多种制备方法
①方法1:45 ~ 50℃时,向CuCl悬浊液中持续通入空气得到Cu2 (OH)2 Cl2·3H2O,该反应的化学方程式为
②方法2:先制得CuCl2,再与石灰乳反应生成碱式氯化铜。Cu与稀盐酸在持续通入空气的条件下反应生成CuCl2,Fe3+对该反应有催化作用,其催化原理如图所示。M'的化学式为

(2)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O。为测定某碱式氯化铜的组成,进行下列实验:
①称取样品2.2320g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25. 00mL溶液A,加入足量AgNO3溶液,得AgCl 0. 3444g;
③另取25. 00mL溶液A,调节pH 4 ~ 5,用浓度为0.08000mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++ H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液60.00mL。通过计算确定该样品的化学式(写出计算过程)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据计算结果填空。
(1)1.8g水与_______ mol硫酸所含的分子数相等,它们所含氧原子数之比是_______ 。
(2)在标准状况下,448mL某气体的质量为0.64g,这种气体的摩尔质量为_______ 。
(3)含0.4mol Al2(SO4)3的溶液中,含_______ mol SO ,Al3+的物质的量
,Al3+的物质的量_______ (填“>”、“<”或“=”)0.8mol。
(1)1.8g水与
(2)在标准状况下,448mL某气体的质量为0.64g,这种气体的摩尔质量为
(3)含0.4mol Al2(SO4)3的溶液中,含
 ,Al3+的物质的量
,Al3+的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】同温同压下,质量相同的三种气体: ①H2 ② O2 ③ CH4
所占的体积由大到小的顺序是(填序号,下同)_________________ ;
所含原子数由多到少的顺序是__________________________ ;
密度由大到小的顺序是_________________________________ 。
所占的体积由大到小的顺序是(填序号,下同)
所含原子数由多到少的顺序是
密度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)等质量的O2和O3所含的原子个数之比是___________ 。
(2)含有相同碳原子数的CO和CO2,其质量比为___________ 。
(3)若1g CO2中含有x个原子,则阿伏加德罗常数可表示为__________ 。
(4)4.9g H2SO4能和________ mol NaOH完全反应。
(5)标准状况下,10 mL N2气体恰好与30 mL H2完全反应生成20 mL气体A,则A的分子式为_________ 。
(6)将34.2g Al2(SO4)3固体溶于水配成100mL溶液从该溶液中取出10mL,稀释到100mL,稀释后溶液中溶质Al2(SO4)3的物质的量浓度为___________ 。
(2)含有相同碳原子数的CO和CO2,其质量比为
(3)若1g CO2中含有x个原子,则阿伏加德罗常数可表示为
(4)4.9g H2SO4能和
(5)标准状况下,10 mL N2气体恰好与30 mL H2完全反应生成20 mL气体A,则A的分子式为
(6)将34.2g Al2(SO4)3固体溶于水配成100mL溶液从该溶液中取出10mL,稀释到100mL,稀释后溶液中溶质Al2(SO4)3的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁铝化合物在生活生产中有广泛应用。
(1)自然界中存在的54Fe和56Fe,它们互称为___ 。
(2)将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因___ 。
(3)已知明矾可以净水,明矾化学式__ ,试结合离子反应方程式与文字解释明矾净水的原因__
(4)以NaAlO2溶液、AlCl3溶液、氨水、CO2气体为原料,选择合适试剂,写出实验室制备Al(OH)3的离子方程式:(任意两条途径)____ 、____
(5)达喜是常用的中和胃酸的药物,其化学成分是铝和镁的碱式盐,化学式为Al2Mg6(OH)16CO3·4H2O【可看做2Al(OH)3·5Mg(OH)2·MgCO3·4H2O】。1mol达喜分别与足量的盐酸和NaOH溶液反应,消耗盐酸和NaOH的物质的量之比为___ 。
(1)自然界中存在的54Fe和56Fe,它们互称为
(2)将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因
(3)已知明矾可以净水,明矾化学式
(4)以NaAlO2溶液、AlCl3溶液、氨水、CO2气体为原料,选择合适试剂,写出实验室制备Al(OH)3的离子方程式:(任意两条途径)
(5)达喜是常用的中和胃酸的药物,其化学成分是铝和镁的碱式盐,化学式为Al2Mg6(OH)16CO3·4H2O【可看做2Al(OH)3·5Mg(OH)2·MgCO3·4H2O】。1mol达喜分别与足量的盐酸和NaOH溶液反应,消耗盐酸和NaOH的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】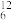 C、
C、 N、
N、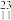 Na、
Na、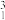 H、
H、 U、
U、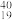 K、
K、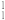 H、
H、 U中共有
U中共有______ 种元素,____ 种核素,____ 和___ 互为同位素。
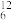 C、
C、 N、
N、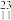 Na、
Na、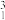 H、
H、 U、
U、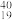 K、
K、 H、
H、 U中共有
U中共有
您最近一年使用:0次

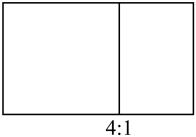
 H、
H、 H、
H、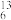 C、
C、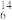 C、
C、 N、
N、 Fe2+、
Fe2+、 O2、
O2、

