某无色溶液中含有K+、Cl-、OH-、SO 、SO
、SO ,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
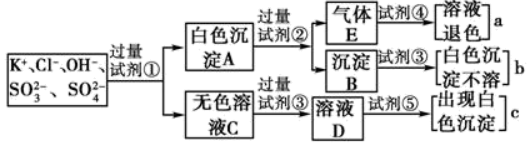
(1)图中试剂①~⑤溶质的化学式分别是:①___________ ,②___________ ,③___________ ,④___________ ,⑤___________ 。
(2)图中现象a、b、c表明检验出的离子分别是:a___________ ,b___________ ,c___________ 。
(3)白色沉淀A加试剂②反应的离子方程式是___________ 。
(4)白色沉淀A若加试剂③而不加试剂②,对实验的影响是___________ 。
(5)气体E通入试剂④发生反应的离子方程式是___________ 。
 、SO
、SO ,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
(1)图中试剂①~⑤溶质的化学式分别是:①
(2)图中现象a、b、c表明检验出的离子分别是:a
(3)白色沉淀A加试剂②反应的离子方程式是
(4)白色沉淀A若加试剂③而不加试剂②,对实验的影响是
(5)气体E通入试剂④发生反应的离子方程式是
更新时间:2021-07-27 15:34:25
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】为除去粗盐中的CaCl2、MgCl2、硫酸盐以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:

(1)第①步中,操作A是__________ ,第⑤步中,操作B是__________ 。
(2)判断试剂X过量的方法是________________________ 。
(3)写出第④步中涉及反应的化学方程式____________________ 。
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、__________ (填化学式)。
(5)此实验方案尚需完善,具体步骤是__________________ 。

(1)第①步中,操作A是
(2)判断试剂X过量的方法是
(3)写出第④步中涉及反应的化学方程式
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、
(5)此实验方案尚需完善,具体步骤是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】氧化钪( )在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含
)在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含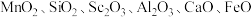 )为原料制备氧化钪的一种工艺流程如图所示。
)为原料制备氧化钪的一种工艺流程如图所示。 ;③草酸可与多种金属离子形成可溶性络合物。
;③草酸可与多种金属离子形成可溶性络合物。
回答下列问题:
(1)为了提高“浸取”效果,可采取的措施有___________ (写出一种)。
(2)“浸取”时铁屑被 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是___________ 。
(3)“萃取除铁”时铁和钪的萃取率与O/A(有机相与水相的体积比)的关系如图所示。该工艺中最佳O/A为___________ 。___________ 。
(5)常温下,“沉淀分离”时加入NaOH溶液调节pH至6,滤液中 的浓度为
的浓度为___________ 。
(6)已知 ,
,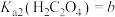 ,
,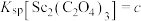 。“沉钪”时,发生反应
。“沉钪”时,发生反应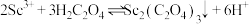 ,此反应的平衡常数
,此反应的平衡常数
___________ (用含a、b、c的代数式表示)。反应过程中,草酸用量过多时,航的沉淀率下降,原因可能是___________ 。
(7)草酸钪晶体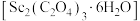 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为
随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为___________ 。
 )在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含
)在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含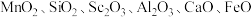 )为原料制备氧化钪的一种工艺流程如图所示。
)为原料制备氧化钪的一种工艺流程如图所示。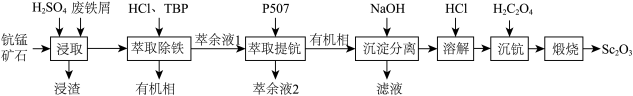
 ;③草酸可与多种金属离子形成可溶性络合物。
;③草酸可与多种金属离子形成可溶性络合物。回答下列问题:
(1)为了提高“浸取”效果,可采取的措施有
(2)“浸取”时铁屑被
 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是(3)“萃取除铁”时铁和钪的萃取率与O/A(有机相与水相的体积比)的关系如图所示。该工艺中最佳O/A为

(5)常温下,“沉淀分离”时加入NaOH溶液调节pH至6,滤液中
 的浓度为
的浓度为(6)已知
 ,
,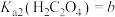 ,
,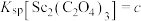 。“沉钪”时,发生反应
。“沉钪”时,发生反应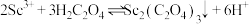 ,此反应的平衡常数
,此反应的平衡常数
(7)草酸钪晶体
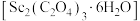 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为
随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为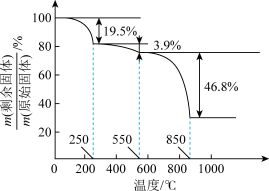
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:

(1)写出三种试剂的化学式:A________ ,B________ ,C________ 。
(2)加过量A的原因是:___________________________________ ,
有关反应的化学方程式为:_______________ ,_________________ 。
(3)加过量B的原因是:_________________________________

(1)写出三种试剂的化学式:A
(2)加过量A的原因是:
有关反应的化学方程式为:
(3)加过量B的原因是:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】定性分析溶液中的微粒组成是化学科学研究的前提和重要方面。请你根据所学知识对以下溶液做出定性的判断。
(1)某无色溶液含有下列离子中的若干种:H+、NH4+、Fe2+、Ba2+、Al3+、CO32–、Cl–、OH–、NO3–。若该溶液显酸性,则溶液中能大量共存的离子最多有_____ 种;若溶液显碱性,则溶液中能大量共存的离子最多有_____ 种。
(2)某溶液由Na+、Cu2+、Ba2+、Fe3+、CO32-、SO42-、Cl-中的若干种离子组成。取适量该溶液进行如下实验:①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②向①所得的溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
③向②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
则原溶液中可能存在的离子是_____ ;一定存在的离子是__________________________ 。
(1)某无色溶液含有下列离子中的若干种:H+、NH4+、Fe2+、Ba2+、Al3+、CO32–、Cl–、OH–、NO3–。若该溶液显酸性,则溶液中能大量共存的离子最多有
(2)某溶液由Na+、Cu2+、Ba2+、Fe3+、CO32-、SO42-、Cl-中的若干种离子组成。取适量该溶液进行如下实验:①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②向①所得的溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
③向②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
则原溶液中可能存在的离子是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】(1)请写出NaHCO3在水中的电离方程式:______________ ;NaOH溶液与NaHCO3溶液反应的离子方程式:________________ 。
(2)某无色透明溶液中可能大量存在NH4+、Na+、Ba2+、Fe3+、CO32-、SO42-、Cl-中的几种离子。从其中取两份各100mL溶液,进行如下实验:
①根据溶液颜色可以判断溶液中不存在的离子是_____________ ;
②取其中的一份溶液进行实验,加入过量氢氧化钠浓溶液并加热,共生成448mL气体(标准状况下),有关的离子方程式为______________ ;
③取另一份溶液加入过量Ba(NO3)2溶液,生成3.94g白色沉淀,过滤,向沉淀中再加入足量稀盐酸,沉淀全部溶解;根据以上实验结果确定:原溶液中肯定存在的离子有___________ ;请你设计实验方案证明该溶液中是否含有Cl-?_____________ 。
(3)某氮肥厂的氨氮废水中氮元素多以NH4+和NH3·H2O的形式存在。该厂的技术团队设计该废水处理方案流程如下:

①过程Ⅱ:在微生物的作用下实现NH4+→NO2-→NO3-转化,称为硝化过程。在碱性条件下,NH4+被氧气(O2)氧化成NO3-的总反应的离子方程式为________________ 。
②过程Ⅲ:在一定条件下向废水中加入甲醇(CH3OH),实现HNO3→NO2-→N2转化,称为反硝化过程。反硝化过程中甲醇(C元素为-2价)转化为CO2,若有6molHNO3完全转化成N2,消耗的甲醇的物质的量为_____________ 。
(2)某无色透明溶液中可能大量存在NH4+、Na+、Ba2+、Fe3+、CO32-、SO42-、Cl-中的几种离子。从其中取两份各100mL溶液,进行如下实验:
①根据溶液颜色可以判断溶液中不存在的离子是
②取其中的一份溶液进行实验,加入过量氢氧化钠浓溶液并加热,共生成448mL气体(标准状况下),有关的离子方程式为
③取另一份溶液加入过量Ba(NO3)2溶液,生成3.94g白色沉淀,过滤,向沉淀中再加入足量稀盐酸,沉淀全部溶解;根据以上实验结果确定:原溶液中肯定存在的离子有
(3)某氮肥厂的氨氮废水中氮元素多以NH4+和NH3·H2O的形式存在。该厂的技术团队设计该废水处理方案流程如下:

①过程Ⅱ:在微生物的作用下实现NH4+→NO2-→NO3-转化,称为硝化过程。在碱性条件下,NH4+被氧气(O2)氧化成NO3-的总反应的离子方程式为
②过程Ⅲ:在一定条件下向废水中加入甲醇(CH3OH),实现HNO3→NO2-→N2转化,称为反硝化过程。反硝化过程中甲醇(C元素为-2价)转化为CO2,若有6molHNO3完全转化成N2,消耗的甲醇的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】某无色稀溶液X中,可能含有下表所列离子中的某几种
现取适量该溶液,向其中加入某试剂Y,产生沉淀物质的量(n)与加入试剂的体积(V)关系如图所示:

(1)若Y是盐酸,所得到的关系图如甲图所示,则X中一定含有的阴离子是______ ,X中一定存在的几种阴离子物质的量之比为____ (按题干表格中阴离子出现的顺序写比例顺序);ab段发生反应的离子方程式为_________________ ;cd段发生的反应的离子方程式为______________ 。
(2)若Y是NaOH 溶液,所得到的关系图如乙用所示,X中一定含有的阳离子是_______ ;ab段发生反应的离子________________ ;bc段发生反应的离子为________________ ;cd段发生反应的离子方程式为______________ 。
| 阳离子 | H+、Na+、Al3+、Fe3+、NH4+、Mg2+ |
| 阴离子 | OH-、CO32-、SiO32-、AlO2-、Cl- |

(1)若Y是盐酸,所得到的关系图如甲图所示,则X中一定含有的阴离子是
(2)若Y是NaOH 溶液,所得到的关系图如乙用所示,X中一定含有的阳离子是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】某化学学习小组在帮助老师整理实验室的化学试剂时,发现一盛无色盐溶液的试剂瓶,标签破损如右图,该小组根据已掌握的知识,对药品作出猜想,并设计实验验证。

(1)该实验药品为中学化学常用试剂,推测它的阳离子化合价为______________________ 。
(2)同学们做出以下三种推测。
猜想1:Na2SO4
实验设计: 进行……,.证明是Na2SO4溶液;
猜想2: K2SO4
实验设计:____________________________ ,证明是K2SO4溶液;
猜想3; (NH4)2SO4
实验设计:____________________________ ,证明是(NH4)2SO4溶液。
(3)通过实验发现“猜想3”成立,已知(NH4)2SO4受热易分解,该小组拟用下图所示装置探究其分解产物。(夹持和加热装置略)
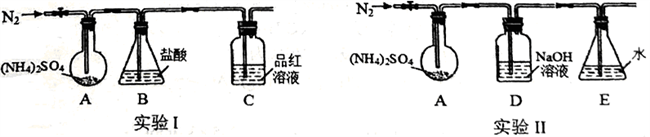
实验I:装置B 盛0.5000mol/L盐酸50.00mL,通入N2排尽空气后,将装置A 加热至260℃一段时间,停止加热,停止通入N2,品红溶液不褪色,取下装置B,用0.1000mol/LNaOH溶液滴定剩余盐酸,消耗NaOH 溶液50.00mL。经检验滴定后的溶液中无SO42-。
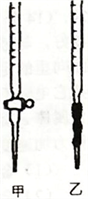
①请从右图选择盛放0.1000mol/LNaOH 溶液的滴定管____________ (填“甲”或“乙”)。
②装置B 内溶液吸收气体的物质的量是_____________________ mol。
实验Ⅱ:通入N2排尽空气后,将装置A 加热到400℃,至固体无残留,停止加热,停止通入N2,观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。
①装置E 的作用是____________________________ 。
②A、D之间的导气管内的少量白色固体是____________________________ 。
③有同学提出在AD之间需要增加一个防倒吸的安全瓶,老师说不需要,原因是____________________________ 。
④进一步研究发现,气体产物中无氮氧化物,则(NH4)2SO4在400℃分解的化学方程式是_______________________________ 。

(1)该实验药品为中学化学常用试剂,推测它的阳离子化合价为
(2)同学们做出以下三种推测。
猜想1:Na2SO4
实验设计: 进行……,.证明是Na2SO4溶液;
猜想2: K2SO4
实验设计:
猜想3; (NH4)2SO4
实验设计:
(3)通过实验发现“猜想3”成立,已知(NH4)2SO4受热易分解,该小组拟用下图所示装置探究其分解产物。(夹持和加热装置略)

实验I:装置B 盛0.5000mol/L盐酸50.00mL,通入N2排尽空气后,将装置A 加热至260℃一段时间,停止加热,停止通入N2,品红溶液不褪色,取下装置B,用0.1000mol/LNaOH溶液滴定剩余盐酸,消耗NaOH 溶液50.00mL。经检验滴定后的溶液中无SO42-。

①请从右图选择盛放0.1000mol/LNaOH 溶液的滴定管
②装置B 内溶液吸收气体的物质的量是
实验Ⅱ:通入N2排尽空气后,将装置A 加热到400℃,至固体无残留,停止加热,停止通入N2,观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。
①装置E 的作用是
②A、D之间的导气管内的少量白色固体是
③有同学提出在AD之间需要增加一个防倒吸的安全瓶,老师说不需要,原因是
④进一步研究发现,气体产物中无氮氧化物,则(NH4)2SO4在400℃分解的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】水合草酸亚铁(FeC2O4·xH2O)是生产锂电池的原料。难溶于水,受热易分解。某化学兴趣小组对草酸亚铁的一些性质进行探究。回答下列问题:
(1) 将水合草酸亚铁溶于适量盐酸。分别取2 mL此溶液于3支试管中,进行实验。能证明水合草酸亚铁中存在Fe2+的试剂有____ (填代号)。
A.KSCN溶液 B.K3[Fe(CN)6]溶液 C.酸性KMnO4溶液
(2) 为测定水合草酸亚铁中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为m2 g。按下图连接好装置进行实验。
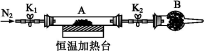
实验步骤如下:
a.打开K1和K2,缓缓通入N2; b.低温加热装置A一段时间;
c.停上加热,冷却到室温; d.关闭K1和K2,称量A;
e. ,记为m3 g。
①补充实验步骤e为__________ (填实验操作和要求)。
②步骤b至步骤e继续通入N2的目的是___________________ 。
(3)为探究草酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示部分的装置(可重复选用)进行实验。打开K1和K2,缓缓通入N2,充分加热。实验后石英玻璃管中固体仅残留一种有磁性的黑色化合物。

①实验装置中,依次连接的合理顺序为A→_______________ 。
②证明产物有CO生成的现象是________________ 。
③写出草酸亚铁受热分解的化学方程式________________ 。
(1) 将水合草酸亚铁溶于适量盐酸。分别取2 mL此溶液于3支试管中,进行实验。能证明水合草酸亚铁中存在Fe2+的试剂有
A.KSCN溶液 B.K3[Fe(CN)6]溶液 C.酸性KMnO4溶液
(2) 为测定水合草酸亚铁中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为m2 g。按下图连接好装置进行实验。

实验步骤如下:
a.打开K1和K2,缓缓通入N2; b.低温加热装置A一段时间;
c.停上加热,冷却到室温; d.关闭K1和K2,称量A;
e. ,记为m3 g。
①补充实验步骤e为
②步骤b至步骤e继续通入N2的目的是
(3)为探究草酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示部分的装置(可重复选用)进行实验。打开K1和K2,缓缓通入N2,充分加热。实验后石英玻璃管中固体仅残留一种有磁性的黑色化合物。

①实验装置中,依次连接的合理顺序为A→
②证明产物有CO生成的现象是
③写出草酸亚铁受热分解的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。

(1)写出装置A中发生反应的化学方程式:______ 。
(2)写出试剂Y的名称:______ 。
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物。充分反应后C中固体可能含有NaHCO3、NaCl、Na2CO3,为确定C中固体成分现设计如下实验:
步骤1:取C中少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中。
步骤2:向A试管中滴加过量的稀HNO3溶液,产生大量气泡,_____ (填能或不能)确定碳酸钠存在,再滴加AgNO3溶液,产生白色沉淀。
步骤3:向B试管中滴加BaCl2溶液,无明显现象。
则C中固体一定含_____ ,一定不含_____ 。
(4)已知C中有0.1molCl2参加反应,由(3)已知和结论,可推知C中反应的化学方程式为_____ 。

(1)写出装置A中发生反应的化学方程式:
(2)写出试剂Y的名称:
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物。充分反应后C中固体可能含有NaHCO3、NaCl、Na2CO3,为确定C中固体成分现设计如下实验:
步骤1:取C中少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中。
步骤2:向A试管中滴加过量的稀HNO3溶液,产生大量气泡,
步骤3:向B试管中滴加BaCl2溶液,无明显现象。
则C中固体一定含
(4)已知C中有0.1molCl2参加反应,由(3)已知和结论,可推知C中反应的化学方程式为
您最近一年使用:0次



