氧化钪( )在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含
)在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含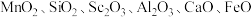 )为原料制备氧化钪的一种工艺流程如图所示。
)为原料制备氧化钪的一种工艺流程如图所示。 ;③草酸可与多种金属离子形成可溶性络合物。
;③草酸可与多种金属离子形成可溶性络合物。
回答下列问题:
(1)为了提高“浸取”效果,可采取的措施有___________ (写出一种)。
(2)“浸取”时铁屑被 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是___________ 。
(3)“萃取除铁”时铁和钪的萃取率与O/A(有机相与水相的体积比)的关系如图所示。该工艺中最佳O/A为___________ 。___________ 。
(5)常温下,“沉淀分离”时加入NaOH溶液调节pH至6,滤液中 的浓度为
的浓度为___________ 。
(6)已知 ,
,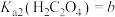 ,
,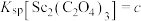 。“沉钪”时,发生反应
。“沉钪”时,发生反应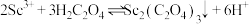 ,此反应的平衡常数
,此反应的平衡常数
___________ (用含a、b、c的代数式表示)。反应过程中,草酸用量过多时,航的沉淀率下降,原因可能是___________ 。
(7)草酸钪晶体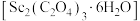 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为
随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为___________ 。
 )在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含
)在合金、电光源、催化剂和陶瓷等领域有广泛应用,以链锰矿石(含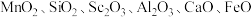 )为原料制备氧化钪的一种工艺流程如图所示。
)为原料制备氧化钪的一种工艺流程如图所示。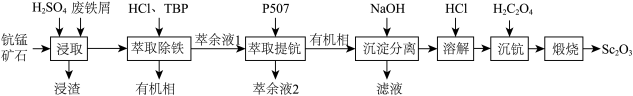
 ;③草酸可与多种金属离子形成可溶性络合物。
;③草酸可与多种金属离子形成可溶性络合物。回答下列问题:
(1)为了提高“浸取”效果,可采取的措施有
(2)“浸取”时铁屑被
 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是(3)“萃取除铁”时铁和钪的萃取率与O/A(有机相与水相的体积比)的关系如图所示。该工艺中最佳O/A为

(5)常温下,“沉淀分离”时加入NaOH溶液调节pH至6,滤液中
 的浓度为
的浓度为(6)已知
 ,
,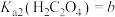 ,
,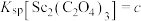 。“沉钪”时,发生反应
。“沉钪”时,发生反应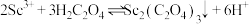 ,此反应的平衡常数
,此反应的平衡常数
(7)草酸钪晶体
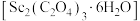 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为
随温度的变化情况如图所示。550-850 ℃发生反应的化学方程式为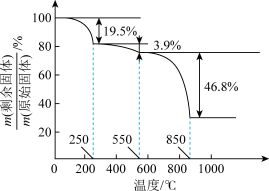
更新时间:2024-05-07 17:20:03
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
【推荐1】某无色溶液中含有K+、Cl-、OH-、SO 、SO
、SO ,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
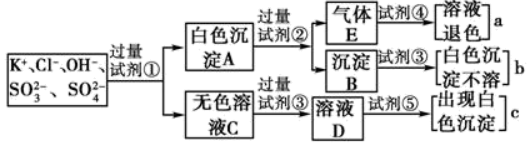
(1)图中试剂①~⑤溶质的化学式分别是:①___________ ,②___________ ,③___________ ,④___________ ,⑤___________ 。
(2)图中现象a、b、c表明检验出的离子分别是:a___________ ,b___________ ,c___________ 。
(3)白色沉淀A加试剂②反应的离子方程式是___________ 。
(4)白色沉淀A若加试剂③而不加试剂②,对实验的影响是___________ 。
(5)气体E通入试剂④发生反应的离子方程式是___________ 。
 、SO
、SO ,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
(1)图中试剂①~⑤溶质的化学式分别是:①
(2)图中现象a、b、c表明检验出的离子分别是:a
(3)白色沉淀A加试剂②反应的离子方程式是
(4)白色沉淀A若加试剂③而不加试剂②,对实验的影响是
(5)气体E通入试剂④发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】有A、B、C、D、E、F、G,7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl3、Ca(NO3)2和Ba (OH )2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。试回答下面问题。(已知AgOH微溶于水)
(1)A的化学式是____ ,G的化学式是_____ 。判断理由是_________________ 。
(2)写出其余几种物质的化学式。B:_____ ,C:_____ ,D:_____ ,E:_____ ,F:_____ 。
| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | ↓ | ↓ | ↓ |
| C | - | - | ― | ↓ | — | ↓ | ↓ |
| D | - | ↓ | - | ↓ | ↓ | ↓ | |
| E | - | ↓ | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
(1)A的化学式是
(2)写出其余几种物质的化学式。B:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:
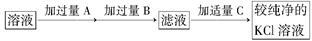
(1)写出三种试剂的化学式:A________ ,B________ ,C________ 。
(2)加过量A的原因是:__________________ ,
有关反应的化学方程式为:__________________ ,_________________ 。
(3)加过量B的原因是:__________________________ ,
有关反应的化学方程式为:_________________________ 。

(1)写出三种试剂的化学式:A
(2)加过量A的原因是:
有关反应的化学方程式为:
(3)加过量B的原因是:
有关反应的化学方程式为:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】氨基磺酸(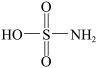 )是一种固体强酸,制备原理:CO(NH2)2+H2SO4+SO3
)是一种固体强酸,制备原理:CO(NH2)2+H2SO4+SO3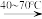 2HOSO2NH2+CO2,完成下列填空:
2HOSO2NH2+CO2,完成下列填空:
(1)O、S属同一主族,该族元素的最外层电子轨道表示式为___ ;CO2的电子式是___ 。
(2)反应原理中涉及的第二周期元素的非金属性由强到弱的顺序是_______ 。
(3)完成氨基磺酸受热分解的化学方程式_______ ,其中还原产物是_______ 。
____HOSO2NH2 SO2↑+____SO3↑+____N2↑+2H2↑+______H2O
SO2↑+____SO3↑+____N2↑+2H2↑+______H2O
(4)用过量的NaOH(aq)充分吸收氨基磺酸热解产生的混合气体,所得吸收液中含硫微粒浓度由大到小的顺序是_______ 。向吸收液中加入_______ 试剂,有_______ 现象,说明氨基磺酸热解产生SO3。
(5)氨基磺酸趋向于形成内盐:H2NSO3H→H3NSO3,可作氯水的稳定剂。H3NSO3与Cl2经取代反应生成的一氯代物缓慢水解成HClO,写出该一氯代物水解的化学方程式_______ 。
 )是一种固体强酸,制备原理:CO(NH2)2+H2SO4+SO3
)是一种固体强酸,制备原理:CO(NH2)2+H2SO4+SO3 2HOSO2NH2+CO2,完成下列填空:
2HOSO2NH2+CO2,完成下列填空:(1)O、S属同一主族,该族元素的最外层电子轨道表示式为
(2)反应原理中涉及的第二周期元素的非金属性由强到弱的顺序是
(3)完成氨基磺酸受热分解的化学方程式
____HOSO2NH2
 SO2↑+____SO3↑+____N2↑+2H2↑+______H2O
SO2↑+____SO3↑+____N2↑+2H2↑+______H2O(4)用过量的NaOH(aq)充分吸收氨基磺酸热解产生的混合气体,所得吸收液中含硫微粒浓度由大到小的顺序是
(5)氨基磺酸趋向于形成内盐:H2NSO3H→H3NSO3,可作氯水的稳定剂。H3NSO3与Cl2经取代反应生成的一氯代物缓慢水解成HClO,写出该一氯代物水解的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】废钼催化剂中钼、钴、镍等金属作为二次资源可加以回收利用,一种从废钼催化剂(主要成分为MoO3、MoS2,含少量CoO、CoS、NiO、Fe2O3等)中回收金属的一种工艺流程如图:
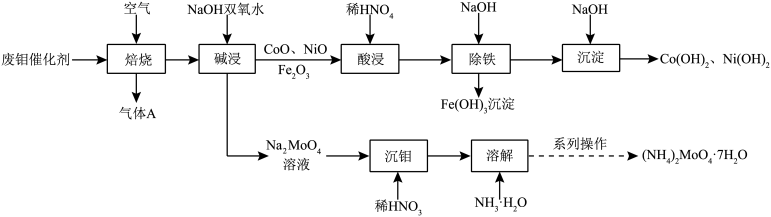
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)Ni2+价层电子轨道表示式为________ ,“焙烧”时产生的气体A的主要成分为________ 。
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式_________ 。
(3)“除铁”时应调节溶液pH的范围为___________ ,“沉淀”时调节溶液pH=9.0,则此时溶液中[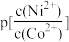 =
=___________ (pX=-lgX)。
(4)“系列操作”为________ 、________ 、过滤、洗涤、干燥得到(NH4)2MoO4·7H2O晶体。
(5)50.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为___________ %(保留小数点后一位数字,收率= )。
)。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Co2+ | Ni2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 2.2 3.2 | 6.4 9.0 | 7.2 8.7 |
(1)Ni2+价层电子轨道表示式为
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式
(3)“除铁”时应调节溶液pH的范围为
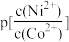 =
=(4)“系列操作”为
(5)50.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为
 )。
)。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠有少量泄漏,可通过喷洒硫代硫酸钠溶液来处理,以减轻污染。某化学兴趣小组在实验室制备硫代硫酸钠,并探究硫代硫酸钠的性质及氰化钠废水的处理。
【实验一】实验室通过如下图(a)所示装置制备Na2S2O3·5H2O
已知:Na2S2O3在酸性溶液中不能稳定存在,有关物质的溶解度曲线如图(b)所示,
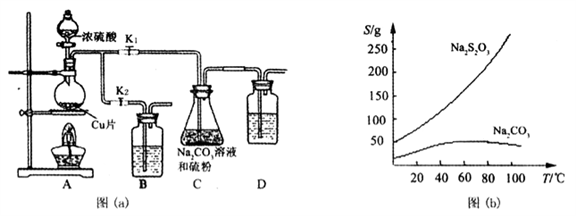
步骤1:如图连接好装置后,检查A、C装置气密性的操作是__________ 。
步骤2:加入药品,打开K1、关闭K2,加热。装置B、D中的药品可选用下列__________ (填编号)
A. NaOH溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.饱和NaHCO3溶液
步骤3:C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少。当C中溶液的pH在7至10时,打开K2、关闭K1并停止加热,C中溶液要控制pH的原因是__________ 。
步骤4:先将C中的混合液过滤,再将滤液经过加热浓缩,趁热过滤,最后将滤液__________ 得到产品。
【实验二】Na2 S2O3的性质及废水处理:
(1)向足量的新制氯水中滴加少量Na2 S2O3溶液,氯水颜色变浅,检查反应后溶液中含有硫酸根,写出该反应的离子方程式__________ 。
(2)氰化钠与硫代硫酸钠的反应为:NaCN + Na2S2O3=NaSCN + Na2SO3;已知:NaSCN中S为-2价,处理掉lmolNaCN,碳原子失去电子的物质的量为__________ 。
(3)废水中的CN-也可在催化剂作用下先用NaClO氧化成CNO-,再在酸性条件下继续用NaClO将CNO-氧化成两种对环境无污染的气体。则后一步反应的离子方程式为:
__________ 。
三、计算题
【实验一】实验室通过如下图(a)所示装置制备Na2S2O3·5H2O
已知:Na2S2O3在酸性溶液中不能稳定存在,有关物质的溶解度曲线如图(b)所示,

步骤1:如图连接好装置后,检查A、C装置气密性的操作是
步骤2:加入药品,打开K1、关闭K2,加热。装置B、D中的药品可选用下列
A. NaOH溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.饱和NaHCO3溶液
步骤3:C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少。当C中溶液的pH在7至10时,打开K2、关闭K1并停止加热,C中溶液要控制pH的原因是
步骤4:先将C中的混合液过滤,再将滤液经过加热浓缩,趁热过滤,最后将滤液
【实验二】Na2 S2O3的性质及废水处理:
(1)向足量的新制氯水中滴加少量Na2 S2O3溶液,氯水颜色变浅,检查反应后溶液中含有硫酸根,写出该反应的离子方程式
(2)氰化钠与硫代硫酸钠的反应为:NaCN + Na2S2O3=NaSCN + Na2SO3;已知:NaSCN中S为-2价,处理掉lmolNaCN,碳原子失去电子的物质的量为
(3)废水中的CN-也可在催化剂作用下先用NaClO氧化成CNO-,再在酸性条件下继续用NaClO将CNO-氧化成两种对环境无污染的气体。则后一步反应的离子方程式为:
三、计算题
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】碳、氮、硫的化合物在生产生活中广泛存在。请回答:
(1)下列有关碳及其化合物的说法正确的是_______
(2)T温度时在容积为2L的恒容密闭容器中只充入1.00molNO2气体发生反应:2NO(g)+O2(g) 2NO2(g) ∆H<0。不同时刻测得容器中n(NO2)如下表:
2NO2(g) ∆H<0。不同时刻测得容器中n(NO2)如下表:
①升高温度K值_______ (增大、减小),T温度时化学平衡常数K=_______ mol-1·L。
②从0~2s该反应的平均速率v(NO2)=_______ 。
③对可逆反应2NO(g)+O2(g) 2NO2(g) ∆H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是
2NO2(g) ∆H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是_______ 。
A.混 合气体的密度不再变化 B.混合气体的压强不再变化
C.氧气的转化率不再变化 D.NO2、O2、NO的物质的量之比为2:1:2
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是_______ (写出主要反应的离子方程式),该溶液中,c(Na+)_______ 2c(SO )+c(HSO
)+c(HSO )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
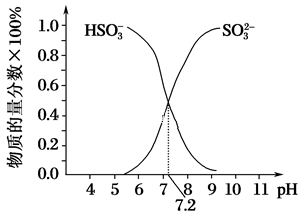
②在某NaHSO3、Na2SO3混合溶液中HSO 、SO
、SO 物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO
物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO 的第一步水解平衡常数=
的第一步水解平衡常数=_______ 。
(1)下列有关碳及其化合物的说法正确的是_______
| A.CO2是导致酸雨的主要气体 |
B.CO2的电子式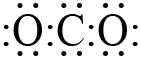 |
| C.金刚石、石墨与C60都是碳的同素异形体 |
| D.在高温条件下,碳能使CO2转变成CO |
 2NO2(g) ∆H<0。不同时刻测得容器中n(NO2)如下表:
2NO2(g) ∆H<0。不同时刻测得容器中n(NO2)如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO2)/mol | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
①升高温度K值
②从0~2s该反应的平均速率v(NO2)=
③对可逆反应2NO(g)+O2(g)
 2NO2(g) ∆H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是
2NO2(g) ∆H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是A.混 合气体的密度不再变化 B.混合气体的压强不再变化
C.氧气的转化率不再变化 D.NO2、O2、NO的物质的量之比为2:1:2
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是
 )+c(HSO
)+c(HSO )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。②在某NaHSO3、Na2SO3混合溶液中HSO
 、SO
、SO 物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO
物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO 的第一步水解平衡常数=
的第一步水解平衡常数=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】处理含硫烟气(主要成分为SO2)备受关注。回答下列问题:
Ⅰ.处理含硫烟气有以下两种方法
(1)水煤气还原法
已知:i.2CO(g)+SO2(g) S(l)+2CO2(g) △H1=—37.0kJ·mol-1
S(l)+2CO2(g) △H1=—37.0kJ·mol-1
ii.2H2(g)+SO2(g) S(l)+2H2O(g) △H2=+45.4kJ·mol-1
S(l)+2H2O(g) △H2=+45.4kJ·mol-1
写出CO(g)与H2O(g)反应生成CO2(g)、H2(g)的热化学方程式为___ 。
(2)碱液吸收法
①步骤1:用足量氨水吸收SO2,试写出该反应的化学方程式___ 。
②步骤2:再加入熟石灰的反应,试写出该反应离子方程式___ 。
③已知:25℃时,Kb(NH3·H2O)=a;Ksp(CaSO3)=b。该温度下,步骤2中反应的平衡常数K=__ (用含a、b的代数式表示)。
Ⅱ.常温下将NaOH溶液滴加到一定浓度的H2SO3溶液中,混合溶液的pH与离子浓度变化的关系如图所示。
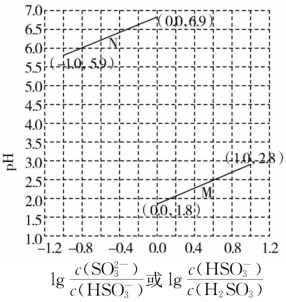
(1)Ka1(H2SO3)=___ 。
(2)当滴加NaOH溶液使混合溶液呈中性时,溶液中各离子浓度大小关系为___ 。
Ⅲ.将组成(物质的量分数)为m%SO2(g)、2m%H2(g)和q%He(g)的气体通入密闭反应器,使反应:H2(g)+ SO2(g)
SO2(g)
 S(l)+H2O(g),在温度t、压强P条件下进行反应,平衡时,若H2转化率为α,则平衡常数Kp=
S(l)+H2O(g),在温度t、压强P条件下进行反应,平衡时,若H2转化率为α,则平衡常数Kp=___ (以分压表示,分压=总压×物质的量分数)。
Ⅰ.处理含硫烟气有以下两种方法
(1)水煤气还原法
已知:i.2CO(g)+SO2(g)
 S(l)+2CO2(g) △H1=—37.0kJ·mol-1
S(l)+2CO2(g) △H1=—37.0kJ·mol-1ii.2H2(g)+SO2(g)
 S(l)+2H2O(g) △H2=+45.4kJ·mol-1
S(l)+2H2O(g) △H2=+45.4kJ·mol-1写出CO(g)与H2O(g)反应生成CO2(g)、H2(g)的热化学方程式为
(2)碱液吸收法
①步骤1:用足量氨水吸收SO2,试写出该反应的化学方程式
②步骤2:再加入熟石灰的反应,试写出该反应离子方程式
③已知:25℃时,Kb(NH3·H2O)=a;Ksp(CaSO3)=b。该温度下,步骤2中反应的平衡常数K=
Ⅱ.常温下将NaOH溶液滴加到一定浓度的H2SO3溶液中,混合溶液的pH与离子浓度变化的关系如图所示。

(1)Ka1(H2SO3)=
(2)当滴加NaOH溶液使混合溶液呈中性时,溶液中各离子浓度大小关系为
Ⅲ.将组成(物质的量分数)为m%SO2(g)、2m%H2(g)和q%He(g)的气体通入密闭反应器,使反应:H2(g)+
 SO2(g)
SO2(g)
 S(l)+H2O(g),在温度t、压强P条件下进行反应,平衡时,若H2转化率为α,则平衡常数Kp=
S(l)+H2O(g),在温度t、压强P条件下进行反应,平衡时,若H2转化率为α,则平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ. 25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,电离平衡常数Ka_______ (填“增大”、“减小”或“不变”),H2CO3的一级电离平衡常数表达式为Ka1 =_______ 。
(2)下列四种离子结合H+能力最强的是_______(填字母)。
(3)下列方法中,可以使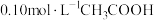 溶液中
溶液中 电离程度增大的是_______。
电离程度增大的是_______。
(4)HClO与Na2CO3溶液反应的离子方程式_______ 。
(5)25℃时,向①NaClO溶液中通入少量CO2,发生反应的离子方程式为_______ 。
II.某温度(t℃)时,测得0.01mol•L-1的NaOH溶液的pH=13,请回答下列问题:
(6)该温度下水的Kw=_______ 。
(7)此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va:Vb=_______ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数Ka | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)一般情况下,当温度升高时,电离平衡常数Ka
(2)下列四种离子结合H+能力最强的是_______(填字母)。
A. | B.ClO- | C.CH3COO- | D. |
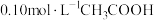 溶液中
溶液中 电离程度增大的是_______。
电离程度增大的是_______。| A.通入少量HCl气体 | B.加入少量冰醋酸 | C.加入少量醋酸钠固体 | D.加入少量水 |
(5)25℃时,向①NaClO溶液中通入少量CO2,发生反应的离子方程式为
II.某温度(t℃)时,测得0.01mol•L-1的NaOH溶液的pH=13,请回答下列问题:
(6)该温度下水的Kw=
(7)此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va:Vb=
您最近一年使用:0次
【推荐1】锰是生产各种合金的重要元素。工业上以含锰矿石(主要成分为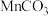 ,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
回答下列问题:
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有_______ (写两种)。
(2)“氧化”步骤发生反应的离子方程式为_______ 。
(3)滤渣1的主要成分是___ ,实验室中为了加快固液混合物的分离,常采用的操作是___ 。
(4)当溶液中可溶组分浓度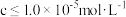 时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为
时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为____ (已知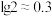 )。
)。
(5)“除杂3”步骤所得溶液中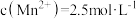 ,则其
,则其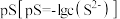 的范围是
的范围是____ 。
(6)电解废液中还含有少量 ,向其中加入饱和
,向其中加入饱和 溶液,有沉淀和气体生成,该反应的离子方程式为
溶液,有沉淀和气体生成,该反应的离子方程式为_______ 。
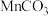 ,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下: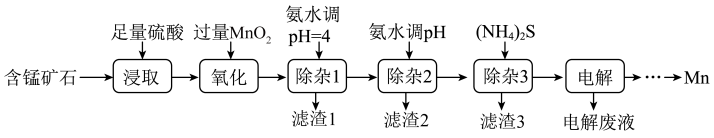
| 物质 |  |  |  | MnS | CoS |
 |  |  |  | 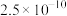 | 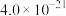 |
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有
(2)“氧化”步骤发生反应的离子方程式为
(3)滤渣1的主要成分是
(4)当溶液中可溶组分浓度
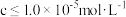 时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为
时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为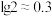 )。
)。(5)“除杂3”步骤所得溶液中
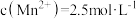 ,则其
,则其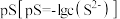 的范围是
的范围是(6)电解废液中还含有少量
 ,向其中加入饱和
,向其中加入饱和 溶液,有沉淀和气体生成,该反应的离子方程式为
溶液,有沉淀和气体生成,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】硫酸锰在农业上是重要的微量元素肥料,也是植物合成叶绿素的催化剂。一种以高硫锰矿(主要成分为含锰化合物及 ,还有含Mg化合物等杂质)与氧化锰矿(主要成分为
,还有含Mg化合物等杂质)与氧化锰矿(主要成分为 等锰的氧化物)为原料制备硫酸锰的工艺流程如图:
等锰的氧化物)为原料制备硫酸锰的工艺流程如图:
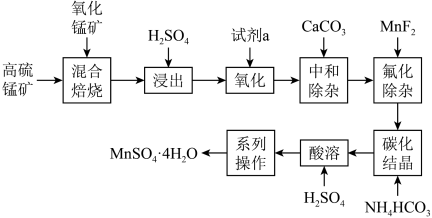
已知:①金属离子在水溶液中沉淀的 范围如下表所示(25℃):
范围如下表所示(25℃):
②离子浓度≤10-5mol/L时,离子沉淀完全。
(1)混合焙烧时一般需要将原料粉碎,这样做的主要目的是___________ 。
(2)混合焙烧过程会产生 气体,用
气体,用 溶液吸收
溶液吸收 可能生成
可能生成 或
或 ,请用离子方程式解释
,请用离子方程式解释 溶液显碱性的原因
溶液显碱性的原因___________ , 溶液显酸性,则在
溶液显酸性,则在 溶液中,下列两种微粒浓度大小关系是
溶液中,下列两种微粒浓度大小关系是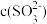
___________ 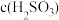 。(填“>”“=”或“<”)。
。(填“>”“=”或“<”)。
(3) 溶液和
溶液和 溶液中,各微柆浓度存在完全相同的等量关系式是
溶液中,各微柆浓度存在完全相同的等量关系式是___________ 。
(4)25℃时,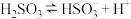 的电离常数
的电离常数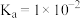 ,则该温度下
,则该温度下 水解反应的平衡常数
水解反应的平衡常数
___________ 。
(5)①若试剂a一般用 ,完成并配平氧化步骤发生反应的离子方程式:
,完成并配平氧化步骤发生反应的离子方程式:________
___________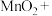 ___________
___________ ___________=___________
___________=___________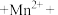 ___________
___________
②若没有“氧化”这一步,可能会造成的影响是___________ 。
(6)中和除杂时,加 调节
调节 在
在___________ 范围,请从平衡移动的角度解释调节溶液的 能达到去除
能达到去除 的目的
的目的___________ 。
(7)氟化除杂时,若使溶液中的 和
和 沉淀完全,需维持
沉淀完全,需维持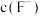 不低于
不低于___________ 。(已知: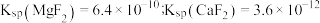 )
)
(8)“碳化结晶”时,加入碳酸氢铵,产生 沉淀。已知常温下部分弱电解质的电离平衡常数如下表,则碳酸氢铵的电离方程式为:
沉淀。已知常温下部分弱电解质的电离平衡常数如下表,则碳酸氢铵的电离方程式为:___________ ,根据下述表格,得出碳酸氢铵溶液呈___________ 性(填“酸”、“碱”或“中”)
(9)碳酸氢铵溶液中下列微粒浓度关系合理的是___________。
(10)流程中“系列操作”应该为___________ 、___________ 、过滤、洗涤、干燥。
 ,还有含Mg化合物等杂质)与氧化锰矿(主要成分为
,还有含Mg化合物等杂质)与氧化锰矿(主要成分为 等锰的氧化物)为原料制备硫酸锰的工艺流程如图:
等锰的氧化物)为原料制备硫酸锰的工艺流程如图:
已知:①金属离子在水溶液中沉淀的
 范围如下表所示(25℃):
范围如下表所示(25℃):| 物质 |  |  |  |  |
开始沉淀的 | 1.9 | 7.6 | 7.3 | 10.4 |
完全沉淀的 | 3.2 | 9.6 | 9.3 | 12.4 |
(1)混合焙烧时一般需要将原料粉碎,这样做的主要目的是
(2)混合焙烧过程会产生
 气体,用
气体,用 溶液吸收
溶液吸收 可能生成
可能生成 或
或 ,请用离子方程式解释
,请用离子方程式解释 溶液显碱性的原因
溶液显碱性的原因 溶液显酸性,则在
溶液显酸性,则在 溶液中,下列两种微粒浓度大小关系是
溶液中,下列两种微粒浓度大小关系是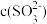
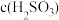 。(填“>”“=”或“<”)。
。(填“>”“=”或“<”)。(3)
 溶液和
溶液和 溶液中,各微柆浓度存在完全相同的等量关系式是
溶液中,各微柆浓度存在完全相同的等量关系式是(4)25℃时,
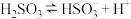 的电离常数
的电离常数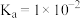 ,则该温度下
,则该温度下 水解反应的平衡常数
水解反应的平衡常数
(5)①若试剂a一般用
 ,完成并配平氧化步骤发生反应的离子方程式:
,完成并配平氧化步骤发生反应的离子方程式:___________
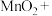 ___________
___________ ___________=___________
___________=___________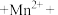 ___________
___________②若没有“氧化”这一步,可能会造成的影响是
(6)中和除杂时,加
 调节
调节 在
在 能达到去除
能达到去除 的目的
的目的(7)氟化除杂时,若使溶液中的
 和
和 沉淀完全,需维持
沉淀完全,需维持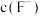 不低于
不低于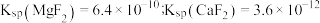 )
)(8)“碳化结晶”时,加入碳酸氢铵,产生
 沉淀。已知常温下部分弱电解质的电离平衡常数如下表,则碳酸氢铵的电离方程式为:
沉淀。已知常温下部分弱电解质的电离平衡常数如下表,则碳酸氢铵的电离方程式为:| 化学式 |  |  | |
| 电离常数 | 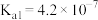 | 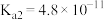 |  |
(9)碳酸氢铵溶液中下列微粒浓度关系合理的是___________。
A.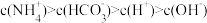 |
B.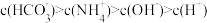 |
C.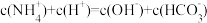 |
D. |
(10)流程中“系列操作”应该为
您最近一年使用:0次
【推荐3】以废旧玻璃粉末(主要含 )为原料可制备无水氯化铈(
)为原料可制备无水氯化铈( ),主要步骤如下:
),主要步骤如下:
(1)酸浸:用稀硫酸和双氧水的混合溶液浸取玻璃粉末,浸取液中含有 、
、 、
、 等金属阳离子。
等金属阳离子。
① 不溶于水,其发生反应的离子方程式:
不溶于水,其发生反应的离子方程式:_________ 。
②铈元素的浸出率与 、温度的关系如图所示。
、温度的关系如图所示。
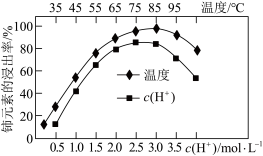
生产中 浓度最适宜控制在
浓度最适宜控制在_________ 。高于85℃时,铈元素浸出率下降的主要原因是:_________ 。
(2)除杂:向浸出液中加入NaOH调节pH除去 。已知:
。已知:
①当 时,
时, 沉淀开始溶解。
沉淀开始溶解。
② 、
、 溶度积常数分别为
溶度积常数分别为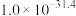 、
、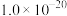 。
。
③“完全沉淀”时,金属离子浓度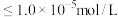
当浸出液中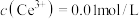 ,除杂时应控制溶液pH的范围是
,除杂时应控制溶液pH的范围是_________ (忽略体积变化)。
(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应: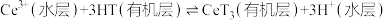 。分离后,再向所得有机层中加入
。分离后,再向所得有机层中加入_________ 能获得较纯的 溶液。
溶液。
结晶析出:将溶液蒸发浓缩、冷却结晶,过滤,得到晶体。
(4)加热脱水:将 固体和
固体和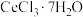 混合,存真空中加热可得无水
混合,存真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是_________ 。
 )为原料可制备无水氯化铈(
)为原料可制备无水氯化铈( ),主要步骤如下:
),主要步骤如下:(1)酸浸:用稀硫酸和双氧水的混合溶液浸取玻璃粉末,浸取液中含有
 、
、 、
、 等金属阳离子。
等金属阳离子。①
 不溶于水,其发生反应的离子方程式:
不溶于水,其发生反应的离子方程式:②铈元素的浸出率与
 、温度的关系如图所示。
、温度的关系如图所示。
生产中
 浓度最适宜控制在
浓度最适宜控制在(2)除杂:向浸出液中加入NaOH调节pH除去
 。已知:
。已知:①当
 时,
时, 沉淀开始溶解。
沉淀开始溶解。②
 、
、 溶度积常数分别为
溶度积常数分别为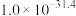 、
、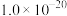 。
。③“完全沉淀”时,金属离子浓度
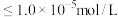
当浸出液中
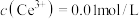 ,除杂时应控制溶液pH的范围是
,除杂时应控制溶液pH的范围是(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应:
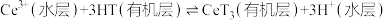 。分离后,再向所得有机层中加入
。分离后,再向所得有机层中加入 溶液。
溶液。结晶析出:将溶液蒸发浓缩、冷却结晶,过滤,得到晶体。
(4)加热脱水:将
 固体和
固体和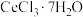 混合,存真空中加热可得无水
混合,存真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是
您最近一年使用:0次



