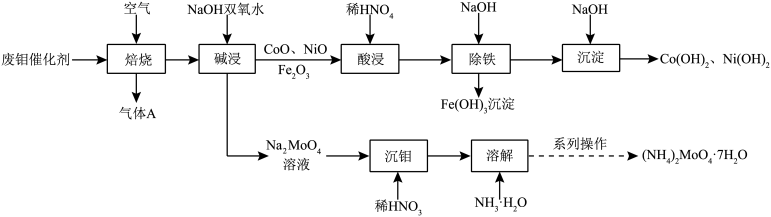
废钼催化剂中钼、钴、镍等金属作为二次资源可加以回收利用,一种从废钼催化剂(主要成分为MoO3、MoS2,含少量CoO、CoS、NiO、Fe2O3等)中回收金属的一种工艺流程如图:
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)Ni2+价层电子轨道表示式为________ ,“焙烧”时产生的气体A的主要成分为________ 。
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式_________ 。
(3)“除铁”时应调节溶液pH的范围为___________ ,“沉淀”时调节溶液pH=9.0,则此时溶液中[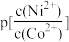 =
=___________ (pX=-lgX)。
(4)“系列操作”为________ 、________ 、过滤、洗涤、干燥得到(NH4)2MoO4·7H2O晶体。
(5)50.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为___________ %(保留小数点后一位数字,收率= )。
)。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Co2+ | Ni2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 2.2 3.2 | 6.4 9.0 | 7.2 8.7 |
(1)Ni2+价层电子轨道表示式为
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式
(3)“除铁”时应调节溶液pH的范围为
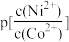 =
=(4)“系列操作”为
(5)50.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为
 )。
)。
更新时间:2023-05-22 14:39:07
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】锗及其化合物可应用于航空航天测控、光纤通信等领域。一种从硅—锗合金废料中制取高纯 的工艺流程如下:
的工艺流程如下:
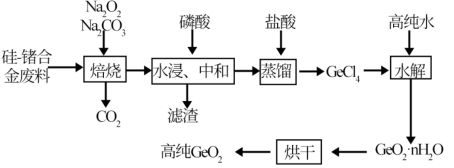
回答下列问题:
(1)为了加快“水浸”的速率可采取的措施有_______ (写两条)。
(2)“焙烧”时硅发生反应的化学方程式为_______ 。
(3)“滤渣”的主要成分为___ (填化学式),“中和”生成 的化学方程式为
的化学方程式为____ 。
(4)实验中磷酸的用量在90~140 时,随着磷酸的用量增加,锗的回收率逐渐提高,当磷酸用量为125
时,随着磷酸的用量增加,锗的回收率逐渐提高,当磷酸用量为125 时,排放液中含磷粒子总浓度为
时,排放液中含磷粒子总浓度为 ,请判断该排放液是否超标?
,请判断该排放液是否超标?_______ (填“超标”或“不超标”)。[《中华人民共和国国家标准一污水综合排放标准GB8978-1996》一级标准,排放液中磷酸盐(以P计)的含量不超过0.5 ]
]
(5)“水解”操作时保持较低温度有利于提高产率,其最可能的原因是____ 。
(6) 是锗酸(
是锗酸( )的酸酐,则25℃时,0.1
)的酸酐,则25℃时,0.1 的
的 溶液的
溶液的
__ (填“>”、“=”或“<”)7,通过计算说明理由:___ 。(已知25℃时, 的
的 ,
, )
)
 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)为了加快“水浸”的速率可采取的措施有
(2)“焙烧”时硅发生反应的化学方程式为
(3)“滤渣”的主要成分为
 的化学方程式为
的化学方程式为(4)实验中磷酸的用量在90~140
 时,随着磷酸的用量增加,锗的回收率逐渐提高,当磷酸用量为125
时,随着磷酸的用量增加,锗的回收率逐渐提高,当磷酸用量为125 时,排放液中含磷粒子总浓度为
时,排放液中含磷粒子总浓度为 ,请判断该排放液是否超标?
,请判断该排放液是否超标? ]
](5)“水解”操作时保持较低温度有利于提高产率,其最可能的原因是
(6)
 是锗酸(
是锗酸( )的酸酐,则25℃时,0.1
)的酸酐,则25℃时,0.1 的
的 溶液的
溶液的
 的
的 ,
, )
)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】Ⅰ.MgH2拥有很高的储氢密度,相对便宜的价格以及良好的可逆储氢性能,在储氢材料中具有重要作用和地位,一直都是广大研究者关注的焦点。回答下列问题:
(1)请写出MgH2的电子式:____ 。
(2)MgH2能与H2O反应生成白色沉淀Mg(OH)2和H2,NH3与H2O类似,MgH2与NH3反应也生成氢气,反应原理类似,请写出反应的化学方程式:____ 。
Ⅱ.(3)尿素(H2NCONH2)水解生成H2NCOONH4(氨基甲酸铵,简称甲铵),甲铵不稳定,迅速分解生成两种气态化合物,溶于水后,一个呈酸性,一个呈碱性,请写出甲铵受热分解的化学方程式:____ 。
(4)甲铵在不同条件下分解的能量变化如图所示,N过程与M过程相比,N过程活化能大大降低的原因可能是____ ;ΔH=___ kJ·mol−1。
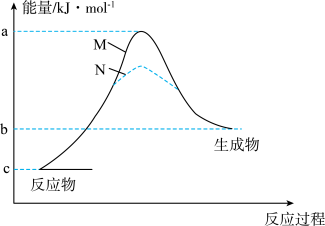
Ⅲ.氨呈弱碱性,氨燃料与碱性燃料电池是一对较好的组合。直接氨碱性(膜)燃料电池总的化学方程式为:4NH3+3O2=2N2+6H2O,工作原理如图:

(5)MnO2电极为__ 极(填“正”“负”“阴”或“阳”),写出Ni电极的电极反应式:____ 。
(1)请写出MgH2的电子式:
(2)MgH2能与H2O反应生成白色沉淀Mg(OH)2和H2,NH3与H2O类似,MgH2与NH3反应也生成氢气,反应原理类似,请写出反应的化学方程式:
Ⅱ.(3)尿素(H2NCONH2)水解生成H2NCOONH4(氨基甲酸铵,简称甲铵),甲铵不稳定,迅速分解生成两种气态化合物,溶于水后,一个呈酸性,一个呈碱性,请写出甲铵受热分解的化学方程式:
(4)甲铵在不同条件下分解的能量变化如图所示,N过程与M过程相比,N过程活化能大大降低的原因可能是

Ⅲ.氨呈弱碱性,氨燃料与碱性燃料电池是一对较好的组合。直接氨碱性(膜)燃料电池总的化学方程式为:4NH3+3O2=2N2+6H2O,工作原理如图:

(5)MnO2电极为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】铁及其化合物在生产、生活中有广泛应用。
(1)FeCl3是常用的净水剂和金属蚀刻剂。
①FeCl3净水的原理是_______ (用离子方程式表示)。
②FeCl3在溶液中分三步水解:






以上水解反应的平衡常数 、
、 、
、 由大到小的顺序是
由大到小的顺序是_______ 。
③电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,写出FeCl3溶液与铜箔发生反应的化学方程式_______ ,检验废腐蚀液中含有Fe3+的实验操作是_______ 。
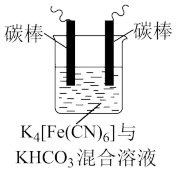
(2)用铁的化合物除硫化氢: ,可通过下图使
,可通过下图使 再生,电解时,阳极的电极反应式为
再生,电解时,阳极的电极反应式为_______ ;电解过程中阴极区溶液的pH_______ (填“变大”、“变小”或“不变”)。
(3)用高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有极强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式_______ 。
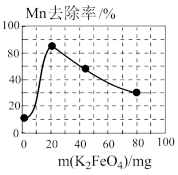
②用K2FeO4处理一定量的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图所示,当K2FeO4超过20mg时,Mn元素的去除率下降的原因可能是_______ 。
(1)FeCl3是常用的净水剂和金属蚀刻剂。
①FeCl3净水的原理是
②FeCl3在溶液中分三步水解:






以上水解反应的平衡常数
 、
、 、
、 由大到小的顺序是
由大到小的顺序是③电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,写出FeCl3溶液与铜箔发生反应的化学方程式
(2)用铁的化合物除硫化氢:
 ,可通过下图使
,可通过下图使 再生,电解时,阳极的电极反应式为
再生,电解时,阳极的电极反应式为
(3)用高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有极强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式
②用K2FeO4处理一定量的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图所示,当K2FeO4超过20mg时,Mn元素的去除率下降的原因可能是

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】金属镍及其化合物有极高的实用价值,可以制备储氢合金、新型镍氢电池及耐腐蚀的合金,还是一种很好的催化剂。某油脂厂废弃的镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其它不溶性物质。采用如下工艺流程制备草酸镍晶体( ):
):
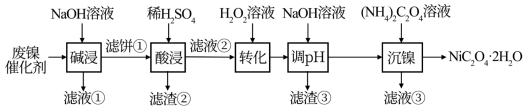
已知①当溶液中某离子浓度小于 mol/L时认为沉淀完全;
mol/L时认为沉淀完全;
② 的电离平衡常数
的电离平衡常数 ;
; 的电离平衡常数
的电离平衡常数 、
、 。
。
③溶液中金属离子浓度用 表示,
表示, 随溶液pH变化的图象如图所示:
随溶液pH变化的图象如图所示:
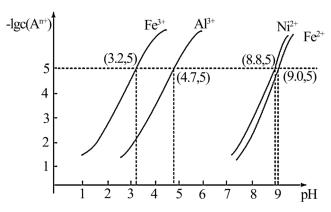
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是:溶解金属铝及其氧化物、_______ 。
(2)保持其它条件相同,在不同温度下进行酸浸时,镍浸出率随时间变化如图所示:
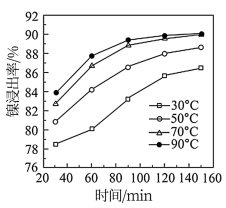
则“酸浸”的适宜温度和时间分别为_______ (填字母)。
a.30℃、30min b.90℃、150min c.70℃、120min
(3)滤渣③的主要成分是_______ (填化学式)。
(4) 溶液呈
溶液呈_______ 性(填“酸”“碱”或“中”),溶液中离子浓度由大到小的顺序是_______ 。
(5)根据题目中的数据计算 的Ksp=
的Ksp=_______ 。如果“转化”后的溶液中 浓度为
浓度为 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是_______ 。
 ):
):
已知①当溶液中某离子浓度小于
 mol/L时认为沉淀完全;
mol/L时认为沉淀完全;②
 的电离平衡常数
的电离平衡常数 ;
; 的电离平衡常数
的电离平衡常数 、
、 。
。③溶液中金属离子浓度用
 表示,
表示, 随溶液pH变化的图象如图所示:
随溶液pH变化的图象如图所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是:溶解金属铝及其氧化物、
(2)保持其它条件相同,在不同温度下进行酸浸时,镍浸出率随时间变化如图所示:

则“酸浸”的适宜温度和时间分别为
a.30℃、30min b.90℃、150min c.70℃、120min
(3)滤渣③的主要成分是
(4)
 溶液呈
溶液呈(5)根据题目中的数据计算
 的Ksp=
的Ksp= 浓度为
浓度为 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】利用氧化锌烟尘(主要成分为ZnO、PbS、As2O3、Fe2O3、SiO2等)制备饲料级碱式氯化锌[Zn5(OH)8Cl·H2O]。其工艺流程如下所示:

回答下列问题:
(1)“浸出”过程中的浸出液含有的阳离子是H+、Pb2+、As3+、Zn2+、Fe2+,则滤渣1主要成分为S和___________ (写出化学式);锌的浸出率和盐酸浓度关系如图;工业上,选择初始浓度为___________ 4mol/L的原因是___________ 。
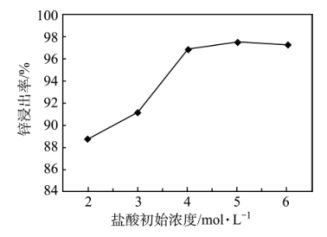
(2)氢氧化铁胶体可以特异性吸附As3+,在“调pH”的过程中,检验有胶体生成的物理方法是___________ 。
(3)写出“除铅”的离子反应方程式___________ ,若除铅后测得c(Zn2+)=0.36mol/L,则溶液中c(Pb2+)=___________ mol/L,已:Ksp(PbCO3)=7.20×10-14;Ksp(ZnCO3)=1.44×10-10.
(4)“合成”时,发生的总的化学反应方程式为___________ 。
(5)用Zn5(OH)8Cl·H2O制得纳米ZnO,其悬浊液可以用于吸收SO2尾气,已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、 、
、 的物质的量分数随pH的变化如图所示。
的物质的量分数随pH的变化如图所示。
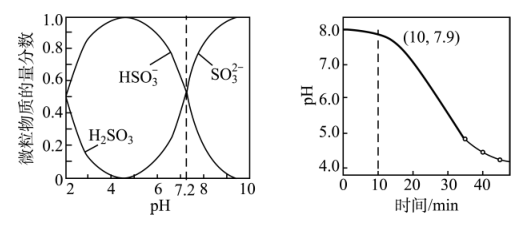
室温下,lgKa2(H2SO3)=___________ ;在开始吸收的40min内,溶液pH的变化如上图所示。0~10min,该反应主要产物是___________ (填化学式);30min以后阶段,主要的化学反应方程式为___________ 。

回答下列问题:
(1)“浸出”过程中的浸出液含有的阳离子是H+、Pb2+、As3+、Zn2+、Fe2+,则滤渣1主要成分为S和

(2)氢氧化铁胶体可以特异性吸附As3+,在“调pH”的过程中,检验有胶体生成的物理方法是
(3)写出“除铅”的离子反应方程式
(4)“合成”时,发生的总的化学反应方程式为
(5)用Zn5(OH)8Cl·H2O制得纳米ZnO,其悬浊液可以用于吸收SO2尾气,已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、
 、
、 的物质的量分数随pH的变化如图所示。
的物质的量分数随pH的变化如图所示。
室温下,lgKa2(H2SO3)=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】铵盐是比较重要的盐类物质,请回答下列问题。
(1)草酸是二元弱酸,能形成两种铵盐。
①(NH4)2C2O4溶液呈酸性,溶液中各离子浓度由大到小的顺序为_______ 。
②NH4HC2O4溶液中,c(H2C2O4)-c(C2O )=
)=_______ 。
(2)NH4SCN溶液与AgNO3溶液反应会生成AgSCN沉淀。已知:常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgSCN)=2.0×10-12,则AgCl转化为AgSCN的平衡常数K=_______ 。
(3)氯化铵是最常见的铵盐,在工业生产中用途广泛。
①热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:_______ 。
②常温下,向100 mL 0.2 mol·L-1的氨水中逐滴加入0.2 mol·L-1的盐酸,所得溶液的pH、溶液中NH 和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
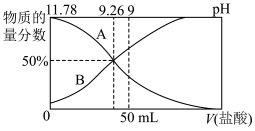
a.表示NH3·H2O物质的量分数变化的曲线是_______ (填“A”或“B”)。
b.NH3·H2O的电离常数为_______ 。
③常温下,在20 mL a mol·L-1氨水中滴加20 mL b mol·L-1盐酸恰好使溶液呈中性。常温下,NH 的水解常数Kh=
的水解常数Kh=_______ (用含a、b的代数式表示)。
(1)草酸是二元弱酸,能形成两种铵盐。
①(NH4)2C2O4溶液呈酸性,溶液中各离子浓度由大到小的顺序为
②NH4HC2O4溶液中,c(H2C2O4)-c(C2O
 )=
)=(2)NH4SCN溶液与AgNO3溶液反应会生成AgSCN沉淀。已知:常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgSCN)=2.0×10-12,则AgCl转化为AgSCN的平衡常数K=
(3)氯化铵是最常见的铵盐,在工业生产中用途广泛。
①热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:
②常温下,向100 mL 0.2 mol·L-1的氨水中逐滴加入0.2 mol·L-1的盐酸,所得溶液的pH、溶液中NH
 和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
a.表示NH3·H2O物质的量分数变化的曲线是
b.NH3·H2O的电离常数为
③常温下,在20 mL a mol·L-1氨水中滴加20 mL b mol·L-1盐酸恰好使溶液呈中性。常温下,NH
 的水解常数Kh=
的水解常数Kh=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】以黄铜矿(主要成分为铁、铜、硫三种元素组成的化合物)为基本原料,通过一系列的冶炼可得到铜、铁、SO2、SO3、H2SO4等物质,回答下列问题:
(1)基态铁原子的价层电子排布图为____________ 。
(2)SO2、SO3、H2SO4中,硫原子的杂化轨道类型为sp3的物质是________ ,SO2的分子构型是____________ ,属于非极性分子的氧化物是___________ 。
(3)氧化铜的熔点为1326℃、沸点为1800℃;氧化亚铜的熔点为1235℃、沸点为1100℃,导致这种差异的原因是___________ 。
(4)SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸 。
。
①与SCN-互为等电子体的微粒_________ (用化学式表示,写一种即可)。
②异硫氰酸的沸点比硫氰酸沸点高的原因是_______________ 。
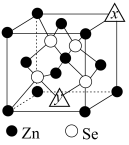
(5)硒化锌的晶胞结构如图所示,图中“△”处所堆积的原子均为________ (填元素符号);该晶胞中硒原子所处空隙类型为_________ (填“立方体”、“正四面体”或“正八面体”),该种空隙的填充率为__________ ;若该晶胞密度为 ,硒化锌的摩尔质量为M g/mol,用NA代表阿伏加德罗常数的数值,则晶胞参数a为
,硒化锌的摩尔质量为M g/mol,用NA代表阿伏加德罗常数的数值,则晶胞参数a为__________ nm。
(1)基态铁原子的价层电子排布图为
(2)SO2、SO3、H2SO4中,硫原子的杂化轨道类型为sp3的物质是
(3)氧化铜的熔点为1326℃、沸点为1800℃;氧化亚铜的熔点为1235℃、沸点为1100℃,导致这种差异的原因是
(4)SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸
 和异硫氰酸
和异硫氰酸 。
。①与SCN-互为等电子体的微粒
②异硫氰酸的沸点比硫氰酸沸点高的原因是
(5)硒化锌的晶胞结构如图所示,图中“△”处所堆积的原子均为
 ,硒化锌的摩尔质量为M g/mol,用NA代表阿伏加德罗常数的数值,则晶胞参数a为
,硒化锌的摩尔质量为M g/mol,用NA代表阿伏加德罗常数的数值,则晶胞参数a为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】高温超导材料广泛应用于超导输电、超导计算机、磁悬浮列车和热核聚变反应堆等。将 、
、 和
和 混合在高温下反应可制得新型节能高温超导体钇钡铜氧(其中Y显+3价,Cu显+2、+3价)。
混合在高温下反应可制得新型节能高温超导体钇钡铜氧(其中Y显+3价,Cu显+2、+3价)。
回答下列问题:
(1)Y(钇)是一种重要的稀土金属元素,与Sc(钪)同族相邻,则Y元索在元素同族相邻,则Y元素在元素周期表中的位置为___________ 。
(2)根据元素原子外围电子排布特征,可将周期表分成五个区域,其中O元素属于___________ 区,基态O原子电子占据最高能级的电子云轮廊图为___________ 形。
(3)基态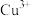 离子价层电子的电子排布图(轨道表示式)为
离子价层电子的电子排布图(轨道表示式)为___________ 。
(4)与 形成配合物的分子或离子应具备的结构特征是
形成配合物的分子或离子应具备的结构特征是___________ 。 中配位体的立体构型为
中配位体的立体构型为___________ 形,铜有两种氧化物 和
和 ,后者比前者的热稳定性强,原因是
,后者比前者的热稳定性强,原因是___________ 。
(5)在 中,C原子采用
中,C原子采用___________ 杂化,第一电离能:C___________ O(填“>”或“<”) 、
、 、
、 受热分解分别生成
受热分解分别生成 、
、 、
、 其中
其中 、
、 、
、 熔点较高的是
熔点较高的是___________ (填化学式)。
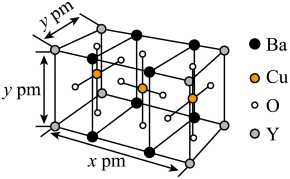
(6)钇钡铜氧的晶胞结构如图,根据晶胞结构确定其化学式为___________ ,若该晶体摩尔质量为 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则晶体密度为
,则晶体密度为___________  。
。
 、
、 和
和 混合在高温下反应可制得新型节能高温超导体钇钡铜氧(其中Y显+3价,Cu显+2、+3价)。
混合在高温下反应可制得新型节能高温超导体钇钡铜氧(其中Y显+3价,Cu显+2、+3价)。回答下列问题:
(1)Y(钇)是一种重要的稀土金属元素,与Sc(钪)同族相邻,则Y元索在元素同族相邻,则Y元素在元素周期表中的位置为
(2)根据元素原子外围电子排布特征,可将周期表分成五个区域,其中O元素属于
(3)基态
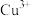 离子价层电子的电子排布图(轨道表示式)为
离子价层电子的电子排布图(轨道表示式)为(4)与
 形成配合物的分子或离子应具备的结构特征是
形成配合物的分子或离子应具备的结构特征是 中配位体的立体构型为
中配位体的立体构型为 和
和 ,后者比前者的热稳定性强,原因是
,后者比前者的热稳定性强,原因是(5)在
 中,C原子采用
中,C原子采用 、
、 、
、 受热分解分别生成
受热分解分别生成 、
、 、
、 其中
其中 、
、 、
、 熔点较高的是
熔点较高的是(6)钇钡铜氧的晶胞结构如图,根据晶胞结构确定其化学式为
 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则晶体密度为
,则晶体密度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】用软锰矿(主要成分MnO2,含有SiO2、Fe2O3、Al2O3、MgCO3等杂质)制备MnSO4·H2O的流程如下:
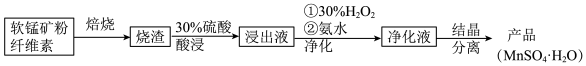
已知:MnO2不溶于酸
回答下列问题:
(1)Mn基态原子价态电子的电子排布图___________ ;周期表位置___________
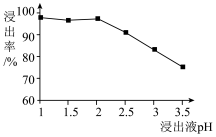
(2)焙烧时,MnO2和Fe2O3在纤维素作用下分别转化为MnO、Fe3O4,则纤维素的作用是___________ 。酸浸时,浸出液的pH与锰的浸出率关系如下图所示:实际生产中,酸浸时控制硫酸的量不宜过多,使pH在2左右。请结合图示和制备硫酸锰的流程,说明硫酸的量不宜过多的原因:___________ 。
(3)净化时,加入30%H2O2的目的是(用离子方程式表示)___________ ;加氨水,调pH范围为是___________ 。
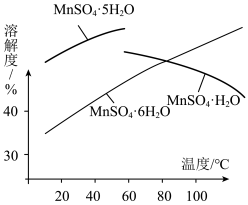
(4)结合MgSO4与MnSO4溶解度曲线,简述“结晶分离”的具体实验操作:___________ 。
(5)产品MnSO4·H2O(相对分子质量为169)纯度测定:称取a g产品,在适宜的条件下用适量NH4NO3将Mn2+氧化为Mn3+,再用0.1000 mol·L-1(NH4)2Fe(SO4)2溶液b mL刚好把Mn3+转化为Mn2+。通过计算可知产品纯度为___________ ,若滴定管洗涤时只用蒸馏水洗涤后直接使用,则所测产品纯度___________ 。(填偏大、偏小或无影响)

已知:MnO2不溶于酸
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.0 | 7.5 | 8.8 | 10.4 |
| 沉淀完全时的pH | 4.1 | 5.2 | 9.7 | 10.4 | 12.4 |
(1)Mn基态原子价态电子的电子排布图
(2)焙烧时,MnO2和Fe2O3在纤维素作用下分别转化为MnO、Fe3O4,则纤维素的作用是

(3)净化时,加入30%H2O2的目的是(用离子方程式表示)
(4)结合MgSO4与MnSO4溶解度曲线,简述“结晶分离”的具体实验操作:

(5)产品MnSO4·H2O(相对分子质量为169)纯度测定:称取a g产品,在适宜的条件下用适量NH4NO3将Mn2+氧化为Mn3+,再用0.1000 mol·L-1(NH4)2Fe(SO4)2溶液b mL刚好把Mn3+转化为Mn2+。通过计算可知产品纯度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】 是一种压电材料。以
是一种压电材料。以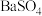 为原料制备粉状
为原料制备粉状 的流程如图。
的流程如图。 易溶于水,
易溶于水, 微溶于水。
微溶于水。
ⅱ.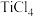 易水解生成
易水解生成 。
。
ⅲ某些温度时 的溶解度如下。
的溶解度如下。
(1)固体1的含硫物质主要是 ,得到固体1的化学方程式是
,得到固体1的化学方程式是___________ 。
(2)试剂 选用
选用___________ (填“水”或“盐酸”),理由是___________ 。
(3)向溶液1中加入盐酸的目的是___________ 。
(4)操作 的具体步骤是
的具体步骤是___________ 。
(5)固体3的主要成分是 。
。
①生成固体3的化学方程式是___________ 。
②得到固体3的过程,需要调控 ,否则
,否则 的产率较低。原因有:
的产率较低。原因有:
ⅰ. 较低时,c(
较低时,c( )较低;
)较低;
ⅱ. 较高时,
较高时,___________ 补充完整)。
(6)高温煅烧固体3,生成的 与
与 的物质的量之比
的物质的量之比 =
=___________ 。
 是一种压电材料。以
是一种压电材料。以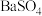 为原料制备粉状
为原料制备粉状 的流程如图。
的流程如图。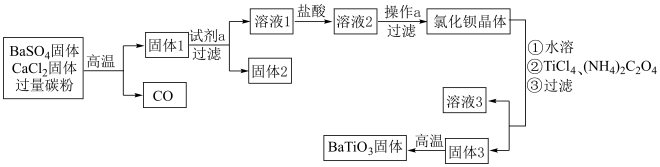
 易溶于水,
易溶于水, 微溶于水。
微溶于水。ⅱ.
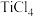 易水解生成
易水解生成 。
。ⅲ某些温度时
 的溶解度如下。
的溶解度如下。温度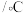 | 0 | 20 | 80 | 100 |
 溶解度 溶解度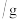 | 31.6 | 35.7 | 52.4 | 59.4 |
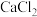 溶解度 溶解度 | 59.5 | 74.0 | 147.0 | 159.0 |
(1)固体1的含硫物质主要是
 ,得到固体1的化学方程式是
,得到固体1的化学方程式是(2)试剂
 选用
选用(3)向溶液1中加入盐酸的目的是
(4)操作
 的具体步骤是
的具体步骤是(5)固体3的主要成分是
 。
。①生成固体3的化学方程式是
②得到固体3的过程,需要调控
 ,否则
,否则 的产率较低。原因有:
的产率较低。原因有:ⅰ.
 较低时,c(
较低时,c( )较低;
)较低;ⅱ.
 较高时,
较高时,(6)高温煅烧固体3,生成的
 与
与 的物质的量之比
的物质的量之比 =
=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】铝热法冶炼金属铬的矿渣中含有Cr2O7、Al2O3及少量Fe2O3,从中提取铬与铝有酸法和碱法两种工艺。请回答:
I.酸法。矿渣经硫酸浸取后,浸取液通过电沉积得到单质Cr;向剩余溶液中加碱回收得到Al(OH)3。
(1)为提高矿渣的浸取率,可采取的措施有_____ (写出两点)。
(2)电沉积时,阴极的电极反应式为______________ 。
II. 碱法。工艺流程如下:
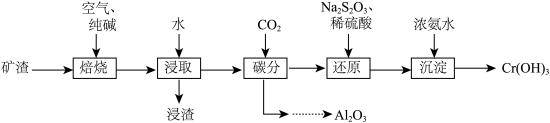
已知:①“焙烧”后固体成分为Na2CrO4、NaAlO2、NaFeO2。
② 、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
(3)浸渣的主要成分为Fe(OH)3。则“浸取”时发生反应的离子方程式为_________ 。
(4)“浸取”后所得溶液中Al的含量可用EDTA滴定法测定:
①取20.00mL浸取液于锥形瓶中,加入c1mol•L-1EDTA标准液V1mL(稍过量);
②依次用盐酸、醋酸钠—醋酸缓冲溶液调溶液至酸性,加热后滴入PAN指示剂;
③用c2mol•L-1ZnSO4标准液滴定至溶液恰好呈紫红色,消耗标准液V2mL。则“浸取”后所得溶液中Al的含量为_________ g•L-1(填计算式即可)。
(5)“碳分”时通入CO2后,通过_____ (填操作名称),即可得到纯净的Al2O3。
(6)“还原”时发生主要反应的离子方程式为__________ 。
(7)“沉淀”时,当c(Cr3+)≤10-5mol•L-1时,应调节溶液的pH至少为_________ 。(Ksp[Cr(OH)3]=1.0×10-32)
I.酸法。矿渣经硫酸浸取后,浸取液通过电沉积得到单质Cr;向剩余溶液中加碱回收得到Al(OH)3。
(1)为提高矿渣的浸取率,可采取的措施有
(2)电沉积时,阴极的电极反应式为
II. 碱法。工艺流程如下:

已知:①“焙烧”后固体成分为Na2CrO4、NaAlO2、NaFeO2。
②
 、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。(3)浸渣的主要成分为Fe(OH)3。则“浸取”时发生反应的离子方程式为
(4)“浸取”后所得溶液中Al的含量可用EDTA滴定法测定:
①取20.00mL浸取液于锥形瓶中,加入c1mol•L-1EDTA标准液V1mL(稍过量);
②依次用盐酸、醋酸钠—醋酸缓冲溶液调溶液至酸性,加热后滴入PAN指示剂;
③用c2mol•L-1ZnSO4标准液滴定至溶液恰好呈紫红色,消耗标准液V2mL。则“浸取”后所得溶液中Al的含量为
(5)“碳分”时通入CO2后,通过
(6)“还原”时发生主要反应的离子方程式为
(7)“沉淀”时,当c(Cr3+)≤10-5mol•L-1时,应调节溶液的pH至少为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】镍及其化合物用途广泛。某矿渣的主要成分是 (铁酸镍)、
(铁酸镍)、 、
、 、
、 、
、 ,下图是从该矿渣中回收
,下图是从该矿渣中回收 的工艺路线:
的工艺路线:

已知:① 在350℃以上会分解生成
在350℃以上会分解生成 和
和
② 在焙烧过程中生成
在焙烧过程中生成 、
、
(1)基态镍原子价电子排布图_______ 。
(2)焙烧前将矿渣与 混合研磨,混合研磨的目的是
混合研磨,混合研磨的目的是_______ 。
(3)“浸泡”过程中 生成
生成 的离子方程式为
的离子方程式为_______ ,“浸渣”的成分除 、
、 外还含有
外还含有_______ (填化学式)。
(4)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入 将
将 还原为
还原为 ,所需
,所需 的物质的量不少于
的物质的量不少于 物质的量的
物质的量的_______ 倍;除去过量的 后,再用酸性
后,再用酸性 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,还原产物为
,还原产物为 ,滴定时反应的离子方程式为
,滴定时反应的离子方程式为_______ 。
(5)“浸出液”中 ,当除钙率达到99%时,溶液中
,当除钙率达到99%时,溶液中
_______  。[已知
。[已知 ]
]
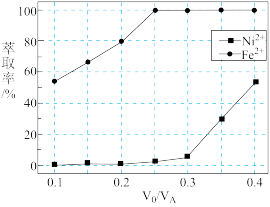
(6)本工艺中,萃取剂与溶液的体积比( )对溶液中
)对溶液中 、
、 的萃取率影响如图所示,
的萃取率影响如图所示, 的最佳取值是
的最佳取值是_______ 。
 (铁酸镍)、
(铁酸镍)、 、
、 、
、 、
、 ,下图是从该矿渣中回收
,下图是从该矿渣中回收 的工艺路线:
的工艺路线:
已知:①
 在350℃以上会分解生成
在350℃以上会分解生成 和
和
②
 在焙烧过程中生成
在焙烧过程中生成 、
、
(1)基态镍原子价电子排布图
(2)焙烧前将矿渣与
 混合研磨,混合研磨的目的是
混合研磨,混合研磨的目的是(3)“浸泡”过程中
 生成
生成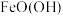 的离子方程式为
的离子方程式为 、
、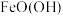 外还含有
外还含有(4)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入
 将
将 还原为
还原为 ,所需
,所需 的物质的量不少于
的物质的量不少于 物质的量的
物质的量的 后,再用酸性
后,再用酸性 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,还原产物为
,还原产物为 ,滴定时反应的离子方程式为
,滴定时反应的离子方程式为(5)“浸出液”中
 ,当除钙率达到99%时,溶液中
,当除钙率达到99%时,溶液中
 。[已知
。[已知 ]
](6)本工艺中,萃取剂与溶液的体积比(
 )对溶液中
)对溶液中 、
、 的萃取率影响如图所示,
的萃取率影响如图所示, 的最佳取值是
的最佳取值是
您最近一年使用:0次



