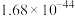氨基磺酸(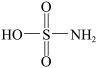 )是一种固体强酸,制备原理:CO(NH2)2+H2SO4+SO3
)是一种固体强酸,制备原理:CO(NH2)2+H2SO4+SO3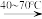 2HOSO2NH2+CO2,完成下列填空:
2HOSO2NH2+CO2,完成下列填空:
(1)O、S属同一主族,该族元素的最外层电子轨道表示式为___ ;CO2的电子式是___ 。
(2)反应原理中涉及的第二周期元素的非金属性由强到弱的顺序是_______ 。
(3)完成氨基磺酸受热分解的化学方程式_______ ,其中还原产物是_______ 。
____HOSO2NH2 SO2↑+____SO3↑+____N2↑+2H2↑+______H2O
SO2↑+____SO3↑+____N2↑+2H2↑+______H2O
(4)用过量的NaOH(aq)充分吸收氨基磺酸热解产生的混合气体,所得吸收液中含硫微粒浓度由大到小的顺序是_______ 。向吸收液中加入_______ 试剂,有_______ 现象,说明氨基磺酸热解产生SO3。
(5)氨基磺酸趋向于形成内盐:H2NSO3H→H3NSO3,可作氯水的稳定剂。H3NSO3与Cl2经取代反应生成的一氯代物缓慢水解成HClO,写出该一氯代物水解的化学方程式_______ 。
 )是一种固体强酸,制备原理:CO(NH2)2+H2SO4+SO3
)是一种固体强酸,制备原理:CO(NH2)2+H2SO4+SO3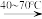 2HOSO2NH2+CO2,完成下列填空:
2HOSO2NH2+CO2,完成下列填空:(1)O、S属同一主族,该族元素的最外层电子轨道表示式为
(2)反应原理中涉及的第二周期元素的非金属性由强到弱的顺序是
(3)完成氨基磺酸受热分解的化学方程式
____HOSO2NH2
 SO2↑+____SO3↑+____N2↑+2H2↑+______H2O
SO2↑+____SO3↑+____N2↑+2H2↑+______H2O(4)用过量的NaOH(aq)充分吸收氨基磺酸热解产生的混合气体,所得吸收液中含硫微粒浓度由大到小的顺序是
(5)氨基磺酸趋向于形成内盐:H2NSO3H→H3NSO3,可作氯水的稳定剂。H3NSO3与Cl2经取代反应生成的一氯代物缓慢水解成HClO,写出该一氯代物水解的化学方程式
2022·上海普陀·二模 查看更多[2]
更新时间:2022-06-18 22:49:27
|
相似题推荐
【推荐1】我国规定生活用水中镉(Cd)排放的最大允许浓度为 ,铊(Tl)排放的最大允许浓度为
,铊(Tl)排放的最大允许浓度为 。处理含镉废水可采用化学沉淀法。已知一些化合物在常温时的
。处理含镉废水可采用化学沉淀法。已知一些化合物在常温时的 如表:
如表:
(1)磷酸镉沉淀溶解平衡常数的表达式
_________
(2)在某含镉废水中加入 ,当
,当 浓度达到
浓度达到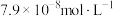 时,水体中
时,水体中 浓度为
浓度为_____ ;
(3)常温下,向含 和
和 的废水中,逐滴加入饱和NaOH溶液,首先产生沉淀的离子是
的废水中,逐滴加入饱和NaOH溶液,首先产生沉淀的离子是__________ 。
处理工业酸性含铬废水的过程是: 。
。
(4)利用硫酸工业废气中的 可以处理废水中的
可以处理废水中的 ,反应的离子方程式为
,反应的离子方程式为_____ 。
电解法也能将酸性废水中 转化为
转化为 ,装置局部如图所示。工作时,溶液中的
,装置局部如图所示。工作时,溶液中的 向着该Fe电极定向移动。
向着该Fe电极定向移动。
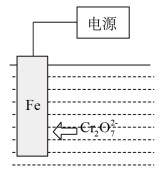
(5)该Fe电极是该装置的__________ 极。
(6)该电极表面发生的电极反应式为__________ 。
(7)该方法中, 被还原的离子方程式如下,配平下列离子方程式并表明电子转移方向及数目为
被还原的离子方程式如下,配平下列离子方程式并表明电子转移方向及数目为__________ 。
________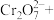 ________
________ ________ ________=________
________ ________=________ ________
________ _______
_______
 ,铊(Tl)排放的最大允许浓度为
,铊(Tl)排放的最大允许浓度为 。处理含镉废水可采用化学沉淀法。已知一些化合物在常温时的
。处理含镉废水可采用化学沉淀法。已知一些化合物在常温时的 如表:
如表:化合物 | CdS |
|
|
|
|
|
|
|
|

(2)在某含镉废水中加入
 ,当
,当 浓度达到
浓度达到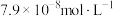 时,水体中
时,水体中 浓度为
浓度为(3)常温下,向含
 和
和 的废水中,逐滴加入饱和NaOH溶液,首先产生沉淀的离子是
的废水中,逐滴加入饱和NaOH溶液,首先产生沉淀的离子是处理工业酸性含铬废水的过程是:
 。
。(4)利用硫酸工业废气中的
 可以处理废水中的
可以处理废水中的 ,反应的离子方程式为
,反应的离子方程式为电解法也能将酸性废水中
 转化为
转化为 ,装置局部如图所示。工作时,溶液中的
,装置局部如图所示。工作时,溶液中的 向着该Fe电极定向移动。
向着该Fe电极定向移动。
(5)该Fe电极是该装置的
(6)该电极表面发生的电极反应式为
(7)该方法中,
 被还原的离子方程式如下,配平下列离子方程式并表明电子转移方向及数目为
被还原的离子方程式如下,配平下列离子方程式并表明电子转移方向及数目为________
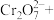 ________
________ ________ ________=________
________ ________=________ ________
________ _______
_______
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ.某化学兴趣小组利用某工业废铁屑制备食品添加剂FeSO4·7H2O,流程图如下___________ (填写化学式);
(2)“酸浸”时需加入试剂的化学式为___________ ,请写出该过程中属于非氧化还原反应的离子方程式___________ ;
(3)溶液C→Al(OH)3的离子方程式是___________ ;
(4)“灼烧”操作应选择下列哪一种仪器___________(填序号)
Ⅱ.高锰酸钾溶液常用于物质的定性检验与定量分析。
(5)现用其测定某补血剂片中亚铁的含量:称取含 (式量为278)的补血剂片a g,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与0.1mol/L的酸性高锰酸钾溶液反应,上述过程发生反应的离子反应式:
(式量为278)的补血剂片a g,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与0.1mol/L的酸性高锰酸钾溶液反应,上述过程发生反应的离子反应式: ___________ ;
(6)甲同学四次实验消耗的KMnO4溶液体积数据如下
根据甲同学的实验数据,该补血剂中 的质量分数为
的质量分数为___________ (用a表示)。
(7)补铁剂使用时建议与维生素C同服,乙同学猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将Fe3+转化为Fe2+”的结论?回答并说明理由:___________ 。
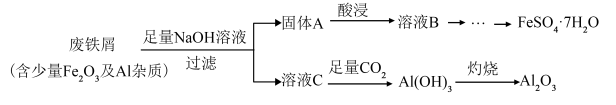
(2)“酸浸”时需加入试剂的化学式为
(3)溶液C→Al(OH)3的离子方程式是
(4)“灼烧”操作应选择下列哪一种仪器___________(填序号)
A. | B. | C.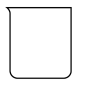 | D.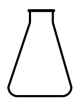 |
Ⅱ.高锰酸钾溶液常用于物质的定性检验与定量分析。
(5)现用其测定某补血剂片中亚铁的含量:称取含
 (式量为278)的补血剂片a g,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与0.1mol/L的酸性高锰酸钾溶液反应,上述过程发生反应的离子反应式:
(式量为278)的补血剂片a g,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与0.1mol/L的酸性高锰酸钾溶液反应,上述过程发生反应的离子反应式: (6)甲同学四次实验消耗的KMnO4溶液体积数据如下
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V(KMnO4液)/mL | 24.98 | 25.02 | 25.00 | 20.00 |
 的质量分数为
的质量分数为(7)补铁剂使用时建议与维生素C同服,乙同学猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
| 实验方案 | 实验现象 |
| 取适量Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 | 紫色褪去 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】 既是一种重要的能源,也是一种重要的化工原料。
既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0g 完全燃烧生成液体水放出444.8kJ热量。则
完全燃烧生成液体水放出444.8kJ热量。则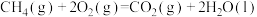 △H=
△H=___________  。若8.0g
。若8.0g 完全燃烧生成气态水,则放出的热量
完全燃烧生成气态水,则放出的热量___________ 444.8kJ。(填“>”、“<”或“=”)
(2)以 为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为
为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为___________ ,通入b气体的电极反应式为___________ 。(质子交换膜只允许 通过)
通过) 与
与 可直接转化成乙酸,这是实现“减排”的一种研究方向。
可直接转化成乙酸,这是实现“减排”的一种研究方向。
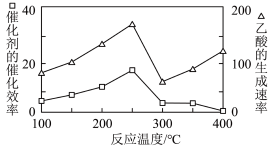
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在___________ 左右。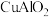 ,难溶物),其中铜元素化合价为
,难溶物),其中铜元素化合价为___________ 。将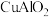 溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为
溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为___________ 。
(4) 还原法是处理
还原法是处理 气体的一种方法。已知一定条件下
气体的一种方法。已知一定条件下 与
与 反应转化为
反应转化为 和
和 ,若标准状况下8.96L
,若标准状况下8.96L 可处理22.4L
可处理22.4L ,则x值为
,则x值为___________ 。
 既是一种重要的能源,也是一种重要的化工原料。
既是一种重要的能源,也是一种重要的化工原料。(1)已知8.0g
 完全燃烧生成液体水放出444.8kJ热量。则
完全燃烧生成液体水放出444.8kJ热量。则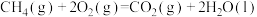 △H=
△H= 。若8.0g
。若8.0g 完全燃烧生成气态水,则放出的热量
完全燃烧生成气态水,则放出的热量(2)以
 为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为
为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为 通过)
通过)
 与
与 可直接转化成乙酸,这是实现“减排”的一种研究方向。
可直接转化成乙酸,这是实现“减排”的一种研究方向。①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在
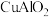 ,难溶物),其中铜元素化合价为
,难溶物),其中铜元素化合价为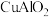 溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为
溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为(4)
 还原法是处理
还原法是处理 气体的一种方法。已知一定条件下
气体的一种方法。已知一定条件下 与
与 反应转化为
反应转化为 和
和 ,若标准状况下8.96L
,若标准状况下8.96L 可处理22.4L
可处理22.4L ,则x值为
,则x值为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】硫及其化合物对人类的生产生活有着重要的作用,回答下列问题:
(1)一定温度下,将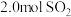 和
和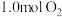 置于刚性容器中,发生反应
置于刚性容器中,发生反应

 。
。
①不能判断该反应达到平衡状态的标志是__________ (填标号)。
A.混合气体中 的浓度等于
的浓度等于 的浓度
的浓度
B.混合气体的平均相对分子质量保持不变
C. 的生成速率和
的生成速率和 的生成速率相等
的生成速率相等
D. 等于2:1:2
等于2:1:2
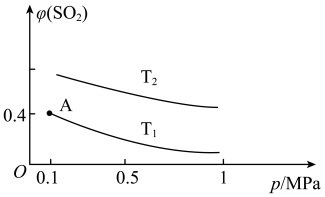
②平衡时 的体积分数随压强和温度变化的曲线如图所示。则温度关系:
的体积分数随压强和温度变化的曲线如图所示。则温度关系:
__________  (填“>”“<”或“=”),A点的化学平衡常数是
(填“>”“<”或“=”),A点的化学平衡常数是
__________  (
( 是以平衡分压代替平衡浓度的平衡常数,分压=总压
是以平衡分压代替平衡浓度的平衡常数,分压=总压 物质的量分数)。
物质的量分数)。
(2)一定温度下将 放入抽空的刚性容器中发生吸热反应:
放入抽空的刚性容器中发生吸热反应:
 。达到平衡后,压缩容器体积,一段时间后达到新平衡,与原平衡相对比,
。达到平衡后,压缩容器体积,一段时间后达到新平衡,与原平衡相对比,
__________ (填“增大”、“减小”或“不变”)。
若相同条件下,上述容器中发生副反应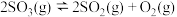 ,达到新平衡时,
,达到新平衡时, 的体积分数为
的体积分数为 ,则此时
,则此时 发生分解反应的平衡常数
发生分解反应的平衡常数
__________ (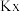 为以物质的量分数表示的平衡常数,计算结果保留两位有效数字,下同)。
为以物质的量分数表示的平衡常数,计算结果保留两位有效数字,下同)。
(3)亚硫酸 在水溶液中存在多种微粒形态。
在水溶液中存在多种微粒形态。 时,向
时,向 亚硫酸溶液中加入
亚硫酸溶液中加入 固体,含硫微粒(
固体,含硫微粒( 、
、 、
、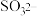 )的lgc和
)的lgc和 的关系如图所示。则曲线①代表的微粒是
的关系如图所示。则曲线①代表的微粒是__________ (填化学式),当 时,溶液中三种含硫微粒浓度大小顺序为
时,溶液中三种含硫微粒浓度大小顺序为__________ ,溶液中c点溶液的 值为
值为__________ 。

(1)一定温度下,将
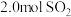 和
和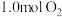 置于刚性容器中,发生反应
置于刚性容器中,发生反应

 。
。①不能判断该反应达到平衡状态的标志是
A.混合气体中
 的浓度等于
的浓度等于 的浓度
的浓度B.混合气体的平均相对分子质量保持不变
C.
 的生成速率和
的生成速率和 的生成速率相等
的生成速率相等D.
 等于2:1:2
等于2:1:2②平衡时
 的体积分数随压强和温度变化的曲线如图所示。则温度关系:
的体积分数随压强和温度变化的曲线如图所示。则温度关系:
 (填“>”“<”或“=”),A点的化学平衡常数是
(填“>”“<”或“=”),A点的化学平衡常数是
 (
( 是以平衡分压代替平衡浓度的平衡常数,分压=总压
是以平衡分压代替平衡浓度的平衡常数,分压=总压 物质的量分数)。
物质的量分数)。
(2)一定温度下将
 放入抽空的刚性容器中发生吸热反应:
放入抽空的刚性容器中发生吸热反应:
 。达到平衡后,压缩容器体积,一段时间后达到新平衡,与原平衡相对比,
。达到平衡后,压缩容器体积,一段时间后达到新平衡,与原平衡相对比,
若相同条件下,上述容器中发生副反应
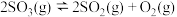 ,达到新平衡时,
,达到新平衡时, 的体积分数为
的体积分数为 ,则此时
,则此时 发生分解反应的平衡常数
发生分解反应的平衡常数
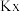 为以物质的量分数表示的平衡常数,计算结果保留两位有效数字,下同)。
为以物质的量分数表示的平衡常数,计算结果保留两位有效数字,下同)。(3)亚硫酸
 在水溶液中存在多种微粒形态。
在水溶液中存在多种微粒形态。 时,向
时,向 亚硫酸溶液中加入
亚硫酸溶液中加入 固体,含硫微粒(
固体,含硫微粒( 、
、 、
、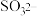 )的lgc和
)的lgc和 的关系如图所示。则曲线①代表的微粒是
的关系如图所示。则曲线①代表的微粒是 时,溶液中三种含硫微粒浓度大小顺序为
时,溶液中三种含硫微粒浓度大小顺序为 值为
值为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】广泛用于纺织工业的连二亚硫酸钠(Na2S2O4),俗称保险粉,是一种强还原剂,可溶于水,但不溶于乙醇,在碱性介质中稳定。
Ⅰ.工业上制备连二亚硫酸钠的流程如下:
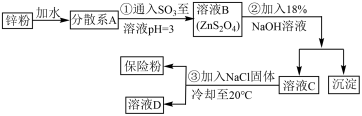
请回答下列问题:
(1)步骤①中的化学方程式为___________________________________ ;
(2)步骤②中沉淀为_________________________________ (填化学式);
(3)步骤③中加入NaCl 固体的作用是______________________________ ,分离出保险粉方法为_______ 、洗涤、干燥,洗涤所用试剂是___________________________
Ⅱ.工业上也可用右图装置电解NaHSO3溶液制Na2S2O4。
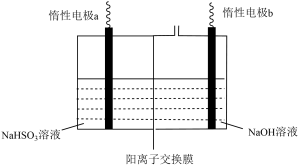
(4)惰性电极a连接电源的_________ (填“正极”或“负极”),其电极反应式为________________ ;
(5)若不加隔膜,则得不到连二亚硫酸钠,其原因是____________________________ 。
Ⅲ.探究Na2S2O4的性质:
某课题小组常温下测定0.050 mol•L-1Na2S2O4溶液在空气中的pH变化如下图所示;
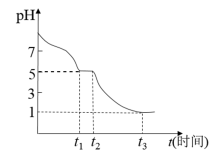
(6)0-t1段主要生成 ,根据pH变化图,写出0- t1发生反应的离子方程式为
,根据pH变化图,写出0- t1发生反应的离子方程式为______________ ;
(7)若t1时溶液中Na2S2O4全部被氧化成NaHSO3,此时溶液中c( )-c(H2SO3) =
)-c(H2SO3) =__________ mol•L-1(填具体数值,不考虑溶液体积变化)
Ⅰ.工业上制备连二亚硫酸钠的流程如下:

请回答下列问题:
(1)步骤①中的化学方程式为
(2)步骤②中沉淀为
(3)步骤③中加入NaCl 固体的作用是
Ⅱ.工业上也可用右图装置电解NaHSO3溶液制Na2S2O4。

(4)惰性电极a连接电源的
(5)若不加隔膜,则得不到连二亚硫酸钠,其原因是
Ⅲ.探究Na2S2O4的性质:
某课题小组常温下测定0.050 mol•L-1Na2S2O4溶液在空气中的pH变化如下图所示;

(6)0-t1段主要生成
 ,根据pH变化图,写出0- t1发生反应的离子方程式为
,根据pH变化图,写出0- t1发生反应的离子方程式为(7)若t1时溶液中Na2S2O4全部被氧化成NaHSO3,此时溶液中c(
 )-c(H2SO3) =
)-c(H2SO3) =
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】工业生产中产生的 、NO直接排放将对大气造成严重污染.利用电化学原理吸收
、NO直接排放将对大气造成严重污染.利用电化学原理吸收 和NO,同时获得
和NO,同时获得  和
和  产品的工艺流程图如下
产品的工艺流程图如下 为铈元素
为铈元素 。
。
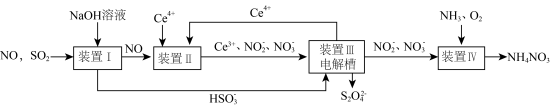
请回答下列问题.
(1)装置Ⅱ中NO在酸性条件下生成 的离子方程式
的离子方程式 ______ .
(2)含硫各微粒 、
、 和
和 存在于
存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数
与NaOH溶液反应后的溶液中,它们的物质的量分数 与溶液pH的关系如图1所示.
与溶液pH的关系如图1所示.
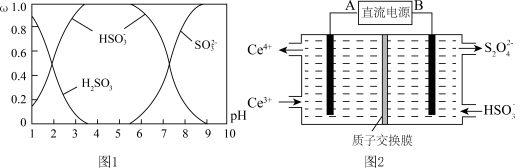
①下列说法正确的是______  填标号
填标号 .
.
A 时,溶液中
时,溶液中


B 由图中数据,可以估算出 的第二级电离平衡常数
的第二级电离平衡常数
C 为获得尽可能纯的 ,应将溶液的pH控制在
,应将溶液的pH控制在  为宜
为宜
D 和
和  时的溶液中所含粒子种类不同
时的溶液中所含粒子种类不同
②若 的NaOH溶液完全吸收
的NaOH溶液完全吸收 标况下
标况下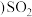 ,则反应的离子方程式为
,则反应的离子方程式为 ______ .
③取装置Ⅰ中的吸收液vmL,用 的酸性高锰酸钾溶液滴定.酸性高锰酸钾溶液应装在
的酸性高锰酸钾溶液滴定.酸性高锰酸钾溶液应装在 ______  填“酸式”或“碱式”
填“酸式”或“碱式” 滴定管中,判断滴定终点的方法是
滴定管中,判断滴定终点的方法是 ______ .
(3)装置Ⅲ的作用之一是再生 ,其原理如图2所示.图中A为电源的
,其原理如图2所示.图中A为电源的 ______  填“正”或“负”
填“正”或“负” 极.右侧反应室中发生的主要电极反应式为
极.右侧反应室中发生的主要电极反应式为 ______ .
(4)已知进入装置Ⅳ的溶液中 的浓度为
的浓度为 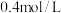 ,要使
,要使  该溶液中的
该溶液中的 完全转化为
完全转化为  ,需至少向装置Ⅳ中通入标准状况下的
,需至少向装置Ⅳ中通入标准状况下的  的体积为
的体积为 ______ L.
 、NO直接排放将对大气造成严重污染.利用电化学原理吸收
、NO直接排放将对大气造成严重污染.利用电化学原理吸收 和NO,同时获得
和NO,同时获得  和
和  产品的工艺流程图如下
产品的工艺流程图如下 为铈元素
为铈元素 。
。
请回答下列问题.
(1)装置Ⅱ中NO在酸性条件下生成
 的离子方程式
的离子方程式 (2)含硫各微粒
 、
、 和
和 存在于
存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数
与NaOH溶液反应后的溶液中,它们的物质的量分数 与溶液pH的关系如图1所示.
与溶液pH的关系如图1所示.
①下列说法正确的是
 填标号
填标号 .
.A
 时,溶液中
时,溶液中


B 由图中数据,可以估算出
 的第二级电离平衡常数
的第二级电离平衡常数
C 为获得尽可能纯的
 ,应将溶液的pH控制在
,应将溶液的pH控制在  为宜
为宜D
 和
和  时的溶液中所含粒子种类不同
时的溶液中所含粒子种类不同②若
 的NaOH溶液完全吸收
的NaOH溶液完全吸收 标况下
标况下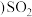 ,则反应的离子方程式为
,则反应的离子方程式为 ③取装置Ⅰ中的吸收液vmL,用
 的酸性高锰酸钾溶液滴定.酸性高锰酸钾溶液应装在
的酸性高锰酸钾溶液滴定.酸性高锰酸钾溶液应装在  填“酸式”或“碱式”
填“酸式”或“碱式” 滴定管中,判断滴定终点的方法是
滴定管中,判断滴定终点的方法是 (3)装置Ⅲ的作用之一是再生
 ,其原理如图2所示.图中A为电源的
,其原理如图2所示.图中A为电源的  填“正”或“负”
填“正”或“负” 极.右侧反应室中发生的主要电极反应式为
极.右侧反应室中发生的主要电极反应式为 (4)已知进入装置Ⅳ的溶液中
 的浓度为
的浓度为 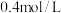 ,要使
,要使  该溶液中的
该溶液中的 完全转化为
完全转化为  ,需至少向装置Ⅳ中通入标准状况下的
,需至少向装置Ⅳ中通入标准状况下的  的体积为
的体积为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
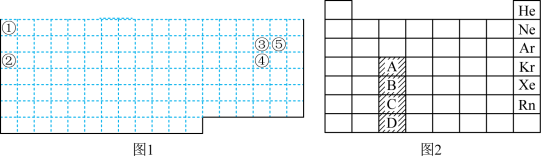
【推荐1】如图1的实线表示元素周期表的部分边界.①~⑤分别表示元素周期表中对应位置的元素.
(1)③④⑤的氢化物稳定性由强到弱的顺序是__________ (用化学式表示).
(2)写出②含有12个中子的核素的化学符号__________
(3)M、N两种化合物均由①②③④四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式__________ .
(4)X、Y、Z代表原子序数依次增大的三种短周期元素.在周期表中,Y与X相邻,Y与Z也相邻;X、Y和Z三种元素原子的最外层电子数之和为17;X、Y、Z三种元素有的是上表中编号①~⑤的元素,有的不是,不是①~⑤的元素在周期表中的位置为________ .X、Y、Z和①可组成一化合物,其原子个数比为2﹕4﹕1﹕8,该化合物所含化学键类型为___________________
(5)某同学受镧系、锕系元素排列方式的启发,将元素周期表设计成下列更简明的形式,把118种元素全部排列在内,图2除A、B、C、D外每个位置只表示一种元素.则该图的A位置包含__________ (填数字)种元素.C位置中的元素是否全部是金属元素__________ (填“是”或“否”).
(1)③④⑤的氢化物稳定性由强到弱的顺序是
(2)写出②含有12个中子的核素的化学符号
(3)M、N两种化合物均由①②③④四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式
(4)X、Y、Z代表原子序数依次增大的三种短周期元素.在周期表中,Y与X相邻,Y与Z也相邻;X、Y和Z三种元素原子的最外层电子数之和为17;X、Y、Z三种元素有的是上表中编号①~⑤的元素,有的不是,不是①~⑤的元素在周期表中的位置为
(5)某同学受镧系、锕系元素排列方式的启发,将元素周期表设计成下列更简明的形式,把118种元素全部排列在内,图2除A、B、C、D外每个位置只表示一种元素.则该图的A位置包含

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】现有部分短周期主族元素的性质或原子结构如下表:
(1)元素Z在周期表中的位置 ,XN2的结构式是: ,
(2)元素X的一种核素可测定文物年代,这种核素的符号是 ;
(3)在X、Y最低价的简单氢化物中,较稳定的化合物的分子式是 。
(4)将少量W2 N2固体投入到水中,剧烈反应,其反应的化学方程式为: 。
(5)下列表述中,能证明元素Z与元素T非金属性的强弱的是
A、常温下Z的单质和T的单质状态不同
B、Z的氢化物比T的氢化物稳定
C、一定条件下Z和T的单质都能与氢氧化钠溶液反
| 元素符号 | 原子结构和元素性质 |
| T | M层上有6个电子 |
| W | 短周期内原子半径最大 |
| N | 原子序数比T小,且与T同主族 |
| X | 最外层电子数是次外层的2倍 |
| Y | 常见单质为双原子分子且氢化物的水溶液呈碱性 |
| Z | 元素最高价为+7 |
(2)元素X的一种核素可测定文物年代,这种核素的符号是 ;
(3)在X、Y最低价的简单氢化物中,较稳定的化合物的分子式是 。
(4)将少量W2 N2固体投入到水中,剧烈反应,其反应的化学方程式为: 。
(5)下列表述中,能证明元素Z与元素T非金属性的强弱的是
A、常温下Z的单质和T的单质状态不同
B、Z的氢化物比T的氢化物稳定
C、一定条件下Z和T的单质都能与氢氧化钠溶液反
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-半径,Y的氧化物是形成酸雨的主要物质之一。
请回答:
(1)Q元素在周期表中的位置_______
(2)将这五种元素原子半径从大到小排列,排在第三的元素原子是______ (填元素符号)
(3)元素的非金属性Z__ Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有____________ (填序号)
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4) X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,写出A的电子式_________ ;B的水溶液不呈中性的原因____________ (用离子方程式表示)
(5) 液态A类似X2Z能微弱电离且产生电子数相同的两种离子,则液态A的电离方程式为
__________________
(6)若使A按下列途径完全转化为F:
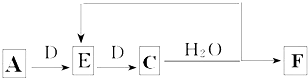
①F的化学式为________ ;
②参加反应的A与完全转化为F时整个过程中消耗D的物质的量之比为________
请回答:
(1)Q元素在周期表中的位置
(2)将这五种元素原子半径从大到小排列,排在第三的元素原子是
(3)元素的非金属性Z
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4) X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,写出A的电子式
(5) 液态A类似X2Z能微弱电离且产生电子数相同的两种离子,则液态A的电离方程式为
(6)若使A按下列途径完全转化为F:

①F的化学式为
②参加反应的A与完全转化为F时整个过程中消耗D的物质的量之比为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】I.连二次硝酸(H2N2O2)是一种二元酸。可用于制NO气体。常温下,用0.01 的NaOH溶液滴定10mL0.01
的NaOH溶液滴定10mL0.01 的H2N2O2溶液。测得溶液pH与NaOH溶液体积的关系如图所示。
的H2N2O2溶液。测得溶液pH与NaOH溶液体积的关系如图所示。
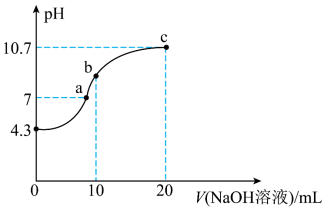
(1)N的价层电子排布图为:_______ 。
(2)常温下H2N2O2的Ka1为_______ 。
(3)b点时溶液中
_______  (填“>”“﹤”“=”,下同)。
(填“>”“﹤”“=”,下同)。
(4)a、b、c三点,水的电离程度最小的是_______ 。
II.25℃时,有浓度均为0.10 的下列4种溶液:①NaCN溶液;②NaOH溶液;③CH3COOH溶液;④NaHCO3溶液。相关电离常数如表所示。
的下列4种溶液:①NaCN溶液;②NaOH溶液;③CH3COOH溶液;④NaHCO3溶液。相关电离常数如表所示。
(5)这4种溶液pH由小到大的顺序是_______ (填序号)。
(6)①中各离子浓度由小到大的顺序是_______ 。
(7)CH3COOH和CH3COONa混合溶液中,若溶液pH=6,则溶液中
_______  (填精确值)。
(填精确值)。
 的NaOH溶液滴定10mL0.01
的NaOH溶液滴定10mL0.01 的H2N2O2溶液。测得溶液pH与NaOH溶液体积的关系如图所示。
的H2N2O2溶液。测得溶液pH与NaOH溶液体积的关系如图所示。
(1)N的价层电子排布图为:
(2)常温下H2N2O2的Ka1为
(3)b点时溶液中

 (填“>”“﹤”“=”,下同)。
(填“>”“﹤”“=”,下同)。(4)a、b、c三点,水的电离程度最小的是
II.25℃时,有浓度均为0.10
 的下列4种溶液:①NaCN溶液;②NaOH溶液;③CH3COOH溶液;④NaHCO3溶液。相关电离常数如表所示。
的下列4种溶液:①NaCN溶液;②NaOH溶液;③CH3COOH溶液;④NaHCO3溶液。相关电离常数如表所示。| HCN | H2CO3 | CH3COOH |
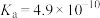 |  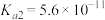 |  |
(6)①中各离子浓度由小到大的顺序是
(7)CH3COOH和CH3COONa混合溶液中,若溶液pH=6,则溶液中

 (填精确值)。
(填精确值)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】回答以下关于元素及其化合物的问题.
(1)下列状态的铝中,最外层电离出一个电子所需要能量由大到小的顺序______________ (填标号)。______________ ,基态氧原子的价层电子不是重排结构,原因是不符合______________ 。
(3)下图中分别代表了碳单质的两种常见晶体,碳元素位于元素周期表的______________ 区;图1晶体中1个最小六元环平均含有C原子数与图2晶体中1个最小六元环平均含有C原子数之比为______________ ;图3是石墨层间插入氟得到层状结构化合物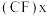 ,该物质仍具润滑性,与石墨相比,
,该物质仍具润滑性,与石墨相比,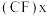 导电性
导电性______________ (填“增强”或“减弱”)。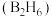 、丁硼烷
、丁硼烷 等.乙硼烷的结构式如图
等.乙硼烷的结构式如图 。分子中B原子通过氢桥键(
。分子中B原子通过氢桥键(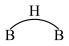 )形成一个四元环。丁硼烷
)形成一个四元环。丁硼烷 分子中存在4个氢桥键且有两个五元环,写出其结构式
分子中存在4个氢桥键且有两个五元环,写出其结构式______________ 。
(1)下列状态的铝中,最外层电离出一个电子所需要能量由大到小的顺序
A.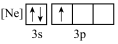 B.
B.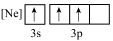 C.
C.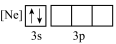 D.
D.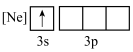
(3)下图中分别代表了碳单质的两种常见晶体,碳元素位于元素周期表的
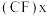 ,该物质仍具润滑性,与石墨相比,
,该物质仍具润滑性,与石墨相比,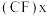 导电性
导电性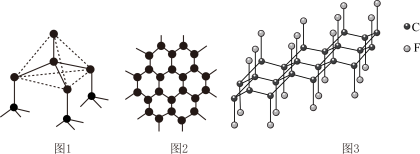
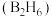 、丁硼烷
、丁硼烷 等.乙硼烷的结构式如图
等.乙硼烷的结构式如图 。分子中B原子通过氢桥键(
。分子中B原子通过氢桥键( )形成一个四元环。丁硼烷
)形成一个四元环。丁硼烷 分子中存在4个氢桥键且有两个五元环,写出其结构式
分子中存在4个氢桥键且有两个五元环,写出其结构式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】稀土元素是指钪(Sc)、钇(Y)和镧系元素,共17种,位于元素周期表中第ⅢB族,均为金属元素,在工业生产中有重要的作用。回答下列问题:
(1)基态钪(Sc)元素的原子核外电子占据的轨道数目共_____ 个,钇(Y)位于元素周期表中钪(Sc)的下一周期,钇(Y)的价电子轨道表达式为_____ 。
(2)稀土元素常常能和许多配位体形成配合物。若一个配位体含有两个或两个以上的能提供孤电子对的原子,这种配位体就叫多齿配位体,有一个能提供孤电子对的原子为一齿,(羰基中的氧原子不能提供孤对电子),EDTA( )是
)是_____ 齿配位体,EDTA所含元素原子第一电离能由大到小顺序为_____ 。
(3)钪(Sc)离子在水中以稳定对称的 存在,其中O-Sc-O的键角只有90度和180度两种,其空间构型为
存在,其中O-Sc-O的键角只有90度和180度两种,其空间构型为_____ 。
(4)甘氨酸铜有顺式和反式两种同分异构体,结构如下图。

①甘氨酸铜中铜原子的杂化类型为_____ (填“ ”或“
”或“ ”)。
”)。
②已知顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因可能是_____ 。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。铁酸钇( )的正交相晶胞结构以及各原子的投影位置如图所示,晶胞棱边夹角均为90°。
)的正交相晶胞结构以及各原子的投影位置如图所示,晶胞棱边夹角均为90°。
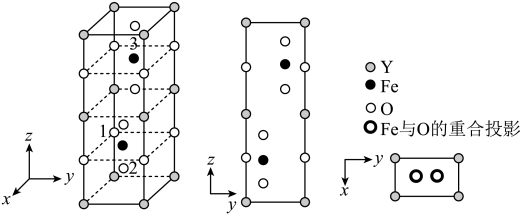
一个晶胞中有_____ 个O。已知1号O原子分数坐标为 ,2号O原子分数坐标为
,2号O原子分数坐标为 ,则3号Fe原子的分数坐标为
,则3号Fe原子的分数坐标为_____ 。
(1)基态钪(Sc)元素的原子核外电子占据的轨道数目共
(2)稀土元素常常能和许多配位体形成配合物。若一个配位体含有两个或两个以上的能提供孤电子对的原子,这种配位体就叫多齿配位体,有一个能提供孤电子对的原子为一齿,(羰基中的氧原子不能提供孤对电子),EDTA(
 )是
)是(3)钪(Sc)离子在水中以稳定对称的
 存在,其中O-Sc-O的键角只有90度和180度两种,其空间构型为
存在,其中O-Sc-O的键角只有90度和180度两种,其空间构型为(4)甘氨酸铜有顺式和反式两种同分异构体,结构如下图。

①甘氨酸铜中铜原子的杂化类型为
 ”或“
”或“ ”)。
”)。②已知顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因可能是
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。铁酸钇(
 )的正交相晶胞结构以及各原子的投影位置如图所示,晶胞棱边夹角均为90°。
)的正交相晶胞结构以及各原子的投影位置如图所示,晶胞棱边夹角均为90°。
一个晶胞中有
 ,2号O原子分数坐标为
,2号O原子分数坐标为 ,则3号Fe原子的分数坐标为
,则3号Fe原子的分数坐标为
您最近一年使用:0次