氮气是空气的重要组成气体,氮气的综合利用在农业和国防中有着重要意义。
(1)合成氨从实验室研究到实现工业生产,大约经历了150 年。
①写出工业合成氨的化学方程式___________
②已知该反应的ΔH= -92.4 kJ/mol, ΔS (T =298K) =- 198.76 J·mol -1·K-1,试判断室温(即298K) 下,合成氨的反应能否自发进行?___________ (填“能”或“否”)
(2) NH3和CO2在120 °C,催化剂作用下可以合成尿素。
①写出该反应的化学方程式___________
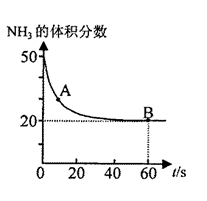
②混合气体中NH3 的含量变化关系如图所示(该条件下尿素为固体)。则A点的正反应速率v正 (CO2)___________ B点的逆反应速率为v逆(CO2) (填“大于”、“小于”或“等于”),NH3的平衡转化率为___________
(3) NH3可用工业上生产硝酸,其尾气中的NO2可用氨水吸收生成NH4NO3.25 °C时,将a mol NH4NO3溶于水,溶液显酸性,其原因是___________ (用离子方程式表示)向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将___________ (填 “正向”、“不”或“逆向”移动,所滴加氨水的浓度为___________ mol·L-1(25 °C时,NH3·H2O 的电离平衡常数取Kb= 2 ×10-5 mol·L-1)
(1)合成氨从实验室研究到实现工业生产,大约经历了150 年。
①写出工业合成氨的化学方程式
②已知该反应的ΔH= -92.4 kJ/mol, ΔS (T =298K) =- 198.76 J·mol -1·K-1,试判断室温(即298K) 下,合成氨的反应能否自发进行?
(2) NH3和CO2在120 °C,催化剂作用下可以合成尿素。
①写出该反应的化学方程式
②混合气体中NH3 的含量变化关系如图所示(该条件下尿素为固体)。则A点的正反应速率v正 (CO2)

(3) NH3可用工业上生产硝酸,其尾气中的NO2可用氨水吸收生成NH4NO3.25 °C时,将a mol NH4NO3溶于水,溶液显酸性,其原因是
更新时间:2021-08-03 09:41:32
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】非金属元素在化工生产中扮演着重要的角色。在众多的化工原料和产品中,都能见到硫和氮等元素的踪迹。
I.物质类别和元素价态,是学习元素及其化合物性质的重要认识视角。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:

(1)Y与O2反应的化学方程式:___________ 。
(2)将足量的Y气体通入下列溶液中,始终没有明显反应现象的是___________。
II.氨在国民经济中占有重要的地位。现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
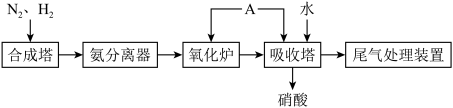
(3)写出氧化炉中的化学反应方程式___________ 。
(4)在氨分离器中,利用氨气___________ 性质可以将氨气从混合气体中分离出来。
(5)向吸收塔中通入A的作用是___________ 。
I.物质类别和元素价态,是学习元素及其化合物性质的重要认识视角。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:

(1)Y与O2反应的化学方程式:
(2)将足量的Y气体通入下列溶液中,始终没有明显反应现象的是___________。
| A.Ba(NO3)2溶液 | B.FeCl3溶液 | C.H2O2溶液 | D.CaCl2溶液 |
II.氨在国民经济中占有重要的地位。现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

(3)写出氧化炉中的化学反应方程式
(4)在氨分离器中,利用氨气
(5)向吸收塔中通入A的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空。
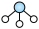
(1)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德•埃特尔在哈伯研究所证实了N2与H2在固体催化剂表面合成氨的反应过程。示意图如图( 、
、 、
、 分别表示N2、H2、NH3):
分别表示N2、H2、NH3):
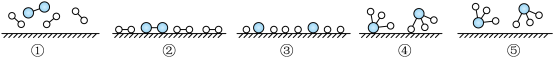
图②表示N2、H2被吸附在催化剂表面,图⑤表示生成的NH3离开催化剂表面,则图③表示___________ ,写出哈伯法合成氨的化学方程式___________ 。
(2)实验室利用复分解反应原理制取NH3的化学方程式是___________ 。
(3)合成法制硝酸是以NH3为原料,经催化氧化后再用水吸收来实现的。写出NH3催化氧化的化学方程式___________ ;若开始时投入17吨NH3,最后生产出的硝酸为42吨,则硝酸的产率是___________ 。
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应最好使用___________ (填“浓”或“稀”)硝酸,结合化学用语简述选择的理由___________ 。
(1)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德•埃特尔在哈伯研究所证实了N2与H2在固体催化剂表面合成氨的反应过程。示意图如图(
 、
、 、
、 分别表示N2、H2、NH3):
分别表示N2、H2、NH3):
图②表示N2、H2被吸附在催化剂表面,图⑤表示生成的NH3离开催化剂表面,则图③表示
(2)实验室利用复分解反应原理制取NH3的化学方程式是
(3)合成法制硝酸是以NH3为原料,经催化氧化后再用水吸收来实现的。写出NH3催化氧化的化学方程式
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应最好使用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】依据如图中氮元素及其化合物的转化关系,回答问题:
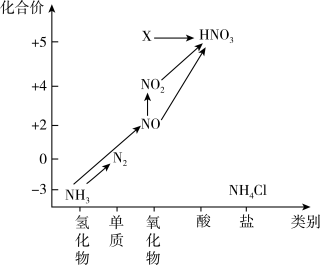
(1)图中, 的化学式为
的化学式为 _______ ,从化合价上看, 具有
具有 _______ 性 “氧化”、“还原”
“氧化”、“还原” 。
。
(2)回答下列关于 的问题:
的问题:
①实验室常用 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为 _______ 。
②下列试剂能用于干燥 的是
的是 _______  填字母
填字母 。
。
A.浓硫酸 B.碱石灰 C.无水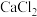
③若要收集一瓶氨气,请将上述装置补充完整,在图中虚框内画出连接图_______ 。
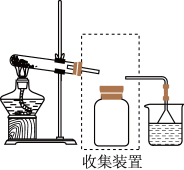
④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式_______ 。
(3)回答下列关于 、
、 的问题:
的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体 和
和 反应可转化为无害气体排放,写出相关反应的化学方程式:
反应可转化为无害气体排放,写出相关反应的化学方程式:_______ 。
② 和
和 按一定比例混合可以被
按一定比例混合可以被 溶液完全吸收,写出相关化学方程式
溶液完全吸收,写出相关化学方程式 _______ 。

(1)图中,
 的化学式为
的化学式为  具有
具有  “氧化”、“还原”
“氧化”、“还原” 。
。(2)回答下列关于
 的问题:
的问题:①实验室常用
 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为 ②下列试剂能用于干燥
 的是
的是  填字母
填字母 。
。A.浓硫酸 B.碱石灰 C.无水
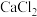
③若要收集一瓶氨气,请将上述装置补充完整,在图中虚框内画出连接图

④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式
(3)回答下列关于
 、
、 的问题:
的问题:①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体
 和
和 反应可转化为无害气体排放,写出相关反应的化学方程式:
反应可转化为无害气体排放,写出相关反应的化学方程式:②
 和
和 按一定比例混合可以被
按一定比例混合可以被 溶液完全吸收,写出相关化学方程式
溶液完全吸收,写出相关化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】目前工业上可利用 CO 或 CO2 来生产燃料甲醇,某研究小组对下列有关甲醇制取的三 个化学反应进行了探究。已知在不同温度下的化学平衡常数(K1、K2、K3)如表所示。
请回答下列问题:
(1)反应②是_____ (填“吸热”或“放热”)反应;反应③的平衡常数表达式为 K=_____ ;
(2)根据反应①与②可推导出 K1、K2 与 K3 之间的关系,则 K3=_____ (用 K1、K2 表示);根据反应③判断ΔS_____ (填“>”“=”或“<”)0,在_____ (填“较高”或“较低”)温度下有利于该反应自 发进行。
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有___________ (填字母,后同)。
A.缩小反应容器的容积 B.增大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.从平衡体系中及时分离出 CH3OH
(4)500 ℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为 0.1 mol·L-1、0.8 mol·L-1、0.3 mol·L-1、0.15 mol·L-1,则此时 v(正)__________ v(逆)(填“>”“=”或“<”)。
| 化学反应 | 焓变 | 平衡 常数 | 温度/℃ | ||
| 500 | 700 | 800 | |||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | ΔH1 | K1 | 2.5 | 0.34 | 0.15 |
②CO2(g)+H2(g) CO(g)+H2O(g) CO(g)+H2O(g) | ΔH2 | K2 | 1.0 | 1.70 | 2.52 |
③CO2(g)+3H2(g) CH3OH(g)+H2O(g) CH3OH(g)+H2O(g) | ΔH3 | K3 | |||
请回答下列问题:
(1)反应②是
(2)根据反应①与②可推导出 K1、K2 与 K3 之间的关系,则 K3=
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有
A.缩小反应容器的容积 B.增大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.从平衡体系中及时分离出 CH3OH
(4)500 ℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为 0.1 mol·L-1、0.8 mol·L-1、0.3 mol·L-1、0.15 mol·L-1,则此时 v(正)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法I.氨热分解法制氢气
相关化学键的键能数据
在一定温度下,利用催化剂将NH3分解为N2和H2。回答下列问题:
(1)反应2NH3(g) N2(g)+3H2(g) ∆H=
N2(g)+3H2(g) ∆H=___________ kJ/mol;
(2)已知该反应的∆S=198.9J·mol-1·K-1,在下列哪些温度下反应能自发进行?___________(填标号);(T(K)=t(℃)+273.15)
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol NH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
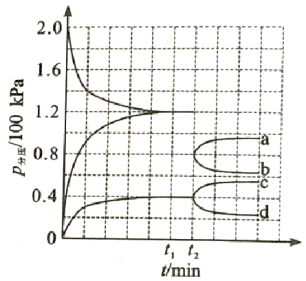
①若保持容器体积不变,t1时反应达到平衡,用H2的浓度变化表示0~ t1时间内的反应速率v(H2)=___________ mol·L-1·min-1 (用含t1的代数式表示);
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________ ;
③在该温度下,反应的标准平衡常数KΘ=___________ 。
(已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g) gG(g)+hH(g)
gG(g)+hH(g)
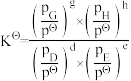 ,其中pΘ=100kPa,pG、pH、pD、pE为各组分的平衡分压)。
,其中pΘ=100kPa,pG、pH、pD、pE为各组分的平衡分压)。
(4)NH3用途广泛,写出基于其物理性质的一种用途:___________ 。
方法I.氨热分解法制氢气
相关化学键的键能数据
| 化学键 | N≡N | H-H | N-H |
| 键能E/(kJ·mol-1) | 946 | 436.0 | 390.8 |
(1)反应2NH3(g)
 N2(g)+3H2(g) ∆H=
N2(g)+3H2(g) ∆H=(2)已知该反应的∆S=198.9J·mol-1·K-1,在下列哪些温度下反应能自发进行?___________(填标号);(T(K)=t(℃)+273.15)
| A.25℃ | B.125℃ | C.225℃ | D.325℃ |

①若保持容器体积不变,t1时反应达到平衡,用H2的浓度变化表示0~ t1时间内的反应速率v(H2)=
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是
③在该温度下,反应的标准平衡常数KΘ=
(已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g)
 gG(g)+hH(g)
gG(g)+hH(g)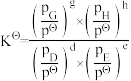 ,其中pΘ=100kPa,pG、pH、pD、pE为各组分的平衡分压)。
,其中pΘ=100kPa,pG、pH、pD、pE为各组分的平衡分压)。(4)NH3用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知甲烷隔绝空气在不同温度下有可能发生如下两个反应:①CH4(g)=C(s)+2H2(g),②2CH4(g)=C2H2(g)+3H2(g)。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,在图书馆查到了如下热力学数据:反应①的ΔH(298 K) =74.848 kJ·mol-1,ΔS(298 K)=80.674 J·mol-1·K-1;反应②的ΔH(298 K)=376.426 kJ·mol-1,ΔS(298 K)=220.211 J·mol-1·K-1。已知焓变和熵变随温度变化很小。请帮助这位同学考虑如下问题:
(1)判断反应②高温自发还是低温自发:_______ (填“高温”或“低温”)。
(2)通过计算判断反应①在常温下能否自发进行_______ (填“能”或“不能”)。
(3)求算制取炭黑的允许温度范围_______ 。
(1)判断反应②高温自发还是低温自发:
(2)通过计算判断反应①在常温下能否自发进行
(3)求算制取炭黑的允许温度范围
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】994 K,当H2缓慢通过过量的块状固体CoO时,部分CoO被还原为固体Co。在流出的平衡气体中H2的物质的量分数为2.50%; 在同一温度,若用CO还原固体CoO时平衡气体中CO的物质的量分数为1.92%。 如果994 K时物质的量比为1:2的一氧化碳和水蒸气的混合物在一定条件下反应,问:
(1)一氧化碳的平衡转化率大约是多少___________ ?
(2)欲获得较纯的H2,请简要说明在生产工艺上应采取的措施___________ 。
(3)994 K,当H2缓慢通过过量的纳米CoO固体粉末时,部分CoO被还原为固体Co。在相同的反应时间内,与块状固体CoO相比,采用纳米固体CoO时流出的平衡气体中H2的物质的量分数将怎样变化___________ ?为什么___________ ?
(1)一氧化碳的平衡转化率大约是多少
(2)欲获得较纯的H2,请简要说明在生产工艺上应采取的措施
(3)994 K,当H2缓慢通过过量的纳米CoO固体粉末时,部分CoO被还原为固体Co。在相同的反应时间内,与块状固体CoO相比,采用纳米固体CoO时流出的平衡气体中H2的物质的量分数将怎样变化
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在一个体积为1L的真空密闭容器中加入0.5molCaCO3,发生反应: CaCO3(s)  CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图所示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图所示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:

(1)下列有关说法正确的是___________
A.该反应的ΔH>0
B.对于可逆反应,若正反应自发进行,则逆反应必不能自发进行
C.在T5°C下,压缩容器为0.5L,则达到平衡后0.2 mol·L-1<c(CO2) <0.4 mol·L-1
D.在T5°C下,体积不变的容器中,容器内压强不变或者气体的密度不变均表明已经达到平衡状态
(2)请说明随着温度的升高,曲线B向曲线A逼近的原因是___________ 。
(3)在T5°C下,维持温度和容器体积不变,向上述平衡体系中再充入0.5mol N2,则最后平衡时容器中的CaCO3的质量为___________ g.若在T5°C下维持温度和总压强不变,充入0.1molN2,容器中最后残留的CaCO3质量为___________ g。
 CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图所示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图所示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
(1)下列有关说法正确的是
A.该反应的ΔH>0
B.对于可逆反应,若正反应自发进行,则逆反应必不能自发进行
C.在T5°C下,压缩容器为0.5L,则达到平衡后0.2 mol·L-1<c(CO2) <0.4 mol·L-1
D.在T5°C下,体积不变的容器中,容器内压强不变或者气体的密度不变均表明已经达到平衡状态
(2)请说明随着温度的升高,曲线B向曲线A逼近的原因是
(3)在T5°C下,维持温度和容器体积不变,向上述平衡体系中再充入0.5mol N2,则最后平衡时容器中的CaCO3的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在一固定容积的密闭容器中,进行如下化学反应:CO2(g) + H2(g)⇌CO(g) + H2O(g)。其化学平衡常数K和温度t的关系如下:
请回答:
(1)上述反应正向进行时,反应为_______ 热反应(填“放”或“吸”)。
(2)能判断该反应已经达到化学平衡状态的依据是_______ 。
a.容器内压强不变 b.v正(H2) = v逆(CO) c.CO2的质量分数不变
(3)温度为850℃时,可逆反应CO (g) + H2O (g)⇌CO2 (g) + H2 (g) 在固定容积的密闭容器中进行,容器内各物质的浓度变化如下:
计算:3min时(CO的浓度)c1 =_______ mol/L,H2O (g)的转化率=_______ 。
(4)表中5min~6min之间数值发生变化,可能的原因是_______(单选)。
| t/℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答:
(1)上述反应正向进行时,反应为
(2)能判断该反应已经达到化学平衡状态的依据是
a.容器内压强不变 b.v正(H2) = v逆(CO) c.CO2的质量分数不变
(3)温度为850℃时,可逆反应CO (g) + H2O (g)⇌CO2 (g) + H2 (g) 在固定容积的密闭容器中进行,容器内各物质的浓度变化如下:
| 时间/min | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
计算:3min时(CO的浓度)c1 =
(4)表中5min~6min之间数值发生变化,可能的原因是_______(单选)。
| A.增加水蒸气 | B.降低温度 | C.使用催化剂 | D.增加氢气浓度 |
您最近一年使用:0次



