994 K,当H2缓慢通过过量的块状固体CoO时,部分CoO被还原为固体Co。在流出的平衡气体中H2的物质的量分数为2.50%; 在同一温度,若用CO还原固体CoO时平衡气体中CO的物质的量分数为1.92%。 如果994 K时物质的量比为1:2的一氧化碳和水蒸气的混合物在一定条件下反应,问:
(1)一氧化碳的平衡转化率大约是多少___________ ?
(2)欲获得较纯的H2,请简要说明在生产工艺上应采取的措施___________ 。
(3)994 K,当H2缓慢通过过量的纳米CoO固体粉末时,部分CoO被还原为固体Co。在相同的反应时间内,与块状固体CoO相比,采用纳米固体CoO时流出的平衡气体中H2的物质的量分数将怎样变化___________ ?为什么___________ ?
(1)一氧化碳的平衡转化率大约是多少
(2)欲获得较纯的H2,请简要说明在生产工艺上应采取的措施
(3)994 K,当H2缓慢通过过量的纳米CoO固体粉末时,部分CoO被还原为固体Co。在相同的反应时间内,与块状固体CoO相比,采用纳米固体CoO时流出的平衡气体中H2的物质的量分数将怎样变化
2013高二·广东·竞赛 查看更多[1]
更新时间:2021/08/03 23:02:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g) Fe(s)+CO2(g)ΔH>0
Fe(s)+CO2(g)ΔH>0
其平衡常数可表示为K=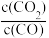 ,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比___________ ,平衡常数K___________ 。(以上均填“增大”“减小”或“不变”)
(2)1100℃时测得高炉中c(CO2)=0.025mol·L-1、c(CO)=0.1mol·L-1,在这种情况下,该反应是否处于化学平衡状态:___________ (填“是”或“否”,若填“是”,则后面问题可不答),此时反应向___________ (填“正反应”或“逆反应”)方向进行,其原因是___________ 。
 Fe(s)+CO2(g)ΔH>0
Fe(s)+CO2(g)ΔH>0其平衡常数可表示为K=
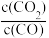 ,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
,已知1100℃时K=0.263.化学平衡常数只与温度有关,不随浓度和压强的变化而变化。(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比
(2)1100℃时测得高炉中c(CO2)=0.025mol·L-1、c(CO)=0.1mol·L-1,在这种情况下,该反应是否处于化学平衡状态:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在一定条件下xA+yB⇌zC的可逆反应达到平衡,
(1)已知A、B、C均为气体,在减压后平衡向逆反应方向移动,则x、y、z的关系是__________ .
(2)已知C是气体且x+y=z,在加压时如果平衡发生移动,则平衡必向__________ 方向移动.(填“正反应”或“逆反应”)
(3)已知B、C是气体,现增加A的物质的量(其他条件不变),平衡不移动,则A是__________ 态.
(1)已知A、B、C均为气体,在减压后平衡向逆反应方向移动,则x、y、z的关系是
(2)已知C是气体且x+y=z,在加压时如果平衡发生移动,则平衡必向
(3)已知B、C是气体,现增加A的物质的量(其他条件不变),平衡不移动,则A是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】勒夏特列原理在生产生活中有许多重要应用。完成下列填空:
(1)实验室配置FeCl3溶液时,将FeCl3溶解在盐酸中,目的是防止________________________ 。
(2)石蕊(用HZ表示)试液中存在的电离平衡HZ(红色) H++Z—(蓝色)。在中性溶液中。石蕊试液呈
H++Z—(蓝色)。在中性溶液中。石蕊试液呈__________ 色;要使石蕊试液呈红色,可加入____________________________ 。
(3)工业制硫酸时,为使SO2尽可能多地转化成SO3,采取的措施是_______________________ 。
(4)合成氨工业采取的以下措施中,可以用勒夏特列原理解释的是_________ (选填编号)。
a.升温至500℃左右 b.使用催化剂
c.加压至20~50MPA. d.将氨及时液化分离
(1)实验室配置FeCl3溶液时,将FeCl3溶解在盐酸中,目的是防止
(2)石蕊(用HZ表示)试液中存在的电离平衡HZ(红色)
 H++Z—(蓝色)。在中性溶液中。石蕊试液呈
H++Z—(蓝色)。在中性溶液中。石蕊试液呈(3)工业制硫酸时,为使SO2尽可能多地转化成SO3,采取的措施是
(4)合成氨工业采取的以下措施中,可以用勒夏特列原理解释的是
a.升温至500℃左右 b.使用催化剂
c.加压至20~50MPA. d.将氨及时液化分离
您最近半年使用:0次
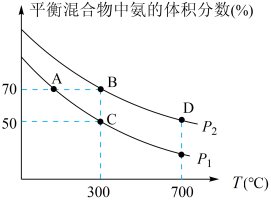
【推荐1】氨在国民经济中占有重要地位,在科学技术和生产中有重要应用。合成氨反应起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。
(1)恒压时, 反应一定达到平衡状态的标志是
反应一定达到平衡状态的标志是______ (选填字母)
A. 和
和 的转化率相等
的转化率相等
B.反应体系密度保持不变
C.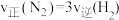
D.断开3molH—H键的同时断开6molN—H键
(2)
_____  (填“>”“=”或“<”,下同);反应的平衡常数:B点
(填“>”“=”或“<”,下同);反应的平衡常数:B点_____ C点。
(3)C点 的转化率为
的转化率为_______ 。(精确到小数点后一位)
(4)为提高合成氨的衡产率,下列可以采取的措施有____________ 。
A.增大压强 B.升高温度 C.使用铁触媒 D.将生成的 及时从混合气体中分离出去
及时从混合气体中分离出去

(1)恒压时,
 反应一定达到平衡状态的标志是
反应一定达到平衡状态的标志是A.
 和
和 的转化率相等
的转化率相等 B.反应体系密度保持不变
C.
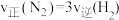
D.断开3molH—H键的同时断开6molN—H键
(2)

 (填“>”“=”或“<”,下同);反应的平衡常数:B点
(填“>”“=”或“<”,下同);反应的平衡常数:B点(3)C点
 的转化率为
的转化率为(4)为提高合成氨的衡产率,下列可以采取的措施有
A.增大压强 B.升高温度 C.使用铁触媒 D.将生成的
 及时从混合气体中分离出去
及时从混合气体中分离出去
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业上通过将CO、CO2与氢气反应,实现碳中和。
(1)已知反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g) ΔH。根据理论计算,在恒压、起始物质的量之比n(CO2):n(H2)=1:3条件下,该反应达平衡时各组分的物质的量分数随温度变化的曲线如图-1所示。
C2H4(g)+4H2O(g) ΔH。根据理论计算,在恒压、起始物质的量之比n(CO2):n(H2)=1:3条件下,该反应达平衡时各组分的物质的量分数随温度变化的曲线如图-1所示。
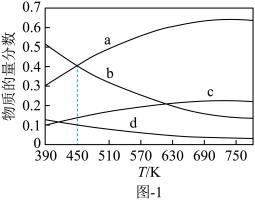
①该反应的平衡常数表达式为_______ ,该反应的ΔH_______ 0(填“>”或“<”)
②图中曲线a、d分别表示的是平衡时_______ 和_______ 的物质的量分数变化。
(2)用CO和H2合成CH3OH的反应为CO(g)+2H2(g) CH3OH(g) ΔH <0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图-2所示。
CH3OH(g) ΔH <0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图-2所示。
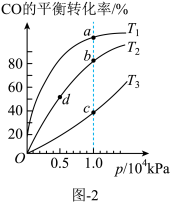
①图中T1、T2、T3的大小关系为_______
②图中b、c、d点上正反应速率的关系为_______
③图中a、b、d点上平衡常数的大小关系为_______
(1)已知反应2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g) ΔH。根据理论计算,在恒压、起始物质的量之比n(CO2):n(H2)=1:3条件下,该反应达平衡时各组分的物质的量分数随温度变化的曲线如图-1所示。
C2H4(g)+4H2O(g) ΔH。根据理论计算,在恒压、起始物质的量之比n(CO2):n(H2)=1:3条件下,该反应达平衡时各组分的物质的量分数随温度变化的曲线如图-1所示。
①该反应的平衡常数表达式为
②图中曲线a、d分别表示的是平衡时
(2)用CO和H2合成CH3OH的反应为CO(g)+2H2(g)
 CH3OH(g) ΔH <0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图-2所示。
CH3OH(g) ΔH <0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图-2所示。
①图中T1、T2、T3的大小关系为
②图中b、c、d点上正反应速率的关系为
③图中a、b、d点上平衡常数的大小关系为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】在一定体积的密闭容器中,进行如下化学反应:CH4(g)+H2O(g) CO(g)+3H2(g),不同温度下达到平衡时,反应体系中各物质的浓度如下表:
CO(g)+3H2(g),不同温度下达到平衡时,反应体系中各物质的浓度如下表:
(1)该反应的平衡常数表达式为K=______________ ,正反应为_________ 反应(填放热、吸热)。
(2)能判断该反应是否已达到化学平衡状态的依据是_________
a.容器压强不变 b.c(CH4)=c(H2O)
c.v正(CH4)=v逆(H2) d .混合气体中c(CO)不变
氮化铝是共价键化合物,高碳热还原制备氮化铝的总反应化学方程式为(未配平):
Al2O3(s)+C(s)+N2(g)→AlN(s)+CO(g) ……①
某氮化铝样品中含有氧化铝杂质.已知氮化铝和NaOH溶液能反应,并产生氨气,其反应方程式为:AlN+NaOH+H2O→NaAlO2+NH3↑……②,
氧化铝也能与氢氧化钠溶液反应而全部溶解……③
(3)配平化学化学方程式①:___ Al2O3(s)+ C(s)+ N2(g)→ AlN(s)+ CO(g)
(4)反应②中产生气体的检验方法为____________________________________________ ;
反应③的离子方程式___________________________________________________________ 。
 CO(g)+3H2(g),不同温度下达到平衡时,反应体系中各物质的浓度如下表:
CO(g)+3H2(g),不同温度下达到平衡时,反应体系中各物质的浓度如下表:温度 | CH4(g) | H2O(g) | CO(g) | H2(g) |
500K | 0.8mol/L | 0.8mol/L | 0.2mol/L | 0.6mol/L |
800K | 0.6mol/L | 0.6mol/L | 0.4mol/L | 1.2mol/L |
1000K | 0.4mol/L | 0.4mol/L | 0.6mol/L | 1.8mol/L |
(1)该反应的平衡常数表达式为K=
(2)能判断该反应是否已达到化学平衡状态的依据是
a.容器压强不变 b.c(CH4)=c(H2O)
c.v正(CH4)=v逆(H2) d .混合气体中c(CO)不变
氮化铝是共价键化合物,高碳热还原制备氮化铝的总反应化学方程式为(未配平):
Al2O3(s)+C(s)+N2(g)→AlN(s)+CO(g) ……①
某氮化铝样品中含有氧化铝杂质.已知氮化铝和NaOH溶液能反应,并产生氨气,其反应方程式为:AlN+NaOH+H2O→NaAlO2+NH3↑……②,
氧化铝也能与氢氧化钠溶液反应而全部溶解……③
(3)配平化学化学方程式①:
(4)反应②中产生气体的检验方法为
反应③的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】CO2转化成有机物可实现碳循环。在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
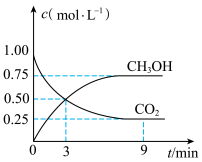
(1)从3min到9min,v(H2)=______ mol•L-1•min-1。
(2)能说明上述反应达到平衡状态的是______ (填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3molH2,同时生成1molH2O
D.v正(H2)=3v逆(H2O)
E.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为______ 。
(4)平衡时混合气体中CH3OH(g)的体积分数是______ 。
(5)一定温度下,第9分钟时v逆(CH3OH)______ (填“大于”、“小于”或“等于”)第3分钟时v正(CH3OH)。
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)从3min到9min,v(H2)=
(2)能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3molH2,同时生成1molH2O
D.v正(H2)=3v逆(H2O)
E.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为
(4)平衡时混合气体中CH3OH(g)的体积分数是
(5)一定温度下,第9分钟时v逆(CH3OH)
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】把二氧化碳“变废为宝”是实现碳达峰、碳中和的关键。
(1)体积为1 L的恒温密闭容器中,充入1 mol 和3 mol
和3 mol  ,在一定条件下反应:
,在一定条件下反应: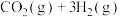
 。测得
。测得 和
和 的浓度变化随时间变化如图1所示。
的浓度变化随时间变化如图1所示。
___________ mol⋅L ⋅min
⋅min
(2)能说明上述反应达到平衡状态的是___________ 。(填字母)
a.混合气体的压强不随时间的变化而变化
b.单位时间内每生成1 mol ,同时生成3 mol
,同时生成3 mol 
c.反应中 和
和 的物质量浓度之比为1∶1
的物质量浓度之比为1∶1
(3)平衡时 的转化率为
的转化率为___________ 。
(4)我国学者提出的 催化加氢合成
催化加氢合成 的机理如图2(其中吸附在催化剂表面的物种用*标注)所示。下列说法正确的是
的机理如图2(其中吸附在催化剂表面的物种用*标注)所示。下列说法正确的是___________ 。(填字母) 的反应速率
的反应速率
b.反应机理表明 参与了
参与了 合成
合成 的反应
的反应
c.反应④中存在共价键的断裂和共价键的生成
(1)体积为1 L的恒温密闭容器中,充入1 mol
 和3 mol
和3 mol  ,在一定条件下反应:
,在一定条件下反应: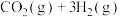
 。测得
。测得 和
和 的浓度变化随时间变化如图1所示。
的浓度变化随时间变化如图1所示。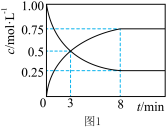

 ⋅min
⋅min
(2)能说明上述反应达到平衡状态的是
a.混合气体的压强不随时间的变化而变化
b.单位时间内每生成1 mol
 ,同时生成3 mol
,同时生成3 mol 
c.反应中
 和
和 的物质量浓度之比为1∶1
的物质量浓度之比为1∶1(3)平衡时
 的转化率为
的转化率为(4)我国学者提出的
 催化加氢合成
催化加氢合成 的机理如图2(其中吸附在催化剂表面的物种用*标注)所示。下列说法正确的是
的机理如图2(其中吸附在催化剂表面的物种用*标注)所示。下列说法正确的是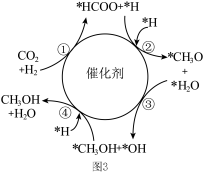
 的反应速率
的反应速率b.反应机理表明
 参与了
参与了 合成
合成 的反应
的反应c.反应④中存在共价键的断裂和共价键的生成
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】氨是最重要的氮肥,是产量最大的化工产品之一。其合成原理为:N2(g)+3H2(g) 2NH3(g)ΔH=-92.4 kJ·mol-1,在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应:
2NH3(g)ΔH=-92.4 kJ·mol-1,在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应:
(1)测得反应放出的热量_________ 92.4kJ。(填“小于”,“大于”或“等于”)
(2)当反应达到平衡时,N2和H2的浓度比是___________ ;N2和H2的转化率比是___________ 。
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量________ 。(填“变大”、“变小”或“不变”)
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将___________ (填“正向”、“逆向”或“不”)移动。
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将____________ (填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________ (填“大于”、“小于”或“等于”)原来的2倍。
 2NH3(g)ΔH=-92.4 kJ·mol-1,在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应:
2NH3(g)ΔH=-92.4 kJ·mol-1,在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应:(1)测得反应放出的热量
(2)当反应达到平衡时,N2和H2的浓度比是
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g) + 2N2(g)+ 6H2(g) Si3N4(s) + 12 HCl(g) ΔH<0
Si3N4(s) + 12 HCl(g) ΔH<0
(1)在一定温度下进行上述反应,若反应容器的容积为2 L, 3 min后达到平衡,测得固体的质量增加了2.80g,则H2的平均反应速率为___________ mol / (Lmin);该反应的平衡常数表达式K=___________
(2)上述反应达到平衡后,下列说法正确的是___________ 。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4的物质的量,平衡向左移动
d.其他条件不变,增大HCl的物质的量,平衡向左移动
(3) 一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是___________
a. 3v逆(N2) = v 正(H2)
b. v正 (HCl) = 4v 正(SiCl4)
c.混合气体密度保持不变
d. c(N2): c(H2) :c(HCl)= 1:3:6
(4)若平衡时H2和HCl的物质的量之比为 ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___________  (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
 Si3N4(s) + 12 HCl(g) ΔH<0
Si3N4(s) + 12 HCl(g) ΔH<0(1)在一定温度下进行上述反应,若反应容器的容积为2 L, 3 min后达到平衡,测得固体的质量增加了2.80g,则H2的平均反应速率为
(2)上述反应达到平衡后,下列说法正确的是
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4的物质的量,平衡向左移动
d.其他条件不变,增大HCl的物质的量,平衡向左移动
(3) 一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是
a. 3v逆(N2) = v 正(H2)
b. v正 (HCl) = 4v 正(SiCl4)
c.混合气体密度保持不变
d. c(N2): c(H2) :c(HCl)= 1:3:6
(4)若平衡时H2和HCl的物质的量之比为
 ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】一个已经处于化学平衡状态的可逆反应,如果改变反应条件,使平衡向正反应方向移动,反应物的转化率一定会增大吗___________ ?请加以说明___________
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】在一固定容积的密闭容器中,进行如下化学反应:CO2(g) + H2(g)⇌CO(g) + H2O(g)。其化学平衡常数K和温度t的关系如下:
请回答:
(1)上述反应正向进行时,反应为_______ 热反应(填“放”或“吸”)。
(2)能判断该反应已经达到化学平衡状态的依据是_______ 。
a.容器内压强不变 b.v正(H2) = v逆(CO) c.CO2的质量分数不变
(3)温度为850℃时,可逆反应CO (g) + H2O (g)⇌CO2 (g) + H2 (g) 在固定容积的密闭容器中进行,容器内各物质的浓度变化如下:
计算:3min时(CO的浓度)c1 =_______ mol/L,H2O (g)的转化率=_______ 。
(4)表中5min~6min之间数值发生变化,可能的原因是_______(单选)。
| t/℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答:
(1)上述反应正向进行时,反应为
(2)能判断该反应已经达到化学平衡状态的依据是
a.容器内压强不变 b.v正(H2) = v逆(CO) c.CO2的质量分数不变
(3)温度为850℃时,可逆反应CO (g) + H2O (g)⇌CO2 (g) + H2 (g) 在固定容积的密闭容器中进行,容器内各物质的浓度变化如下:
| 时间/min | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
计算:3min时(CO的浓度)c1 =
(4)表中5min~6min之间数值发生变化,可能的原因是_______(单选)。
| A.增加水蒸气 | B.降低温度 | C.使用催化剂 | D.增加氢气浓度 |
您最近半年使用:0次



