下列有关浓硫酸的叙述正确的是
①浓硫酸在常温下能够使铁、铝等金属钝化
②浓硫酸与铜加热反应后,铜片有剩余,硫酸完全反应
③浓硫酸具有吸水性,因而能使蔗糖炭化
④浓硫酸与过量的铜加热反应后,硫酸会有剩余
⑤浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
⑥浓硫酸与铁加热反应后,铁片有剩余,生成的气体除水蒸气外只有SO2
⑦浓硫酸具有强氧化性,常温下能与Cu发生剧烈反应
⑧浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2
⑨向5 mL 18 mol•L-1的浓硫酸中加入足量Cu并加热使其充分反应,被还原的H2SO4和生成的SO2气体均小于0.045 mol
①浓硫酸在常温下能够使铁、铝等金属钝化
②浓硫酸与铜加热反应后,铜片有剩余,硫酸完全反应
③浓硫酸具有吸水性,因而能使蔗糖炭化
④浓硫酸与过量的铜加热反应后,硫酸会有剩余
⑤浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
⑥浓硫酸与铁加热反应后,铁片有剩余,生成的气体除水蒸气外只有SO2
⑦浓硫酸具有强氧化性,常温下能与Cu发生剧烈反应
⑧浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2
⑨向5 mL 18 mol•L-1的浓硫酸中加入足量Cu并加热使其充分反应,被还原的H2SO4和生成的SO2气体均小于0.045 mol
| A.①②⑤ | B.①④⑨ | C.⑥⑦⑧ | D.③④⑨ |
20-21高一下·重庆沙坪坝·期中 查看更多[4]
四川省射洪中学校2022-2023学年高一下学期期中考试化学试题重庆第二十三中学校2021-2022学年高一下学期第一次月考化学试题(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)重庆市南开中学2020-2021学年高一下学期期中考试化学试题
更新时间:2021-08-06 10:47:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于浓硝酸和浓硫酸的叙述中正确的是
| A.常温下都可用铝制容器贮存 |
| B.露置在空气中,容器内酸液的质量都减轻 |
| C.常温下都能与铜较快反应 |
| D.露置在空气中,容器内酸液的浓度都增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列不能用浓硫酸干燥的是
| A.CO | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关实验操作,现象或结论不正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向氯水中通入适量 气体 气体 | 溶液褪至无色 |  比 比 酸性强 酸性强 |
| B | 浓 久置或光照 久置或光照 | 变黄色 | 浓 不稳定易分解 不稳定易分解 |
| C | 向蔗糖中滴加浓硫酸 | 蔗糖变黑 | 浓硫酸具有脱水性 |
| D | 向某盐溶液中加入浓 溶液,加热 溶液,加热 | 产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】关于非金属含氧酸及其盐的性质,下列说法正确的是
A.浓 具有强吸水性,能吸收糖类化合物中的水分并使其炭化 具有强吸水性,能吸收糖类化合物中的水分并使其炭化 |
B.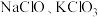 等氯的含氧酸盐均可用于制取氯气 等氯的含氧酸盐均可用于制取氯气 |
C.加热 与浓 与浓 混合物可制备 混合物可制备 ,说明 ,说明 比 比 酸性强 酸性强 |
D.浓 和稀 和稀 与 与 反应的还原产物分别为 反应的还原产物分别为 和 和 ,故稀 ,故稀 氧化性更强 氧化性更强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验不能达到相应实验目的的是
| A.实验室制Fe(OH)2 | B.制备并收集少量NO2气体 | C.验证CaO的吸水性 | D.验证浓H2SO4的脱水性、强氧化性 |
 |  |  | 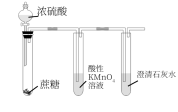 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学反应中会出现“一种物质过量,另一种物质仍不能完全反应”的特殊情况。下列反应中属于这种情况的是
①过量稀硫酸与块状石灰石;
②过量的氢气与氮气催化剂存在下充分反应;
③过量稀硝酸与铜反应;
④常温下将铝片投入到过量浓硫酸中;
⑤过量铜与浓硫酸反应;
⑥过量的锌与 的硫酸反应;
的硫酸反应;
①过量稀硫酸与块状石灰石;
②过量的氢气与氮气催化剂存在下充分反应;
③过量稀硝酸与铜反应;
④常温下将铝片投入到过量浓硫酸中;
⑤过量铜与浓硫酸反应;
⑥过量的锌与
 的硫酸反应;
的硫酸反应;| A.③④⑤ | B.②③⑤ | C.①②④⑤ | D.①②③④⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 证明Cu和浓H2SO4反应生成CuSO4 | 将铜与浓H2SO4反应后的溶液慢慢加入适量水中,边加边搅拌,溶液变蓝 |
| B | 测定硫酸铜晶体中结晶水的含量 | 加热盛有硫酸铜晶体的坩埚,待固体全部呈白色后将坩埚放置在铁架台上冷却,再称重 |
| C | 除去NaCl固体中混有的少量KNO3杂质 | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| D | 用NaCl固体配制100mL1.00mol•L-1NaCl溶液 | 将5.85gNaCl固体放在烧杯中,加入100mL蒸馏水,搅拌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某同学进行如下实验:
下列说法不正确 的是
| 实验 | 实验现象 | |
| ⅰ | 将铜粉加入试管中,再加入稀 | 溶液变蓝,液面上方呈浅红棕色;至不再产生气泡时,铜粉有剩余,余液呈酸性 |
| ⅱ | 继续向ⅰ中试管加入少量固体 | 又产生气泡,铜粉减少,液面上方呈浅红棕色 |
| ⅲ | 取饱和 溶液,加入少量固体 溶液,加入少量固体 和铜粉 和铜粉 | 无明显变化 |
A. 氧化性的强弱与其浓度大小有关 氧化性的强弱与其浓度大小有关 |
| B.ⅰ、ⅱ中铜粉减少的原因能用相同的离子反应解释 |
C.ⅰ中余液呈酸性的主要原因是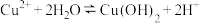 |
D.用一定浓度的 与 与 也能使铜粉溶解 也能使铜粉溶解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】CuSO4是一种重要的化工原料,有关制备途径及相关转化如图所示,下列有关说法错误的是
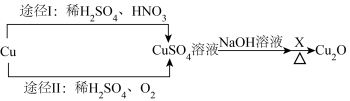

| A.X可以是葡萄糖 |
| B.途径I发生的是置换反应 |
| C.途径I、II相比,途径Ⅱ符合绿色化学思想 |
| D.制备等量的CuSO4,参加反应的n(HNO3):n(O2)=4:3 |
您最近一年使用:0次



