硫酸铜受热分解生成氧化铜和气体,受热温度不同生成的气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组通过设计以下探究性实验,探究测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验用到的仪器如下图所示:
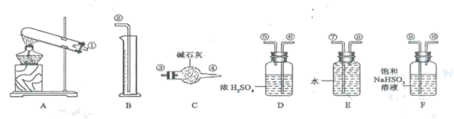
(1)[提出猜想]
①所得气体的成分可能只含_______ 一种。
②所得气体的成分可能含有_______ 二种。
③所得气体的成分可能含有_______ 三种。
(2)[实验探究]
实验操作过程(略),已知实验结束时,硫酸铜完全分解。请回答下列问题:
①请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为_______ (填序号)。
②若实验结束,B中量筒没有收集到水,则证明猜想_______ 。正确。
③若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3。请说明理由_______ 。
④有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学反应方程式:
一组:_______ ;二组:_______ 。

(1)[提出猜想]
①所得气体的成分可能只含
②所得气体的成分可能含有
③所得气体的成分可能含有
(2)[实验探究]
实验操作过程(略),已知实验结束时,硫酸铜完全分解。请回答下列问题:
①请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为
②若实验结束,B中量筒没有收集到水,则证明猜想
③若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3。请说明理由
④有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4的质量/g | 装置C增加的质量/g | 量筒中水的体积(折算成标准状况下气体的体积)/mL |
| 一 | 6.4 | 2.56 | 448 |
| 二 | 6.4 | 3.84 | 224 |
一组:
更新时间:2021-08-05 16:20:36
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某中学化学兴趣小组利用如下实验装置(部分加热装置已省略)探究SO2与Mg的反应及SO2的某些性质。据此回答相关问题:_______ ,A装置中产生的SO2可能混有少量的 ,B装置中的试剂可以是
,B装置中的试剂可以是_______ 。(填写序号)
a.NaOH溶液 b.浓硫酸 c.饱和 溶液
溶液
(2)类比分析、模型认知与证据推理是中学化学学习的重要方法之一、从物质分类上分析,SO2和CO2都是酸性氧化物,从化合价态角度分析,SO2和CO2都具有_______ (填具体的化学性质)。
(3)实验小组查阅相关资料整理出硫及其部分化合物的性质:①S单质难溶于水、非氧化性的酸溶液,微溶于酒精、易溶于 ;②MgS在冷水中易水解生成
;②MgS在冷水中易水解生成 、
、 、热水中易水解生成
、热水中易水解生成 、
、 ;③
;③ 是一种具有特殊臭味的气体。
是一种具有特殊臭味的气体。
实验1:取少量装置C的剩余固体样品加入稀盐酸,样品部分溶解,有黄色固体剩余,并伴有刺激性气味气体产生。
实验小组结合实验1现象,认为剩余固体中一定有S单质、MgO和MgS,MgS产生的原因点燃是:2Mg+SO2 2MgO+S;
2MgO+S;_______ (用化学方程式表示)。并对实验1产生气体的组成提出以下猜想:
猜想1:气体为H2
猜想2:气体为H2S
猜想3:气体为H2、H2S的混合气体
写出实验1中产生刺激性气味气体的化学方程式_______ ;由实验1现象可知_______ 不成立(填“猜想1”、或“猜想2”、或“猜想3”);
实验2:取少量装置C的剩余固体样品加入热水溶解、过滤,并往洗涤过后的滤渣加入足量稀盐酸,无气泡产生。由实验2现象可知_______ 不成立(填“猜想1”、或“猜想2”、或“猜想3”)。
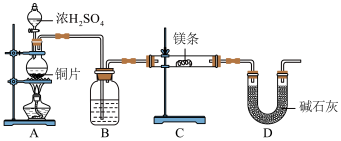
 ,B装置中的试剂可以是
,B装置中的试剂可以是a.NaOH溶液 b.浓硫酸 c.饱和
 溶液
溶液(2)类比分析、模型认知与证据推理是中学化学学习的重要方法之一、从物质分类上分析,SO2和CO2都是酸性氧化物,从化合价态角度分析,SO2和CO2都具有
(3)实验小组查阅相关资料整理出硫及其部分化合物的性质:①S单质难溶于水、非氧化性的酸溶液,微溶于酒精、易溶于
 ;②MgS在冷水中易水解生成
;②MgS在冷水中易水解生成 、
、 、热水中易水解生成
、热水中易水解生成 、
、 ;③
;③ 是一种具有特殊臭味的气体。
是一种具有特殊臭味的气体。实验1:取少量装置C的剩余固体样品加入稀盐酸,样品部分溶解,有黄色固体剩余,并伴有刺激性气味气体产生。
实验小组结合实验1现象,认为剩余固体中一定有S单质、MgO和MgS,MgS产生的原因点燃是:2Mg+SO2
 2MgO+S;
2MgO+S;猜想1:气体为H2
猜想2:气体为H2S
猜想3:气体为H2、H2S的混合气体
写出实验1中产生刺激性气味气体的化学方程式
实验2:取少量装置C的剩余固体样品加入热水溶解、过滤,并往洗涤过后的滤渣加入足量稀盐酸,无气泡产生。由实验2现象可知
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学拟在实验室进行“Na2CO3纯度的分析”实验,下面是他的实验过程:他先设计如图实验装置,

其中:
A装置盛有无水Na2CO3试剂(杂质不与水和酸反应)10.0g,分液漏斗内盛有稀硫酸。
B装置内为碱石灰固体,根据碱石灰质量的增重可计算Na2CO3的纯度。他重复了三次正确操作,结果数据出现了较大偏差。
(1)你分析出现较大偏差的原因。
设原容器内CO2气体的含量可忽略不计,各容器内反应完全。
①____ ;
②____ ;
③____ 。
通过仔细分析,该同学又设计了一套实验装置(如图),可供选的试剂和药品还有:锌片、浓硫酸、氢氧化钠溶液,碳酸钙固体、蒸馏水。
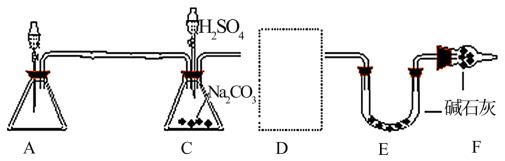
(2)重新设计的装置尚未完整,D虚框内需加上的装置图(仪器和药品)____ 。
(3)A装置中分液漏斗所盛液体为___ ,锥形瓶内药品为___ 。
(4)A装置在整套装置中的作用是___ 。
(5)D装置的的作用是___ 。
(6)F装置的的作用是___ 。
(7)如果实验后E装置质量增重3.96g,则无水Na2CO3的纯度为___ 。

其中:
A装置盛有无水Na2CO3试剂(杂质不与水和酸反应)10.0g,分液漏斗内盛有稀硫酸。
B装置内为碱石灰固体,根据碱石灰质量的增重可计算Na2CO3的纯度。他重复了三次正确操作,结果数据出现了较大偏差。
(1)你分析出现较大偏差的原因。
设原容器内CO2气体的含量可忽略不计,各容器内反应完全。
①
②
③
通过仔细分析,该同学又设计了一套实验装置(如图),可供选的试剂和药品还有:锌片、浓硫酸、氢氧化钠溶液,碳酸钙固体、蒸馏水。

(2)重新设计的装置尚未完整,D虚框内需加上的装置图(仪器和药品)
(3)A装置中分液漏斗所盛液体为
(4)A装置在整套装置中的作用是
(5)D装置的的作用是
(6)F装置的的作用是
(7)如果实验后E装置质量增重3.96g,则无水Na2CO3的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某膨松剂由碳酸氢钠与碳酸钠组成。某学校兴趣小组为研究该膨松剂中碳酸氢钠的含量,利用下图所示装置进行相关实验。已知各装置中的试剂皆为足量。_________ ;
(2)装置C的作用是_________ ;
(3)装置E中所用仪器的名称是_________ ;
(4)已知碱石灰是固体氢氧化钠和氧化钙的混合物,则装置D中NaOH发生化学方程式为_________ ;
(5)将一定质量的该膨松剂样品装入装置B中,测定实验前后装置_________ (填装置对应的字母符号)的质量,其质量差即为样品产生的CO2的质量。
(6)上述实验中,若没有装置E,可能会造成测定结果_________ (填“偏大”、“偏小”或“不变”);
(7)若上述实验中加入的样品质量为30g,测得生成的CO2的质量为6.6g。则样品中NaHCO3的质量分数为_________ 。

(2)装置C的作用是
(3)装置E中所用仪器的名称是
(4)已知碱石灰是固体氢氧化钠和氧化钙的混合物,则装置D中NaOH发生化学方程式为
(5)将一定质量的该膨松剂样品装入装置B中,测定实验前后装置
(6)上述实验中,若没有装置E,可能会造成测定结果
(7)若上述实验中加入的样品质量为30g,测得生成的CO2的质量为6.6g。则样品中NaHCO3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体。某研究性学习小组对蓝色固体的成分进行了如下探究。
(一)猜想与假设:
猜想一:固体为CuCO3,理由:___________ (用化学反应方程式表示)。
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈___________ (填“酸”或“碱”)性。
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①Cu(OH)2和CuCO3晶体均不带结晶水;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
(三)设计与实验:
I.固体的获取:
(1)将反应后的固、液混合物经_______ 、洗涤、低温烘干得蓝色固体。
(2)判断固体已洗净的方法及现象______
II.用下图所示装置,定性探究固体的成分。

(3)若用装置A、B组合进行实验,B中无现象,则猜想________ 正确;
(4)若用装置A、C组合进行实验,C中无现象,则猜想_______ 正确;
(5)小组同学将装置按A、_______ 、______ (填“B”、“C”)的顺序组合进行实验,验证出猜想三是正确的,实验中:B中的现象为_______ ,C中的现象为_______ 。
结论:固体为Cu(OH)2和CuCO3的混合物。
III.固体成分定量测定:
已知Cu(OH)2的分解温度为66℃∽68℃,CuCO3的分解温度为200℃∽220℃。设固体的组成为aCu(OH)2•bCuCO3.小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如图,

请根据图示回答下列问题:
(6)写出AB、CD段发生反应的化学方程式:
AB段:________ ;
CD段:_______ ;
(7)通过计算可得:a∶b=_______ 。
(8)若将24.0g剩余固体继续加热到更高的温度,发现固体质量减少了2.4g后质量不再改变,写出此过程中可能发生反应的化学方程式:_______ 。
(一)猜想与假设:
猜想一:固体为CuCO3,理由:
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①Cu(OH)2和CuCO3晶体均不带结晶水;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
(三)设计与实验:
I.固体的获取:
(1)将反应后的固、液混合物经
(2)判断固体已洗净的方法及现象
II.用下图所示装置,定性探究固体的成分。

(3)若用装置A、B组合进行实验,B中无现象,则猜想
(4)若用装置A、C组合进行实验,C中无现象,则猜想
(5)小组同学将装置按A、
结论:固体为Cu(OH)2和CuCO3的混合物。
III.固体成分定量测定:
已知Cu(OH)2的分解温度为66℃∽68℃,CuCO3的分解温度为200℃∽220℃。设固体的组成为aCu(OH)2•bCuCO3.小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如图,

请根据图示回答下列问题:
(6)写出AB、CD段发生反应的化学方程式:
AB段:
CD段:
(7)通过计算可得:a∶b=
(8)若将24.0g剩余固体继续加热到更高的温度,发现固体质量减少了2.4g后质量不再改变,写出此过程中可能发生反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】常温下氯化铜为浅绿色固体,易潮解,实验室设计如下实验制备无水氯化铜。

A B C D
回答下列问题:
(1)盛放浓盐酸的仪器名称为______ 。
(2)实验操作的先后顺序为______ (填选项字母)。
a.点燃A处酒精灯 b.点燃C处酒精灯 c.按图连接装置 d.向装置中添加相应药品 e.检查装置气密性
(3)装置A中发生反应的离子方程式为______ 。
(4)填写表中装置加入试剂的目的。
(5)某同学提出该装置存在缺陷,应增加一个干燥装置,该装置应该加在______ (填序号)。
A.A与B之间 B.B与C之间 C.C与D之间 D.D之后
(6)用改进后的装置进行实验,若C中开始时加入Cu粉6.40g,反应结束后,得到12.79g固体(设除 外,Cu未与其他物质发生反应),则固体中
外,Cu未与其他物质发生反应),则固体中 的物质的量为
的物质的量为______ 。

A B C D
回答下列问题:
(1)盛放浓盐酸的仪器名称为
(2)实验操作的先后顺序为
a.点燃A处酒精灯 b.点燃C处酒精灯 c.按图连接装置 d.向装置中添加相应药品 e.检查装置气密性
(3)装置A中发生反应的离子方程式为
(4)填写表中装置加入试剂的目的。
| 装置序号 | 加入的试剂 | 加入该试剂的目的 |
| B | 浓 | |
| D |  溶液 溶液 |
A.A与B之间 B.B与C之间 C.C与D之间 D.D之后
(6)用改进后的装置进行实验,若C中开始时加入Cu粉6.40g,反应结束后,得到12.79g固体(设除
 外,Cu未与其他物质发生反应),则固体中
外,Cu未与其他物质发生反应),则固体中 的物质的量为
的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯苯在染料、医药工业中用于制造苯酚、硝基氯苯、苯胺、硝基酚等有机中间体。实验室中制备氯苯的装置如图所示(夹持仪器已略去)。请回答下列问题:
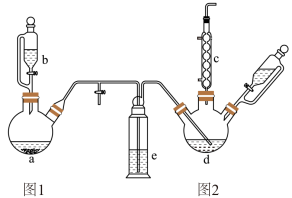
(1)仪器a中盛有KMnO4晶体,仪器b中盛有浓盐酸。打开仪器a中的活塞,使浓盐酸缓缓滴下,仪器中产生黄绿色气体,用离子方程式表示产生该现象的原因:____ 。
(2)仪器b中细玻璃导管的作用是_____ 。
(3)仪器d内盛有苯、FeCl3粉末,仪器a中生成的气体经过仪器e进入到仪器d中。
①仪器e的名称是洗气瓶,内盛装的试剂是____ ;
②仪器d中的反应进行过程中,保持温度在40-60℃,以减少副反应发生。仪器d的加热方式最好采用___ 加热。
(4)仪器c的作用是___ ;d中发生的化学反应方程式是____ 。
(5)该方法制备的氯苯中含有很多杂质,工业生产中通过水洗,然后通过碱洗,再水洗,最后通过分液得到含氯苯的有机物的混合物,混合物成分及沸点如图2表格所示:
①碱洗前先进行水洗的目的是____ ;
②取该有机物的混合物中的氯苯时,采用蒸馏的方法,收集___ ℃左右的馏分。

(1)仪器a中盛有KMnO4晶体,仪器b中盛有浓盐酸。打开仪器a中的活塞,使浓盐酸缓缓滴下,仪器中产生黄绿色气体,用离子方程式表示产生该现象的原因:
(2)仪器b中细玻璃导管的作用是
(3)仪器d内盛有苯、FeCl3粉末,仪器a中生成的气体经过仪器e进入到仪器d中。
①仪器e的名称是洗气瓶,内盛装的试剂是
②仪器d中的反应进行过程中,保持温度在40-60℃,以减少副反应发生。仪器d的加热方式最好采用
(4)仪器c的作用是
(5)该方法制备的氯苯中含有很多杂质,工业生产中通过水洗,然后通过碱洗,再水洗,最后通过分液得到含氯苯的有机物的混合物,混合物成分及沸点如图2表格所示:
| 有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
| 沸点/℃ | 80 | 132.2 | 180.4 | 173.0 | 174.1 |
②取该有机物的混合物中的氯苯时,采用蒸馏的方法,收集
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】除一种元素外,其余由周期表中前20号元素组成的物质A、B、C、D、E,它们间的反应关系如下图所示:

(1)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则B的化学式为_______ 。写出该反应的离子方程式_______ 。
(2)若A和B都是盐,A难溶于水而B易溶于水,D不溶于稀硝酸,C为无色无味气体,则B的化学式为_______ 。写出该反应的离子方式_______ 。
(3)A是2:1型的离子化合物,B是正盐,D既可溶于盐酸又可溶于NaOH溶液,且A与B以物质的量之比为3:1恰好完全反应,推知B的化学式为_______ ;写出该反应的化学方程式:_______ 。
(4)若A是一个1:2型的离子化合物,A与B的溶液反应时只生成C、D和水;C的燃烧热为QkJ/mol,其燃烧产物通过装有碱石灰干燥管或浓硫酸的洗气瓶,两者质量都增重,则A的电子式_______ ;C燃烧的热化学方程式为_______ 。

(1)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则B的化学式为
(2)若A和B都是盐,A难溶于水而B易溶于水,D不溶于稀硝酸,C为无色无味气体,则B的化学式为
(3)A是2:1型的离子化合物,B是正盐,D既可溶于盐酸又可溶于NaOH溶液,且A与B以物质的量之比为3:1恰好完全反应,推知B的化学式为
(4)若A是一个1:2型的离子化合物,A与B的溶液反应时只生成C、D和水;C的燃烧热为QkJ/mol,其燃烧产物通过装有碱石灰干燥管或浓硫酸的洗气瓶,两者质量都增重,则A的电子式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】取一定质量的NaBr、NaI的混合物平均分成五等份,分别加水配成溶液并编号为甲、乙、丙、丁和戊,再分别向各溶液中通入一定体积的氯气,将反应后所得溶液蒸干灼烧得固体,通入氯气的体积与最终所得固体质量记录如下:
(1)填写表中空白_______ ,_______ ,_______ ,_______ 。
(2)标准状况下通入Cl2的体积V为_______ ,原混合物中NaBr的物质的量为____________ 。
编号 | 甲 | 乙 | 丙 | 丁 | 戊 |
固体组成 | NaCl | ||||
Cl2的体积/mL | V | 2V | 3V | 4V | 5V |
固体质量/g | 56.41 | 47.26 | 38.11 | 33.67 | 29.25 |
(2)标准状况下通入Cl2的体积V为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】将电解铜阳极泥与浓硫酸混合,于443~573K焙烧数小时,使其中硒、碲转变为二氧化物,其它物质转化为硫酸盐。然后升温至773~873K,使二氧化硒挥发(碲化合物不挥发)进入吸收塔被水吸收,与同被吸收的其它气体在溶液中发生反应,于363K加热Ih,得到硒单质。
(1)写出硒、碲、铜、硒化亚铜、硒化银与浓硫酸反应的化学方程式;___________
(2)写出二氧化硒气体进入吸收塔被水吸收和生成硒的反应方程式;___________
(3)称取6.000 g电解铜阳极泥样品以合适方法溶解,配成250.00 mL硫磷混酸溶液。移取上述溶液25.00 mL于锥形瓶中,加入2000 mL 0.005000 mol· L-1K2Cr2O7标准溶液(此时只有Te(IV )反应生成Te( VI)。待反应完全后,滴入2~3滴二苯胺作指示剂,以0.05000 mol· L-1Fe2+标准溶液滴到终点,耗去10.00 mL。另取一份上述样品溶液25.00mL于锥形瓶中,加入25.00mL0.01000 mol· L-1KMnO4标准溶液(此时Se(IV)、Te(IV )反应生成Se( VI))和Te( VI))。反应完全后,用0. 05000 mol· L-1Fe2+标准溶液滴至终点,消耗15. 00 mL。请计算电解铜阳极泥中Se%和Te%。___________
(1)写出硒、碲、铜、硒化亚铜、硒化银与浓硫酸反应的化学方程式;
(2)写出二氧化硒气体进入吸收塔被水吸收和生成硒的反应方程式;
(3)称取6.000 g电解铜阳极泥样品以合适方法溶解,配成250.00 mL硫磷混酸溶液。移取上述溶液25.00 mL于锥形瓶中,加入2000 mL 0.005000 mol· L-1K2Cr2O7标准溶液(此时只有Te(IV )反应生成Te( VI)。待反应完全后,滴入2~3滴二苯胺作指示剂,以0.05000 mol· L-1Fe2+标准溶液滴到终点,耗去10.00 mL。另取一份上述样品溶液25.00mL于锥形瓶中,加入25.00mL0.01000 mol· L-1KMnO4标准溶液(此时Se(IV)、Te(IV )反应生成Se( VI))和Te( VI))。反应完全后,用0. 05000 mol· L-1Fe2+标准溶液滴至终点,消耗15. 00 mL。请计算电解铜阳极泥中Se%和Te%。
您最近一年使用:0次



